ОПЫТ ЛЕЧЕНИЯ ВНЕПЕЧЕНОЧНЫХ ПОРТОСИСТЕМНЫХ ВАСКУЛЯРНЫХ АНОМАЛИЙ С ИСПОЛЬЗОВАНИЕМ ГИДРАВЛИЧЕСКОГО ОККЛЮДЕРА
Еще фото
Автор (ы): А.Н. ЛАПШИН, С.Г. АТАНАСОВА, П.В. БЕЛОКОПЫТОВ, Т.В. ПИМЧЕНКО, С.К. СОБАКИНА
Организация(и): Инновационный Ветеринарный Центр Московской ветеринарной академии
Журнал: №2 - 2018
УДК: 619:616.624-089
Ключевые слова: портосистемные шунты, портосистемные васкулярные аномалии, гидравлический окклюдер
Key words: portosystemic vascular anomalies, portosystemic shunts
Сокращения: ПСВА – портосистемные васкулярные аномалии, ГО – гидравлический окклюдер
Аннотация
Использование гидравлического окклюдера – новая и очень перспективная хирургическая техника для лечения портосистемных шунтов
Summary
Hydraulic occluder placement is new and very promising surgical teqnique for portosystemic shunts treatments
Введение
Портосистемные васкулярные аномалии(ПСВА) – группа сосудистых патологий печени. Наиболее частой ПСВА являются портосистемные шунты. Портосистемные шунты – это сосудистыми аномалии, которые характеризуются наличием соединения между сосудами воротной вены печени и системным кровотоком. Данное сосудистое соединение между двумя системами обеспечивает частичное, но значимое дренирование крови от желудка, кишечника, селезенки и поджелудочной железы в обход печеночных синусов напрямую в каудальную полую или непарную вены. Зачастую данное шунтирование крови в обход печени не носит абсолютный характер и мимо печени проходит лишь некий объем крови, который нельзя назвать постоянной единицей. Симптоматика портосистемных васкулярных аномалий напрямую зависит от объема шунтирующей крови и может быть представлена в виде выраженного и постоянного процесса, так и эпизодических изменений в общем состоянии.
Выделяют 3 основных группы симптомов: урологические, гастроэнтерологические и неврологические.
Наиболее часто встречаемые симптомы со стороны ЦНС: атаксия, ступорное состояние, хождение по кругу, слепота, эпилептиформные приступы и комотозное состояние. Урологические симптомы: нефролитиаз, уретеролитиаз, уролитиаз, цистит, обструкция уретры. Гастроэнтерологические: хроническая диарея, рвота с кровью, избирательный аппетит.
Диагностика портосистемных васкулярных аномалий сводится к лабораторным и визуальным методам. При выполнении рутинных лабораторных исследований у животных с ПСВА наиболее часто выявляют гипопротеинемию, гипоальбуминемию, гипогликемию, также могут быть определены низкие концентрации мочевины, креатинина и умеренное повышение печеночных ферментов. В общем клиническом анализе крови может быть выявлены лейкоцитоз и нерегенеративная анемия.
Функциональные пробы традиционно показывают значительное повышение уровня желчных кислот и свободного аммиака. Для оценки последующей эффективности проводимого лечения может быть выполнено исследование крови на содержание C-пептида, что при динамическом исследовании может показать восстановление функции печени, а в ряде случаев верифицировать макроскопические портосистемные шунты от микроваскулярной дисплазии. К сожалению, С-пептид в настоящее время невозможно исследовать в РФ. Важным в классификации портосистемных васкулярных аномалий является определение анатомической локализации. По анатомической локализации шунты подразделяются на внутрипеченочные и внепеченочные. Внутрипеченочные соответственно классифицируются, исходя из того какая печеночная вена соединена с интрагепатической браншей воротной вены и разделяются на право-, левосторонние и центральные внутрипеченочные шунты. Внепеченочные шунты подразделяются на портокавальные, портоазигональные, а также может быть выявлено так называемое azygous continuation с портоазигональным шунтом.
В настоящее время существуют 4 основные концепции в хирургическом лечении внепеченочных портосистемных шунтов: тотальная окклюзия (лигирование, эндоваскулярное лечение), парциальная окклюзия (частичное лигирование, установка целлофанового бандажа – ЦБ), постепенная окклюзия (импантация амероидного констриктора, имплантация целлофанового бандажа), а также контролируемая постепенная окклюзия (гидравлический окклюдер). Выбор методики лечения зачастую обусловлен предпочтениями врача и финансовыми возможностями представителей пациентов.
Стоит немного пояснить ситуацию с хирургическими предпочтениями. В выборе методики на основе предпочтений врача-хирурга нет ничего негативного и зачастую это обусловлено рядом факторов, таких, как отсутствие хорошо доказанных фактов о превосходстве одной методики над другой, в особенности в РФ. Но, с другой стороны, в настоящий момент появляются сравнительные анализы различных методик, что, безусловно, изменит клинические подходы. Наиболее свежий сравнительный анализ от Traverson и коллег (опубликовано в феврале 2018 г.), результаты которого показали отсутствие разницы в послеоперационных рисках, сравнивая технику имплантации амероидного констриктора (АК) и целлофанового бандажа (ЦБ). Но определили более значительный риск формирования резидуального шунта. По данным Traverson, на 26 прооперированных пациентов с использованием ЦБ резидуальный шунт был выявлен у 31,6% пациентов. Наш опыт в использовании ЦБ показывает 10% риск развития резидуального шунта (2 пациента из 19 прооперированных). Представленные данные можно трактовать как полное превосходство АК над ЦБ, но не стоит забывать, что в РФ вопрос стерилизации АК стоит особенно остро ввиду отсутствия полноценной газовой стерилизации.
Имея ввиду эти данные, можно сделать вывод, что новые методики хирургического лечения внепеченочных ПСВА могут быть с успехом интегрированы (рис. 1,2).
Описание техники
Техника хирургического лечения с использованием гидравлического окклюдера была выполнена у 2 пациентов. Гидравлический окклюдер представляет собой полую манжету, соединенную с трубкой и подсоединяемой порт-системой (рис. 3).
Клинический случай 1
Кот породы мейн-кун, возраст при поступлении на операцию – 2,8 лет. Из истории болезни известно, что животное с 7 месячного возраста перестало набирать вес и появились жалобы на хроническую диарею. Причиной обращения стало учащенное мочеиспускание. При ультразвуковом исследовании была выявлена микрогепатия.
Тест с желчными кислотами показал результат: 5,9 мкмоль/л до кормления и 19,9 мкмоль/л, параметры крови по ОКА и рутинным Б/Х показателям были в рамках референтных значений. Была выполнена компьютерная томография и поставлен диагноз: «Единичный внепеченочный портофренальный шунт». Было принято решение об имплантации гидравлического окклюдера.
Клинический случай 2
Йоркширский терьер, 10 месяцев. Поступил с жалобами на вялость (малую активность). Были выявлены следующие отклонения от референтных значений параметров крови. Мочевина: 1,9 ммоль/л, альбумин: 19 г/л, ЖК 58,1 мкмоль/л и 84,4 мкмоль/л.
Была выполнена компьютерная томография и поставлен диагноз: «Eдиничный внепеченочный портофренальный шунт». Далее была выполнена установка целлофанового бандажа (ЦБ). В течение 3 мес. с момента имплантации ЦБ владельцы пациента не отметили выраженного улучшения самочувствия, и наметилась негативная динамика (эпизодические эпилептиформные приступы, ступорное состояние, общий белок: 38.7 г/л, альбумин: 23.3 г/л, глюкоза: 2.15 мкмоль/л, мочевина: 3.07 mmol/l ).
Была выполнена повторная компьютерная томография и установлено наличие тока крови по портосистемному шунт, что может быть связано с формированием резидуального шунта или отсутствия тромбирования ПСВА после имплантации ЦБ. Принято решение об имплантации гидравлического окклюдера.
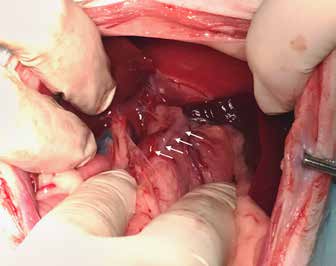
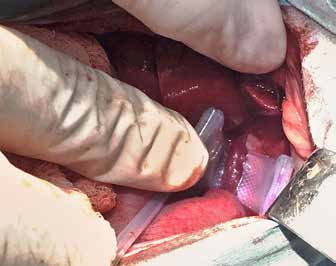
Техника имплантации ГО
Лапаротомия по белой линии живота. Идентификация портосистемного шунта. Выполнение диссекции и измерение диаметра шунтирующего сосуда. Выбор манжеты ГО из расчетов, что диаметр манжеты ГО должен быть равен диаметру сосуда, умноженного на 2. Длина диссекции шунта не должна превышать ширины выбранной манжеты (Рис. 4,5). После успешного позиционирования манжеты соединяющая трубка выводится через прокол на брюшной стенке. Далее формируется карман между фасцией брюшной стенки и подкожной жировой клетчаткой. В это место выводится трубка от манжеты. Далее в трубку вводится катетер и производится промывание катетера и устранение тем самым воздуха из полостей импланта. После чего трубка соединяется с порт-системой и проверяется герметичность введением и аспирацией физиологического раствора (рис. 6) . Порт-система подшивается к фасции брюшной стенки с небольшим захватом мышечных волокон, затем выполняется послойное ушивание раны вместе с подкожным карманом для порт-системы (рис. 7).
Результаты
В клиническом случае 1 имплантация ГО была произведена после диссекции сальника по малой кривизне желудка, в месте, где был выявлен шунтирующий сосуд. Анатомическое расположение было достаточно удобным, поэтому проведение диссекции в области левой печеночной вены и диафрагмальной вены не потребовалось. Контрольная портография непосредственно после имплантции показала отсутствие компрессии контрастной колонны, что можно было интерпретировать как корректное позиционирование манжеты. Контрольное КТ было выполнено через 4 недели, и оно показало отсутствие тока контраста по портофренальному шунту, а также отсутствие множественных шунтов.
В клиническом случае 2 мы столкнулись со сложностью процесса диссекции портосистемного шунта по месту первой операции. Выраженный спаечный процесс не позволил осуществить повторную диссекцию по месту, ввиду это пришлось выполнять диссекцию в области левой печеночной вены. Данный этап был достаточно трудозатратным и потенциально опасным ввиду работы в непосредственной близости от магистральных сосудов. Таким образом, манжета была размещена между печенью и диафрагмой, что создавало определенные условия для одномоментой окклюзии шунта в момент имплантации. В течение месяца после операции у пациента было зафиксировано значительное улучшение клинического состояния, снижение концентрации желчных кислот и повышение уровня альбумина и мочевины.
Обсуждение
Техника постепенной контролируемой окклюзии с использованием гидравлического окклюдера должна предоставлять пациенту и специалисту полностью подконтрольный процесс закрытия шунтирующего сосуда. С другой стороны, тканевая реакция на имплантируемую манжету, которая схожа по своей сути с результатом имплантации искусственного уретрального сфинктера в виде развития периуретрального рубца. В то же время особенностью работы данной техники при взаимодействии с сосудами большего диаметра является отсутствие спонтанного закрытия шунта. Основными плюсами данной техники мы видим возможность контроля резидуального шунта в случае его возникновения в постоперационном периоде, а также отсутствие вопросов, связанных с стерилизацией имплантов. Данная техника, безусловно, должна быть рекомендована при хирургии реканализации или формирования резидуального шунта. В остальных случаях данная методика может рассматриваться как один из методов, который требует более глобального изучения.
Конфликт интересов
Д-р Антон Лапшин декларирует, что является лицом, представляющим интересы Norfolk Vet Products на территории РФ. Norfolk Vet Products – производитель гидравлических окклюдеров под названием HSO ( Hepatic Shunt Occluder).
По всем вопросам пишите: lapshindvm@gmail.com
Литература
1. Adin CA, Sereda CW,Thompson MS, Wheeler JL, Archer LL. Outcome associated with use of a percutaneously controlled hydraulic occluder for treatment of dogs with intrahepatic portosystemic shunts. J Am Vet Med Assoc. 2006, Dec 1;229(11):1749-55.
2. Sereda CW, Adin CA, Ginn PE, Farese JP.Evaluation of a percutaneously controlled hydraulic occluder in a rat model of gradual venous occlusion. Vet Surg. 2005 Jan-Feb;34(1):35-42.
3. Traverson M, Lussier B, Huneault L, Gatineau M.Comparative outcomes between ameroid ring constrictor and cellophane banding for treatment of single congenital extrahepatic portosystemic shunts in 49 dogs (1998-2012). Vet Surg. 2018 Feb;47(2):179-187. doi: 10.1111/vsu.12747. Epub 2017 Dec 16.
4. Parry AT, White RN.Post-temporary ligation intraoperative mesenteric portovenography: comparison with CT angiography for investigation of portosystemic shunts. J Small Anim Pract. 2018 Feb;59(2):106-111. doi: 10.1111/jsap.12786. Epub. 2017, Nov. 24.





Назад в раздел

















