ХИЛОТОРАКС У КОШЕК. ДИАГНОСТИКА И МЕТОДЫ ЛЕЧЕНИЯ/Chylothorax in cats. Diagnosis and various methods of treatment
Автор (ы): П.В. Белокопытов, А.Н. Лапшин, С.К.Собакина, С.Г. Атанасова, Т.В.Пимченко
Организация(и): Инновационный Ветеринарный Центр Московской ветеринарной академии
Журнал: №3 - 2018
УДК: 619:616.131
Аннотация
В статье описаны различные методы диагностики хилоторакса и методы хирургического лечения.
Summary
The article describes various methods for the diagnosis of chylothorax and methods of surgical treatment.
Введение
Хилоторакс – прогрессирующее накопление хилезной жидкости (лимфы с большим содержанием липидов) в плевральной (рис. 1) полости, обусловленное его истечением из грудного протока.
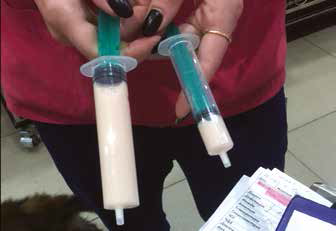
Рис. 1. Жидкость аспирированная из плевральной полости кошки при хилотораксе
Считается, что накопление хилезного выпота происходит вторично по отношению к уменьшенному дренированию лимфы по грудному лимфатическому протоку в краниальную полую вену. Пациенты с хилотораксом должны оцениваться по первичной или основной причине их выпота. Таковыми причинами являются первичная сердечная патология (кардиомиопатия, дирофиляриоз, пороки правых отделов сердца), перикардиальный выпот, неоплазия, травма грудного лимфатического протока, тромбоз полой вены. При невозможности выявления первичной причины выпота применяют термин идиопатический хилоторакс [6].
Диагностика сводится к визуальным и лабораторным методам.
После стабилизации состояния и улучшения дыхательного статуса необходимо выполнить рентгенологическое исследование для исключения новообразований в органах грудной клетки и средостения. Необходимо исключить кардиопатологии (ЭХОКГ), а также травму грудного лимфатического протока (КТ и лимфангиография) [4,5,6]. (Рис. 2).
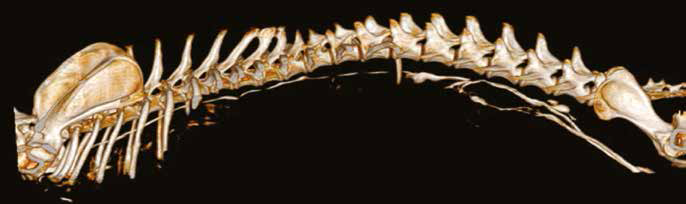
Рис. 2. Лимфангиография, выполненная путем введения контрастного агента в подколенный лимфатический узел или семенник
(собственность Андрея Герасимова и Марии Азаровой, СПБ)
В биохимическом анализе крови зачастую выявляют гипоальбуминемию и гипопротеинемию. При исследовании выпота обнаруживается большое количество триглицеридов, а при микроскопии определяется большое количество лимфоцитов. Также необходимо исключить вирусы лейкемии (FeLV) и иммунодефицита кошек (ВИК).
Лечение хилоторакса должно быть направлено на исправление первичного заболевания, если диагностируется основная причина выпота [1,2,3,6].
Существуют как консервативные, так и хирургические методы лечения хилоторакса.
Консервативное лечение идиопатического хилоторакса сводится к диете с низким содержанием жиров, назначении рутина, октреотида, а также аспирации жидкости из плевральной полости по мере необходимости. Отсутствие хилоторакса при данном лечении трудно отличить от спонтанного разрешения, однако такое разрешение более вероятно в случае травматического хилоторакса. Продолжительность лечения консервативным методом у кошек и собак может составлять от 2 до 8 недель, но может быть и более быстрым – 1-2 недели в случае травматической причины проблемы хилоторакса [6]. Осложнения при повторяющихся торакоцентезах бывают редко, но среди них травматизация легкого, инфицирование плевральной полости при несоблюдении принципов асептики и антисептики.
Хирургическое вмешательство рассматривается, если пациент не отвечает на консервативное лечение. Общепринятыми хирургическими методами и комбинациями у собак и кошек являются лигирование грудного лимфатического протока (TDL), TDL с перикардэктомией, абляция цистерны хили с TDL, эмболизация грудного лимфатического протока, плевроперитонеальное шунтирование.
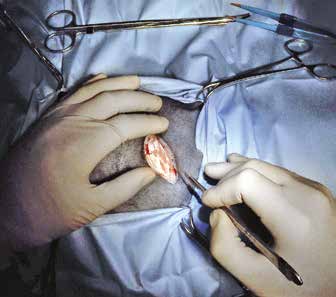
Традиционная методика проведения хирургического лечения кошек в нашей операционной проходит следующим образом. Пациент позиционируется на правом боку. Вся левая боковая поверхность тела от подмышечной области до топографического расположения маклока подготавливается с соблюдением принципа аспетики и антисептики. Отступив от крайнего ребра 2 см, мы выполняем паракостальную минилапаротомию (рис. 3).
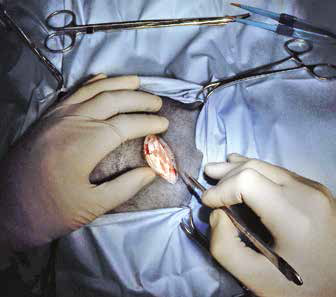
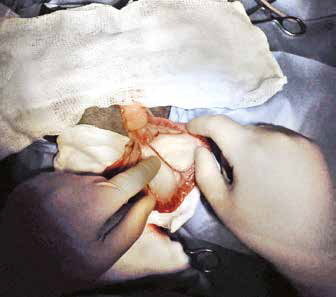
Рис. 3. Парокостальная минилапаротомия Рис. 4. Подготовка перед введением контрастного агента в мезентериальный лимфатический узел
Цель данного приема – выполнение доступа к системе мезэнтериальных лимфатических узлов для проведения контрастирования и процедуры интраоперационной визуализации грудного лимфатического протока и цистерны хили (рис. 4).
После визуализации любого из мезентериальных лимфатических узлов в него с помощью инсулиновой иглы делается инъекция контрастного агента (йогексол в объеме 0,5-1,5 мл на исследование кошки, в зависимости от качества контрастирования). Далее выполняется серия интраоперационных рентгеновских снимков или рентгеноскопическое исследование в режиме 4-8 fps/сек. Выполняется оценка рентгенографической анатомии цистерны хили и грудного лимфатического протока (рис. 5-8) .
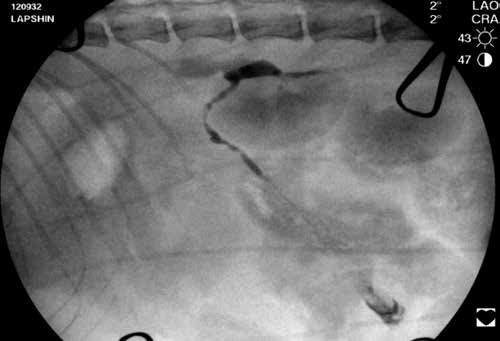
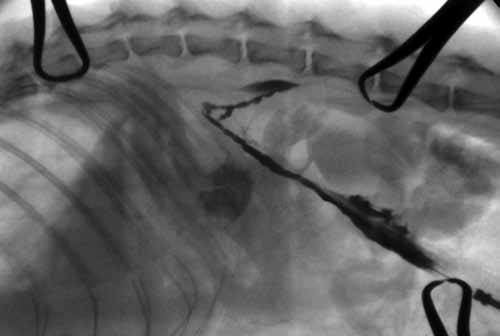
Рис. 5. Пример лимфангиографии и заполнение контрастом Рис. 6. Пример лимфангиографии №2 и заполнение контрастом
цистерны хили. Окрашен лимфатический сосуд цистерны хили, также окрашен лимфатический сосуд.
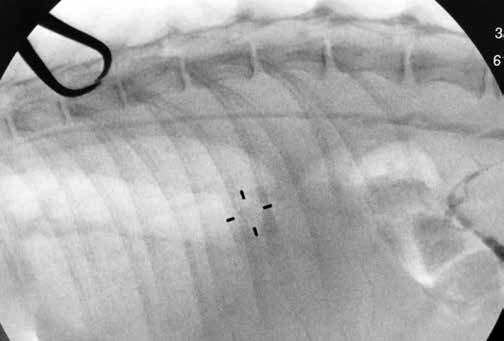
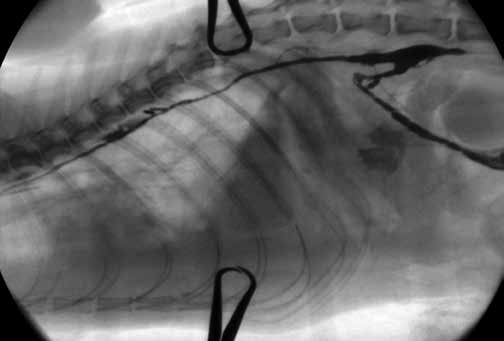
Рис. 7. Пример лимфангиографии. Окрашен грудной Рис. 8. Пример лимфангиографии. Окрашен грудной лимфатический проток.
лимфатический проток Состояние после операции.
Контрастное исследование помогает определить наиболее оптимальный межреберный промежуток для выполнения лигирования грудного лимфатического протока. Традиционным местом латеральной торакотомии для ЛГЛП являются 9-10 межреберья, однако важным фактором является зона крепления диафрагмы и возможность выполнения лигирования максимально близко к ней. Торакотомия выполняется слева в верхней трети, в выбранном по результатам мезентериальной лимфангиографии межреберном промежутке (рис. 9,10).
рис.9 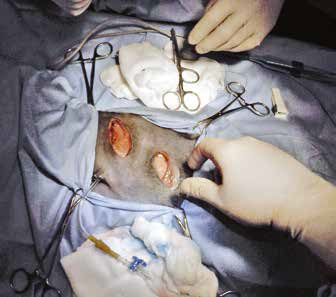 рис.10
рис.10 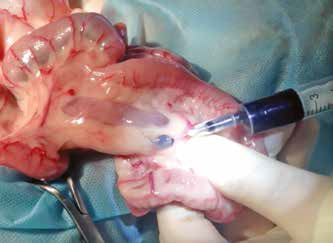 рис. 11
рис. 11 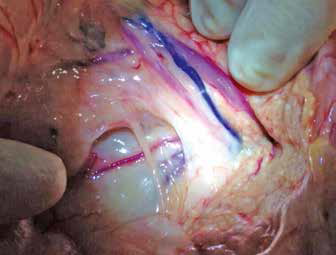
Рис. 9. Вид операционной раны. Рис. 10. Введение красителя Рис. 11. Окрашивание лимфатического сосуда после введения
и латеральная торакотомия
Рассечение тканей для торакотомного отверстия выполняется в привычной хирургу манере. Для ретракции межреберного промежутка можно использовать ранорасширитель Weitlaner или педиатрический реберный дистрактор Finochetto. После формирования доступа и визуализации аорты (аорта является маркером зоны диссекции ГЛП) вновь выполняется пункция мезентериального лимфатического узла в брюшной полости и вводится краситель для интраоперационной навигации и определения ГЛП [8] (рис. 11-13).
рис.12 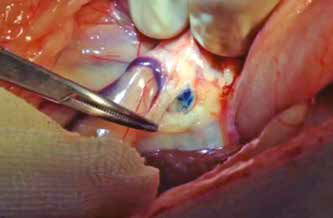 рис.13
рис.13 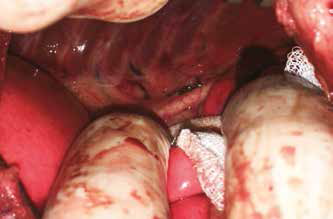
Рис. 12. Окрашивание цистерны хили после введения красителя; Рис. 13. Окрашивание грудного лимфатического протока выше
аорты (кадаверный материал)
После визуализации грудного лимфатического протока выполняется диссекция дорсальной поверхности аорты и отделение от нее ГЛП. В нашей практике, после успешной диссекции, мы выполняем клипирование ГЛП хирургическими клипсами. Техника клипирования более эргономична для данной области нежели традиционное лигирование, но исторически сложилось, что данная процедура каким бы методом она не проводилась, называется именно лигированием грудного лимфатического протока. Далее выполняется контрольное введение индигокармина в мезентериальный лимфатический узел с целью интраоперационного контроля проходимости грудного лимфатического протока после установки клипс. Далее проводится контрастная лимфангиография, целью которой является определение персистенции мелких браншей ГЛП и проходимости лимфы по ним в обход зоны операции (т.е., ввиду повышения давления в системе цистерны хили и абдоминальной части грудного лимфатического протока могут начать персистировать мелкие коллатерали лимфатической системы в плевральной полости) (рис. 14).
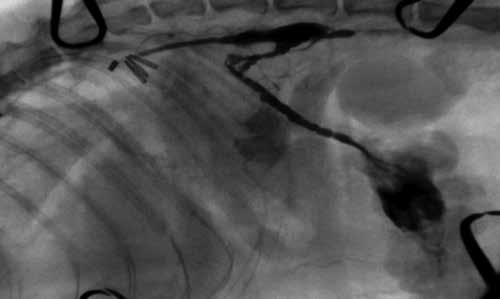
Рис. 14. Лимфангиография после успешного клипирования грудного
лимфатического протока. Отмечается отсутствие тока
контрастного агента по ГЛП
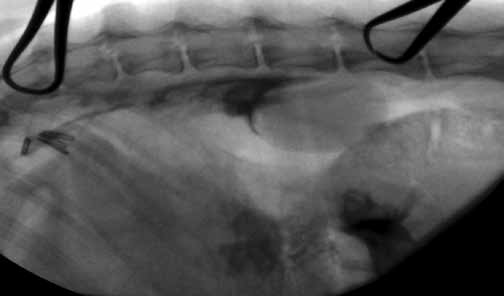
Рис. 15 Инфильтрация ретроперитонеального
пространства контрастным агентом после абляции
цистерны хили
Абляцию цистерны хили в один этап с лигированием ГЛП мы выполняем только в случае отличной визуализации цитерны интраоперационно через парокостальный лапаротомический доступ, так как нередко бывают ситуации плохой визуализации и необходимости дополнительного доступа, что может значительно увеличить продолжительность операции и травму (рис. 15). В свою очередь, АЦХ может быть применена как монометод, так и в сочетании с субфренальной перикадэктомией при неэффективности ЛГЛП как монометода. Сочетание техник зачастую обусловлено возможностью их проведения у конкретного пациента в короткий временной промежуток. Ввиду вариабельности анатомии цистерны хили основным фактором в успешной абляции цистерны хили (АЦХ) является ее интраоперационное окрашивание с помощью индигокармина или любого другого стерильного биодоступного красителя.
Традиционным местом визуализации цистерны хили является область медиальнее краниального полюса левой почки и левее аорты. Зачастую цистерну хили достаточно неплохо видно после окрашивания в околопочечном жиру между левой почкой и левым надпочечником, но как уже было сказано, ввиду вариабельности анатомии это не всегда простая задача
После окончания операции выполняется дренирование плевральной полости с целью послеоперационного контроля за аккумуляцией хилеза и воздуха. В среднем дренирование актуально на последующие 2-3 дня, после этого дренаж удаляется. Динамическое наблюдение за результатом операции (снижение продукции и аккумуляции хилеза) мы традиционно продолжаем в течение месяца. При отсутствии эффекта рекомендуется выполнение иных техник (абляция цистерны хили, субфренальная перикардэктомия или установка постоянного дренажа – PleuralPort от Norfolk Vet Products).
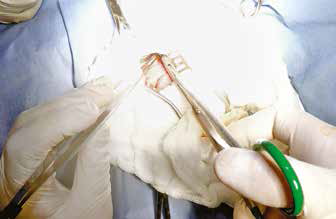
Рис. 16. Клипирование ГЛП с помощью клипсаппликатора и клипс Vitalitec
Выводы
Консервативное лечение хилоторакса у кошек и собак оправдано в качестве первоначального подхода в тех случаях, которые возможны с медицинской или спонтанной точки зрения [6,9].
Хирургический подход будет оправдан, если консервативное лечение не дало результатов, а количество транссудата остается неизменным, без видимых уменьшений.
Публикации журнала Veterinary Surgery за несколько лет показывают эффективность методики лигирования ГЛП совместно с выполненной перикардэктомией [11,12].
Лигирование ГЛП методом «En Bloc», показало хорошие результаты согласно публикации журнала Veterinary Surgery. Оно отличается отсутствием необходимости в дополнительном лапаротомическом доступе, а также в контрастировании ГЛП и лимфангиографии. Соответственно, снижается количество затраченного времени на операцию, но не исключается возможность персистенции мелких браншей ГЛП, что может привести в дальнейшем к возможной дополнительной операции, которая будет служить той же цели, что и предыдущая [10].
В нашей операционной бригаде принято отдавать предпочтение методу, при котором требуется минимальное количество доступов и затраченного времени, с максимально возможной эффективностью. Наша цель – в первую очередь лигировать ГЛП, и сделать ангиографию для исключения проходимости и персистенции мелких браншей ГЛП. В дальнейшем, по возможности, провести АЦХ, если имеется хорошая визуализация. Это не требует дополнительный доступ и не приведет к увеличению времени операции. Меньшее время нахождения пациента в состоянии наркоза лучше сказывается на общем состоянии животного, которое зачастую и без того ослаблено. При отсутствии улучшений после лигирования ГЛП как монометода, возможно выполнение АЦХ с более точной навигацией и совместной перикардэктомией [7].
Примечание: авторы декларируют отсутствие конфликта интересов.
Литература
1. Birchard SJ, Ware WA, Fossum TW, et al: Chylothorax associated with congestive cardiomyopathy in a cat. J Am Vet Med Assoc 1986; 189:1462–1464.
2. Fossum TW, Miller MW, Rogers KS, et al: Chylothorax associated with right-sided heart failure in five cats. JAmVet Med Assoc 1994;204:84–89.
3. Campbell SL, Forrester SD, Johnston SA, et al: Chylothorax associated with constrictive pericarditis in a dog. J Am Vet Med Assoc 1995;206:1561–1564.
4. Meincke JE, Hobbie WV, Barto LR: Traumatic chylothorax with associated diaphragmatic hernias in the cat. J Am Vet Med Assoc 1969;155:15–20.
5. Fossum TW, Miller MW, Rogers KS, et al: Chylothorax associated with right-sided heart failure in five cats. JAmVet Med Assoc 1994;204:84–89.
6. Birchard SJ, McLoughlin MA, Smeak DD: Chylothorax in the dogs and cat: a review. Lymphology 1995;28:64–72.
7. Jonathan F. McAnulty, DVM, PhD. Prospective Comparison of Cisterna Chyli Ablation to Pericardectomy for Treatment of Spontaneously Occurring Idiopathic Chylothorax in the Dog. Veterinary Surgery 40 (2011), 926–934.
8. Benjamin J. Bayer, DVM, Diplomate ACVS, Mauricio Dujowich, DVM, Diplomate ACVS, Alexander I. Krebs, DVM, Timothy G. Leeds, MD, FACOG, Gregory M. Anderson, DVM, Diplomate ACVS, and David F. Merkley, DVM, Diplomate ACVS. Injection of the Diaphragmatic Crus With Methylene Blue for Coloration of the Canine Thoracic Duct. Veterinary Surgery 43 (2014), 829–833.
9. Carlos C. Hodges, DVM, MS. Theresa W. Fossum, DVM, MS, PhD, Diplomate ACVS, and Winston Evering, DVM, PhD. Evaluation of Thoracic Duct Healing After Experimental Laceration and Transection. Veterinary Surgery, 22, 6,431 -435, 1993.
10. NICHOLAS J. MACDONALD, BVetMed, MVM, PETER-JOHN M. NOBLE, BVM&S, PhD, and RACHEL D. BURROW, BVetMed, Diplomate ECVS. Efficacy of En Bloc Ligation of the Thoracic Duct: Descriptive Study in 14 Dogs. Veterinary Surgery 37:696–701, 2008.
11. Theresa W. Fossum, Michelle M. Mertens, Matthew W. Miller, John T. Peacock, Ashley Saunders, Sonya Gordon, Galen Pahl, Lori A. Makarski, Anne Bahr, and Phil H. Hobson. Thoracic Duct Ligation and Pericardectomy for Treatment of Idiopathic Chylothorax. J Vet Intern Med 2004;18:307–310.
12. David A. Allman, DVM, Maryann G. Radlinsky, DVM, MS, Diplomate ACVS, Alan G. Ralph, DVM, and Clarence A. Rawlings, DVM, PhD, Diplomate ACVS. Thoracoscopic Thoracic Duct Ligation and Thoracoscopic Pericardectomy for Treatment of Chylothorax in Dogs. Veterinary Surgery 39:21–27, 2010.

Назад в раздел

















