Этиопатогенез современных инфекций. Часть 2. Резистентность возбудителей к антибиотикам. Госпитальные инфекции. Перспективные средства терапии / Aetiopathogenesis of contemporary infections. Part 2. Antibiotic resistance. Nosocomial infections. Prospectiv
Еще фото
Автор (ы): P.С. Овчинников, к.б.н. / R. Ovchinnikov, Phd, Senior researcher
Организация(и): Федеральный научно-исследовательский центр эпидемиологии и микробиологии имени Н.Ф. Гамалеи («ФНИЦЭМ им. Н.Ф. Гамалеи»), Москва / Federal Research Centre for Epidemiology and Microbiology n.a. N.F. Gamaleya, Moscow
Журнал: №3 - 2015
УДК 619:616-022
Ключевые слова: инфекционные болезни животных, возбудители, резистентность к антибиотикам, госпитальные инфекции, лабораторная диагностика, энзибиотики, эпидемиологическое благополучие
Key words: animal infectious diseases, pathogens, antibiotic resistance, nosocomial infections, laboratory diagnosis, enzybiotics, public health
Аннотоция
Вторая часть обзора посвящена проблемам антибиотикорезистентности, госпитальным инфекциям, лабораторной диагностике бактериальных и грибковых инфекций, а также новым перспективным средствам терапии. Освещены различные типы лекарственной резистентности микроорганизмов, в т.ч. мультирезистентность. Появление агрессивных, высококонтагиозных и резистентных штаммов привело к распространению в ветеринарии внутрибольничных инфекций. На этом фоне требуют пересмотра традиционные подходы к диагностике и терапии инфекционных заболеваний. Особую значимость приобретает лабораторная диагностика и корректное определение антибиотикочувствительности. Перспективным средством борьбы с инфекциями могут стать энзибиотики – новый тип противомикробных препаратов. Инфекционные болезни животных необходимо рассматривать в контексте эпидемиологического благополучия человека.
Summary
The second part of the survey is devoted to problems of antibiotic resistance, nosocomial infections, laboratory diagnosis of bacterial and fungal infections, as well as promising new therapies. Different types of antibiotic resistance (including multiresistance) are reviewed. The emergence of aggressive, highly contagious and resistant strains led to the spread of nosocomial infections in veterinary practice. Against this background, a revision of traditional approaches to diagnosis and treatment of infectious diseases is required. The laboratory diagnosis and the correct definition of antibiotic susceptibility are particularly significant. Promising tools to control infections are enzybiotics – a new type of antimicrobial agents. Infectious diseases of animals should be considered in the context of public health.
В настоящее время практикующие врачи все чаще сталкиваются с инфекционными заболеваниями, с трудом поддающимися традиционным средствам и схемам терапии. Это связано с распространением в этиологической структуре штаммов возбудителей, устойчивых к действию противобактериальных лекарственных средств.
Резистентность к антибиотикам обусловлена не только образованием биопленок (см. первую часть статьи), но и другими механизмами, имеющими генетическую природу. Одним из важнейших механизмов является образование микробных ферментов, способных непосредственно разрушать антибиотики. Наибольшую клиническую значимость сегодня представляют следующие типы лекарственной резистентности:
• у грамм-отрицательных бактерий – бета-лактамазы расширенного спектра (БЛРС) и карбапенемазы (KP);
• у стафилококков – метициллин-резистентность (MRS), которая является индикатором устойчивости ко всем бета-лактамным антибиотикам. Также начинают распространяться ванкомицин-резистентные штаммы стафилококков (VRS);
• у энтерококков также наблюдается резистентность к гликопептидному антибиотику ванкомицину (VRE).
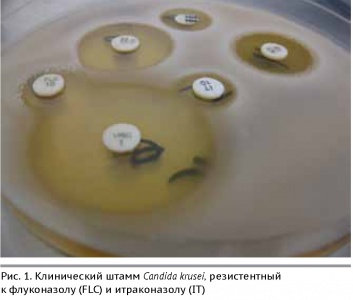
Патогенные грибы также проявляют резистентность к противогрибковым препаратам. На Рис. 1 представлен штамм дрожжевого гриба Candida krusei, резистентный к флуконазолу и итраконазолу – наиболее распространенным в практике противогрибковым препаратам.
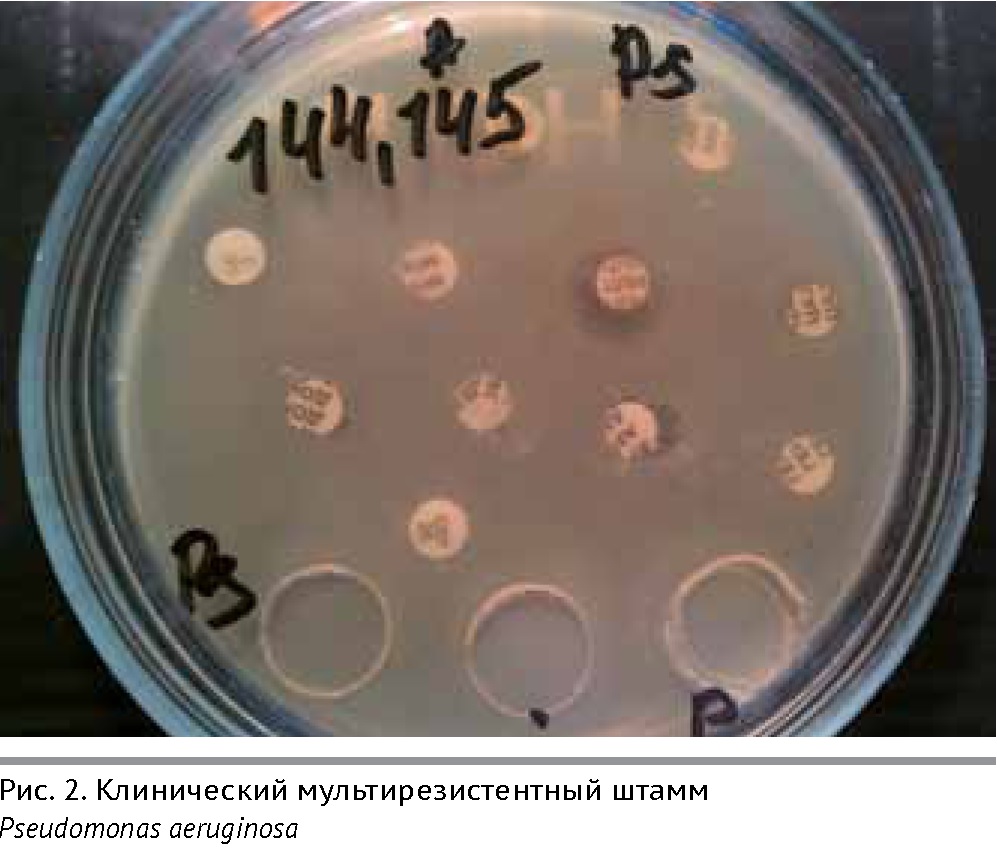
Кроме того, в последние годы растет число мультирезистентных штаммов микроорганизмов, которые проявляют резистентность одновременно к нескольким антибиотикам разных классов (H. Nikaido, 2009). Такой высокий уровень устойчивости может образовываться двумя путями. В первом случае в бактериальной клетке аккумулируется множество генов, каждый из которых кодирует резистентность к какому-либо одному антибиотику. Во втором случае мультирезистентность обусловлена повышенной экспрессией генов, кодирующих механизм эффлюкса (активного выброса из клетки чужеродных веществ, в т.ч. антибиотиков). Один из мультирезистентных штаммов Pseudomonas aeruginosa представлен на Рис. 2 – он проявил устойчивость к антибиотикам следующих групп: пенициллины (в т. ч. «защищенные»), цефалоспорины III и IV поколений, карбапенемы, фторхинолоны, аминогликозиды, тетрациклины, котримоксазол.
В настоящее время мультирезистентные возбудители приобрели настолько серьезное значение, что им присвоен статус «глобальной эмерджентной болезни» (global emergent disease). Животные могут являться источниками мультирезистентных штаммов, опасных для человека, что представляет серьезную проблему для общественного здравоохранения (I. Roca et al., 2015).
Возникновению антибиотикорезистентности способствует неграмотное и зачастую неоправданное терапевтическое использование антибиотиков, профилактическое использование антибиотиков, а также использование антибиотиков в качестве стимуляторов роста (у продуктивных животных). Известно, что при неоправданном применении антибиотиков широкого спектра действия нарушается баланс в нормальной микробиоте животного – чувствительные микроорганизмы уничтожаются, а более устойчивые выживают и размножаются. В результате этого развивается резистентность не только у бактерий-возбудителей, но и у бактерий, составляющих эндогенную комменсальную микробиоту организма животных. Такие бактерии-комменсалы способны самостоятельно вызывать оппортунистические инфекции, а кроме того являются своеобразным резервуаром генов резистентности для болезнетворных бактерий (A. van den Bogaard et al., 1999).
Резистентные штаммы бактерий (таких как Escherichia coli, Salmonella spp., Campylobacter spp., Staphylococcus spp., Enterococcus spp. и др.) могут передаваться от животных к человеку как при непосредственном контакте, так и через пищевую цепочку. Более того, бактерии от животных могут передавать свои гены резистентности возбудителям болезней человека. Так, после внедрения в практику ветеринарного антибиотика апрамицина гены резистентности к нему были обнаружены не только у бактерий от животных, но также и у бактерий-представителей комменсальной микрофлоры человека, у зооантропонозных возбудителей (Salmonella spp.), а также у строго антропофильных патогенов, таких как Shigella spp. (A. van den Bogaard et al., 2000).
Изложенные выше особенности современных возбудителей во многом привели к распространению внутрибольничных инфекций (ВБИ), которые уже в течение многих лет являются острейшей проблемой гуманной медицины. Однако в последние годы наблюдается тревожная тенденция распространения ВБИ и в ветеринарной практике, что косвенно связанно с прогрессом ветеринарной медицины – массовым появлением стационаров, отделений реанимации и интенсивной терапии, проведением высокотехнологичных операций, внедрением современных инвазивных методов диагностики и терапии. Как и в гуманной медицине, возбудители внутрибольничных инфекций животных характеризуются широким спектром устойчивости к антибиотикам (Johnson J., 2002).
ВБИ (известные также как госпитальные, нозокомиальные инфекции) связаны с пребыванием животного в лечебном ветеринарном учреждении. Это может быть как длительное пребывание в стационаре, так и кратковременный визит. Соответственно, заражение животного происходит теми штаммами возбудителей, которые циркулируют в данной ветеринарной клинике. Источником заражения могут служить все объекты больничной среды, оборудование, инструменты, медикаменты, а также другие животные-пациенты. Однако наиболее значимым фактором заражения является ветеринарный персонал.
Инфекции могут быть локализованы в любом месте, но наиболее часто встречаются ВБИ мочевыделительной системы, кровеносной системы, пневмонии, бактериальные диареи, хирургические инфекции.
Штаммы микроорганизмов, циркулирующие во внутрибольничной среде («госпитальные штаммы»), имеют ряд отличительных черт. Прежде всего, это очень вирулентные штаммы, обладающие широким набором факторов агрессивности. Кроме того, они высоко контагиозны и, что особенно важно, высокоустойчивы к действию антибиотиков и дезинфектантов. Нередки случаи, когда резервуарами госпитальных штаммов являются даже дезинфицирующие растворы, применяющиеся в ветучреждении. Именно во внутрибольничной среде происходит селекция и накопление агрессивных мультирезистентных штаммов возбудителей, вызывающих трудно излечимы е инфекционные заболевания. Известно, что в гуманной медицине на госпитальные штаммы приходится самый высокий уровень заболеваемости, рецидивов и смертности (M. Mohammed et al., 2014).
Внутрибольничные инфекции гораздо более устойчивы к антибиотикотерапии, т. к. вызываются мультирезистентными штаммами.
Терапия таких инфекций обходится существенно дороже, т.к. требует применения новейших дорогостоящих препаратов. Для ветеринарной медицины это играет особо важную роль, т.к. нередко владельцы животных ограничены в средствах и не могут оплатить длительное пребывание животного в стационаре и лечение дорогостоящими антибиотиками, в результате чего животных подвергают эвтаназии (A. Steele, 2009).
Наиболее часто возбудителями ВБИ являются такие микроорганизмы, как Enterococcus spp., E. coli, Staphylococcus spp., Enterobacter spp., Klebsiella spp., Acinetobacter spp., Pseudomonas spp. Из них Enterococcus spp., E. coli и Staphylococcus spp. способны легко приобретать детерминанты резистентности: резистентность к ванкомицину у энтерококков, мультирезистентность у E. coli, метициллин-резистентность у стафилококков. В течение многих лет эти микроорганизмы являются проблемой для гуманной медицины, а в настоящее время приобретают всё большее значение и в ветеринарии.
В гуманной медицине к настоящему времени накоплен большой опыт по профилактике и борьбе с внутрибольничными инфекциями, и ветеринарным специалистам необходимо взять этот опыт на вооружение. Тем более, что в большинстве случаев для профилактики ВБИ достаточно таких элементарных мер, как мытье рук между пациентами, дезинфекционная обработка инструментов, инвентаря и рабочих помещений. Как уже упоминалось, владельцы нередко прибегают к эвтаназии животных в случае заражения трудноизлечимой ВБИ. Т.к. в большинстве случаев эти инфекции можно было предупредить, ответственность за них ложится на плечи ветеринарного персонала, который должен знать и строго соблюдать профилактические меры.
Сложившаяся ситуация требует пересмотреть традиционные подходы к диагностике и терапии инфекционных заболеваний. Адекватная достоверная диагностика невозможна без проведения компетентного микробиологического исследования (Рис. 3). Оно позволяет судить обо всём микробном пейзаже в очаге поражения, выделить и идентифицировать всех членов микробной ассоциации, оценить численность популяции микроорганизмов. Количественная оценка позволяет с известной точностью отличить инфекцию от колонизации и контаминации.
Первостепенное значение приобретает точность выбора противомикробного средства (антибиотика), его эффективность против конкретного возбудителя. Имея дело с резистентными госпитальными штаммами, нельзя полностью полагаться на эмпирический подход в терапии.
При этом определение чувствительности возбудителя традиционным диско-диффузионным методом может оказаться недостаточным. Для препаратов с до-зозависимым эффектом возникает необходимость количественного определения МПК (минимальной подавляющей концентрации) (Рис. 4, 5). Это поможет определить эффективную дозу для конкретного возбудителя с учетом локализации инфекции. Для полирезистентных госпитальных штаммов это может быть единственным способом определения эффективной терапии. Также лаборатория должна быть способна к выявлению специфических типов лекарственной резистентности, которые не всегда обнаруживаются рутинными методами.
Терапия инфекций, вызываемых высокоустойчивыми штаммами микроорганизмов, является важнейшей проблемой современной медицины, как гуманной, так и ветеринарной. В ответ на появление таких инфекций, фармакологами были предложены новые модификации антибиотиков, чья формула обеспечивает устойчивость к действию литических микробных ферментов. Например, действие микробных бета-лактамаз способна блокировать клавулановая кислота, которую вводят в состав некоторых бета-лактамных антибиотиков. Такие антибиотики получили название «защищенных», например, амоксициллина клавуланат. Они эффективны против тех штаммов, которые устойчивы к действию обычных, незащищенных форм бета-лактамов.
Также может быть эффективным сочетанное применение двух антибиотиков, обладающих синергидным эффектом. Однако для использования этого подхода необходимо лабораторное определение эффективности действия двух препаратов в отношении конкретного штамма возбудителя – препараты могут проявить как синергидный, так и конкурентный эффекты (M. Поляк, 2014).
Следует учитывать, что имеющиеся на сегодня классы антибиотиков в разной степени подвержены действию микробных литических ферментов. К некоторым из них, например, незащищенным беталак-тамам (пенициллины, цефалоспорины), резистентность встречается гораздо чаще, чем, например, к антибиотикам класса фторхинолонов. Также установлено, что определенные антибиотики могут быть эффективны даже в отношении биопленок. В частности, фторхинолоны третьего поколения эффективны против биопленок, образуемых Pseudomonas aeruginosa (T. Goto et al., 1999). Еще раз следует отметить, что при выборе средства терапии необходимо учитывать результаты лабораторного исследования, в т. ч. антибиотикограммы.
Однако в целом становится всё более очевидным, что имеющихся в арсенале лекарственных средств уже недостаточно для эффективной терапии инфекционных заболеваний, и победоносная эра антибиотиков клонится к своему закату. Количество новых препаратов, выходящих на рынок, в 2000-х годах резко сократилось, и в ветеринарии их нехватка ощущается особенно остро. Что касается открытия новых механизмов действия, то еще с 1987 г. ни одного принципиально нового класса антибиотиков предложено не было.
Каковы же дальнейшие перспективы борьбы с инфекционными заболеваниям? По мнению многих исследователей, прийти на смену антибиотикам могут т. н. энзибиотики – препараты, в корне отличающиеся от антибиотиков по механизму действия. По своей природе они являются ферментами, способными непосредственно лизировать те или иные структуры микробной клетки. Продуцентами этих ферментов являются бактериофаги, а также бактерии и другие микроорганизмы. Колоссальным преимуществом энзибиотиков является то, что они с успехом лизируют микроорганизмы любого типа резистентности, в т. ч. и госпитальные штаммы, и при этом не проявляют таких побочных эффектов на макроорганизм, как многие антибиотики.
К энзибиотикам во всем мире сейчас приковано самое пристальное внимание, и, безусловно, этот новый тип лекарственных средств открывает огромные перспективы в борьбе с инфекционными заболеваниями. Разработкой энзибиотиков сейчас активно занимаются многие научные лаборатории во всем мире, в том числе и в нашей стране. О том, насколько активно ведутся эти исследования, можно судить по онлайн-базе phiBIOTICS (http://www.phibiotics.org), где собрана информация по нескольким десяткам энзибиотиков, применяемым с терапевтической целью.
Отдельные препараты этой группы уже выпущены на рынок некоторых стран. Например, дисперсин – энзибиотик, действующий целенаправленно на биопленки. Он лизирует цементирующее вещество биопленочного матрикса поли-N-ацетил-глюкозамин. Данное вещество образуется в биопленках как грамположительных, так и грамотрицательных организмов, т.е. дисперсин обладает широким противомикробным потенциалом. В настоящее время коммерческий дисперсин для ветеринарного применения доступен в Канаде как средство против отитов и инфекций, ассоциированных с атопическим дерматитом.
Еще одним перспективным энзибиотиком является лизостафин, действие которого специфически направлено против Staphylococcus aureus, важнейшего возбудителя инфекций, в т. ч. и внутрибольничных. Литическое действие лизостафина направлено против пептидогликана – структурного вещества клеточной стенки стафилококков (J. Kumar, 2008). Лизостафин эффективен в отношении высокорезистентных штаммов, а также в отношении стафилококковых биопленок. Примечательно, что он может применяться не только наружно, но и парентерально, то есть может использоваться для терапии стафилококковых инфекций глубокой локализации. В настоящее время лизостафин для клинического применения пока выпускается только в Китае. В России разработкой лекарственных средств на основе дисперсина и лизостафина активно занимается «ФНИЦЭМ им. Н.Ф. Гамалеи».
В завершении хотелось бы отметить, что инфекции животных и человека находятся в тесной взаимосвязи – между ними циркулируют одни и те же виды возбудителей и даже те же штаммы. Современные вызовы, которые бросают инфекционные заболевания, касаются и гуманной, и ветеринарной медицины, и для успешного их преодоления необходимы консолидированные усилия специалистов смежных дисциплин, совместные научно-исследовательские и прикладные проекты с участием практикующих специалистов. Не случайно всё большее признание получает концепция «One Health» - «Одно здоровье», которая декларирует комплексный подход к проблеме инфекционных заболеваний. Мы еще раз убеждаемся в том, что ветеринария обеспечивает здоровье и благополучие не только животных, но и человека.
Автор будет рад получить отзывы и ответить на вопросы читателей на странице Facebook по адресу www.facebook.com/vetinfections или по почте: rsovchinnikov@mail.ru
Литература
1. Поляк М. Роль микробиологической службы в обеспечении эффективной антибиотикотерапии на современном этапе. Медицинский алфавит – Современная лаборатория, 2014, 15(231), стр. 51-55.
2. Anthony E. van den Bogaard, Stobberingh E. Antibiotic usage in animals: impact on bacterial resistance and public health. Drugs. 1999 Oct;58(4):589-607.
3. Anthony E. van den Bogaard, Stobberingh E. Epidemiology of resistance to antibiotics. Links between animals and humans. Int J Antimicrob Agents. 2000 May;14(4):327-35.
4. Goto T., Nakame Y., Nishida M., Ohi Y. In vitro bactericidal activities of beta-lactamases, amikacin and fluoroquinolones against Pseudomonas aeruginosa biofilm in artificial urine. Urology. 1999 May;53(5):1058-62.
5. Johnson J. Nosocomial infections. Vet Clin North Am Small Anim Pract. 2002 Sep; 32(5):1101-26.
6. Kumar J. Lysostaphin: an antistaphylococcal agent. Appl Microbiol Biotechnol. 2008 Sep; 80(4):555-61. doi: 10.1007/s00253-008-1579-y.
7. Mohammed M., Mohammed A., Mirza M., Ghori A. Nosocomial infections: An overview. Int. Res. J. Pharm., 2014, 5(1), pp 7-12; doi:10.7897/2230-8407.050102.
8. Nikaido H. Multidrug resistance in bacteria. Annu Rev Biochem. 2009;78:119-46. doi: 10.1146/annurev.biochem.78.082907.145923.
9. Roca I., Akova M., Baquero F., Carlet J. et al. The global threat of antimicrobial resistance: science for intervention. New Microbes New Infect. 2015 Apr 16;6:22-9. doi:10.1016/j.nmni.2015.02.007. eCollection 2015.
10. Steele A. Nosocomial infections: what's the big deal? AAHA Phoenix 2009 proceedings. American Animal Hospital Association, Phoenix, Arizona, March 26-29, 2009, PP 737-741.



Назад в раздел


















