Препараты для анестезии - что важно знать врачу
Еще фото
Автор (ы): А.Н.Мальцева, врач анестезиолог-реаниматолог, руководитель отделения анестезии, реанимации и интенсивной терапии ветеринарной клиники «Белый клык», Москва
Журнал: №1 -2017
В прошлых статьях мы обсуждали предоперационную подготовку и премедикацию, теперь перейдем к рассмотрению препаратов, которые мы можем использовать для обеспечения анестезиологического пособия.
Прежде чем применять тот или иной препарат для анестезии, врач должен быть уверен, что он знает ответы на следующие вопросы.
- • На какие рецепторы препарат воздействует, какого эффекта на организм можно ожидать?
- • Обладает ли препарат анальгетическим эффектом?
- • Обладает ли препарат снотворным, миорелаксирующим эффектом?
- • Можно ли сочетать его с другими препаратами?
- • Каким пациентам категорически нельзя данный препарат?
Выбирая тот или иной препарат для анестезии или их комбинацию, мы должны получать желаемую цель: обеспечить сон нужной глубины, миорелаксацию и, что очень важно, аналгезию.
Давайте рассмотрим основные доступные нам препараты для анестезии с этой точки зрения, чтобы лучше разбираться, чем должен быть обусловлен выбор препарата для наркоза в том или ином случае.
Производные фенотиазина
Наиболее часто применяемый препарат этой группы – ацепромазин. Также у животных применяется прометазин (медицинский препарат Пипольфен, который в основном используется как антигистаминное средство). Точный механизм действия ацепромазина до конца не ясен. Известно, что он блокирует постсинаптические допаминовые рецепторы в центральной нервной системе, также он может угнетать участки активирующей ретикулярной системы, которые участвуют в контроле температуры тела, скорости метаболизма, рвоты, вазомоторного тонуса и сознания. Помимо этого, он также обладает антихолинергическим, антигистаминным, спазмолитическим эффектом и блокирует альфа-адренергические рецепторы [1].
Частые побочные эффекты ацепромазина – воздействие на гемодинамику. После применения может развиваться гипотензия, иногда вместе с брадикардией. Ацепромазин может снижать частоту дыхания, но обычно не вызывает опасного брадипноэ, нарушений оксигенации и вентиляции. Также он может вызывать снижение гематокрита, эффект дозозависимый. Считается, что это происходит из-за усиления секвестрации эритроцитов в селезенке.
Стоит обратить внимание, что в большинстве случаев необходимые дозы ацепромазина значительно ниже, чем те, которые указывают производители. Применение более низких доз часто позволяет достигнуть хорошего седативного эффекта с меньшим риском побочных эффектов.
Эффект ацепромазина наступает не сразу, максимальное действие может наступить только через 30 минут, даже после внутривенного введения. При этом действие препарата длится долго, как правило, несколько часов [1].
Стоит избегать применения ацепромазина или как минимум снижать дозу у пациентов с нестабильной гемодинамикой, с заболеваниями сердца, печени, пожилым животным. Также есть данные, что собаки гигантских пород могут быть более чувствительны к нему. Пациенты с ABCB1-1Δ; мутацией (также называемой MDR мутацией*) более чувствительны к ацепромазину, им также нужно обязательно снижать дозу. Ветеринарная клиническая фармакологическая лаборатория Вашингтона рекомендует снижать дозу на 25% для собак, гетерозиготных по MDR1 мутации, и на 30–50% для гомозиготных. По имеющимся на данный момент исследованиям, не выявлено отрицательного влияния ацепромазина на пациентов с судорогами в анамнезе [2, 3].
Ацепромазин не обладает сам никаким анальгетическим эффектом, хотя считается, что он может усиливать анальгетический эффект опиоидов. В связи с этим как препарат для анестезии он достаточно бесполезен – долгое наступление эффекта, длительное действие (то есть плохая управляемость), отрицательное воздействие на гемодинамику, при этом полное отсутствие анальгетического эффекта и адекватной глубины сна. Однако полностью забывать про этот препарат не стоит. При применении в низких дозах побочные эффекты обычно не выражены. Учитывая его долгий эффект, он подходит для седации пациентов во время нахождения в клинике (например, чтобы собака не лаяла в клетке в ожидании операции или процедуры) или если пробуждение после анестезии сопровождается избыточным возбуждением.
Дозы ацепромазина варьируют очень широко (0,005–2,2 мг/кг), однако в большинстве случаев для седации достаточно низких доз (0,005–0,01 мг/кг) – это совсем небольшое количество препарата, часто врачу даже сложно поверить, что оно может оказать какой-либо эффект. Однако оно часто позволяет седировать пациента без побочных эффектов.
Раствор ацепромазина для инъекций можно делать внутримышечно или вводить перорально. Допускается также внутривенное введение, однако оно должно быть очень медленным, риск падения артериального давления при таком способе введения может быть выше.
Антидота к ацепромазину не существует. При развитии гипотензии ее корректируют внутривенными болюсами жидкости, при неэффективности – инфузией вазопрессоров (допамин или норадреналин), брадикардию купируют атропином.
Таким образом, можно сказать, что ацепромазин в анестезиологическом пособии может быть полезен как препарат для седации на неболезненные манипуляции, где допустима поверхностная седация (например, УЗИ), для нахождения в клетке, уменьшения ажитации при выходе из наркоза. Если применяются опиоиды, то ацепромазин можно использовать в дополнение к ним, так как он может профилактировать тошноту и, возможно, потенцировать анальгетический эффект.
Бензодиазепины
Основные препараты этой группы, используемые в ветеринарной медицине, – мидазолам и диазепам. К сожалению, многим врачам в России они недоступны. Бензодиазепины взаимодействуют со специфическими бензодиазепиновыми рецепторами, расположенными в лимбической системе мозга, таламусе, гипоталамусе, восходящей активирующей ретикулярной формации ствола мозга и вставочных нейронах боковых рогов спинного мозга. Бензодиазепины усиливают чувствительность ГАМК-рецепторов к медиатору (ГАМК), в результате происходит усиление тормозного влияния ГАМК и угнетение межнейронной передачи в соответствующих отделах ЦНС. Соответственно, основная цель применения препаратов этой группы – седация, миорелаксация и анксиолизис. Также они обладают противосудорожным эффектом и могут применяться для купирования эпистатуса. Бензодиазепины практически не оказывают влияния на гемодинамику (хотя в редких случаях могут вызывать гипотензию), но могут угнетать дыхание, вызывать повреждение печени (особенно, у кошек) и парадоксальную ажитацию и возбуждение.
В анестезиологии чаще используется мидазолам (если есть возможность его применять), так как у него менее выражены побочные эффекты. Основная цель применения – седация в премедикации. В монорежиме уровень седации для каждого конкретного пациента предсказать невозможно. Поэтому обычно бензодиазепины используют в комбинации с другими препаратами (ацепромазином, дексмедетомидином). Их можно применять совместно с опиоидами для обеспечения нейролептоаналгезии (комбинация нейролептика бензодиазепина для седации и уменьшения тревоги и опиоида для обезболивания). Также бензодиазепин – это обычный «друг» диссоциативного анестетика, поскольку в монорежиме они вызывают галлюцинации и возбуждение, которое хорошо купируется бензодиазепинами. Именно поэтому обычно используется комбинация кетамин+мидазолам, кетамин+диазепам или уже привычная нам комбинация тилетамин+золазепам.
Бензодиазепины не обладают анальгетическим эффектом, поэтому в монорежиме не могут обеспечить нужную глубину наркоза и аналгезию. Их применяют вместе с опиоидами, альфа-2-агонистами, диссоциативными анестетиками.
При развитии побочных эффектов или передозировке можно использовать антагонист бензодиазепинов – флумазенил. К сожалению, он также недоступен большинству ветеринарных врачей.
Дозы для премедикации
Диазепам 1 мг/кг в/венно или ректально (обратите внимание – всасывание препарата при внутримышечном введении непредсказуемо, поэтому не рекомендуется). Мидазолам 0,1–0,3 мг/кг в/в, в/в или п/к.
Опиоиды
Опиоиды являются группой препаратов с наиболее выраженным анальгетическим эффектом. Рецепторы к опиоидным анальгетикам обнаруживаются в лимбической системе, спинном мозге, таламусе, гипоталамусе, полосатом теле, а также в желудочно-кишечном, мочевыделительном трактах и гладкой мускулатуре других органов.
Опиоидные рецепторы разделяются на несколько подгрупп, из которых наиболее важные у наших пациентов, отвечающие за аналгезию, – это мю- и каппа-рецепторы. Активация мю-опиоидных рецепторов ингибирует пресинаптическое выделение (особенно в дорсальных рогах спинного мозга) и постсинаптический ответ возбуждающих нейротрансмиттеров. С помощью ряд механизмов это приводит к гиперполяризации нейрона, снижению выделения субстанции Р. Это, в свою очередь, нарушает трансмиссию (передачу) болевого стимула.
Анальгетические и побочные эффекты опиоидов зависят от того, на какие рецепторы действует препарат. Например, морфин является чистым мю-агонистом. Он имеет выраженный анальгетический эффект, но также угнетает дыхание и может вызывать выделение гистамина и тошноту. У опиоидов других подгрупп эти эффекты менее выражены.
У кошек из-за нарушенного метаболизма морфин обладает гораздо более слабым анальгетическим эффектом и не является идеальным анальгетиком [4]. Также к чистым мю-агонистам относятся оксиморфин, метадон, фентанил и мепередин. Наиболее часто в зарубежной анестезиологической практике используется фентанил. Его анальгетическая активность почти в 100 раз выше, чем у морфина. Он обладает ультракоротким действием, поэтому его используют только в виде инфузии с постоянной скоростью или в виде пластырей.
К этой же группе относится трамадол. Он считается слабым анальгетиком (в 10 раз слабее морфина), однако его все шире используют для лечения хронической нейропатической боли у людей и животных, поскольку он является также агонистом норэпинефрина и серотонина (ингибирующие нейротрансмиттеры) [6, 7]. К сожалению, метаболизм трамадола у собак отличается от такового у людей и кошек [8]. В их организме трамадол может не превращаться в активный метаболит, связывающийся с опиоидными рецепторами. Поэтому, вероятнее всего, его анальгетическая активность у собак связана в основном с серотониновой и норадренергической активностью. Из-за высокого риска побочных эффектов трамадол нельзя применять вместе с другими препаратами, обладающими серотонинергической активностью (например, трициклические антидепрессанты (амитриптилин)).
Буторфанол является агонистом каппа- и антагонистом мю-рецепторов. Хотя он слабый антагонист мю-рецепторов, он будет реверсировать эффект полных мю-агонистов. Влияние на каппа-рецепторы вызывает увеличение образования тормозящих нейротрансмиттеров (например, ГАМК). У собак после буторфанола анальгетический эффект длится очень короткое время (30–40 минут), хотя седативный эффект длится намного дольше. Поэтому обычно его рекомендуют скорее как препарат для седации, нежели чем для аналгезии.
У полных мю-агонистов есть антидот – налоксон (антагонист опиоидных мю-рецепторов). Его используют для лечения передозировки мю-агонистами или при развитии побочных эффектов.
Побочные эффекты на опиоиды у животных отличаются от таковых у людей. Больших статистических данных нет, при опросе практикующих ветеринарных врачей в США получился следующий список: дисфория (41%), тошнота, констипация (15%), илеус (15%), неэффективная аналгезия (7%), депрессия дыхания (3%), 20% врачей вообще не наблюдали никогда у своих пациентов побочных эффектов от опиоидов. Поскольку один из ведущих побочных эффектов – это воздействие на желудочно-кишечный тракт, большую надежду внушает появление препарата, который блокирует воздействие на опиоидные рецепторы изолированно в кишечнике, при этом мы получаем отсутствие влияния опиоидов на ЖКТ без уменьшения анальгетического эффекта (Peripherally Acting Mu Opioid Receptor Antagonists (PAMOR)).
К сожалению, сложности с организацией хранения и приобретения опиоидов не дают большинству из нас возможности наблюдать их анальгетические и побочные эффекты. Разумеется, если появляется возможность их использования, опиоиды обязательно нужны – их используют в премедикации, при необходимости (если опиоид короткого действия) вводят непосредственно во время хирургического вмешательства.
Доза трамадола для собак – 1–2 мг/кг 1 р/8–12 ч, для кошек – 1–3 мг/кг 1 р/8–12 ч. Также предлагается использовать его в виде инфузии с постоянной скоростью 0,1–0,3 мг/кг/ч (Veterinary Anesthesia & Analgesia Support Group).
Несмотря на то что трамадол является слабым анальгетиком, его наличие лучше, чем полное отсутствие опиоидов, поэтому при возможности можно и нужно его использовать.
Альфа-2-агонисты
Препараты этой группы начали использовать в ветеринарной медицине еще в 60-х годах XX века. Однако долгое время их применение было ограничено из-за побочных эффектов. С появлением новых препаратов и благодаря оптимальному подбору доз они стали широко использоваться в человеческой и ветеринарной медицине.
Альфа-2-адренергические рецепторы (адренорецепторы) широко распространены в организме. Их можно найти в пре-, пост- и экстрасинаптических пространствах, они являются важной составляющей частью симпатической нервной системы. В настоящее время открыто несколько подтипов альфа-2-адренорецепторов (А, В, С).
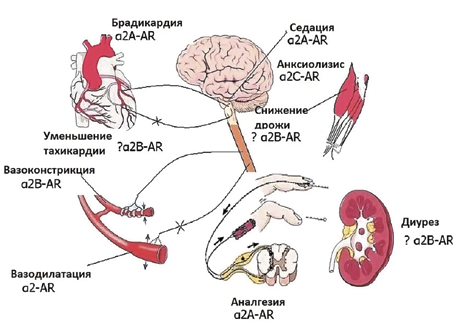
Схема воздействия альфа-2-агонистов на организм. AR – адренорецепторы (α2 А, α2 В, α2 С). Вазодилатация наблюдается за счет блокирования
симпатической нервной системы, бывает при использовании очень высоких доз, при рутинном применении обычно не выражена
Альфа-2-агонисты воздействуют на норадренергические рецепторы в головном мозге (в частности, на голубое пятно), ингибируют образование норадреналина, стимулируют образование ГАМК и галанина, снижают образование гистамина – это все вызывает снотворный эффект.
При этом процесс очень похож на нормальный физиологический сон [10]. За счет блокады рецепторов на уровне рогов спинного мозга достигается антиноцицептивный эффект альфа-2-агонистов (см. рис. 1). Также они уменьшают мышечную дрожь.
К сожалению, все альфа-2-агонисты воздействуют не только на альфа-2-, но и на альфа-1-рецепторы. Стимуляция альфа-1-рецепторов усиливает побочные эффекты – вазоконстрикцию, нарушения ритма и уменьшает антиноцицептивный эффект [11]. Учитывая этот фактор, отдают предпочтение более селективным альфа-2-агонистам. Аффинность ксилазина α2/α1 – 160/1 (то есть на каждые 160 активированных альфа-2-рецепторов приходится один альфа-1-рецептор), медетомидин и дексмедетомидин в 10 раз более селективны (их аффинность α2/α1 оценивается как 1620/1) [26]. В связи с этим ксилазин все меньше используется в анестезиологии мелких домашних животных, так как другие препараты этой группы вызывают меньше
побочных эффектов при более эффективных анальгетических возможностях.
Медетомидин – это рацемическая смесь, содержащая 50% дексмедетомидина и 50% левомедетомидина. Необходимым нам седативным и анальгетическим эффектом обладает только дексмедетомидин. При этом левомедетомидин не просто «бесполезный» партнер дексмедетомидина – он может уменьшать его анальгетический и седативный эффект, при этом увеличивать частоту побочных эффектов [13]. По этой причине в гуманитарной медицине и в анестезиологии мелких домашних животных на Западе используется преимущественно дексмедетомидин. В России его применение было ограничено в связи с высокой стоимостью препарата. Благодаря появлению в 2016 году доступного ветеринарного аналога («Дексдомитор»), у нас наконец-то также появилась возможность его использовать.
Побочные эффекты альфа-2-агонистов часто пугают врачей. Однако эти препараты гораздо безопаснее, чем мы привыкли думать. Возможно, опасения связаны с тем, что много лет мы были вынуждены пользоваться менее селективными препаратами. Также побочные эффекты во многом зависят от дозы. Например, в некоторых инструкциях к медетомидину доза препарата, необходимая для глубокой седации, указана как 150 мкг/кг, в то время как стандартные рекомендации фармакологических справочников – не превышать дозу в 20 мкг/кг, а в большинстве случаев будет достаточно 10 мкг/кг. Неудивительно, что при применении таких высоких доз врач может столкнуться с фатальными побочными эффектами.
Один из самых частых побочных эффектов при применении альфа-2-агонистов – брадикардия. Эти препараты вызывают периферическую вазоконстрикцию (именно поэтому мы видим бледные слизистые оболочки у пациентов после альфа-2). Вазоконстрикция повышает общее периферическое сосудистое сопротивление и артериальное давление. В ответ происходит рефлекторное снижение частоты сердечных сокращений (ЧСС) для уменьшения сердечного выброса и снижения артериального давления.
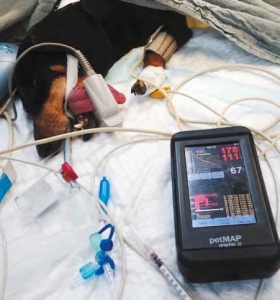
При наличии тонометра обычно очень хорошо видно, что, несмотря на брадикардию (часто ЧСС бывает около 50 раз в минуту), у пациента сохраняется нормальное или даже повышенное артериальное давление. Именно поэтому с такой брадикардией нет необходимости бороться с помощью холиноблокаторов (атропина), так как это только увеличит риск нарушений ритма.
Еще один механизм снижения ЧСС – повышение тонуса вагуса (наиболее часто это вызывает синусовую брадикардию и атриовентрикулярные блокады). Однако опасные для жизни аритмии встречаются крайне редко при применении селективных альфа-2-агонистов [12]. Если брадикардия при применении альфа-2-агонистов не сопровождается артериальной гипертензией (то есть скорее обусловлена усилением тонуса вагуса, а не периферической вазоконстрикцией), то можно рассмотреть введение атропина, но более эффективным и безопасным будет применение антидота ати-
памезола. Про то, что атропин не следует использовать рутинно для премедикации пациентов, мы уже обсуждали в предыдущей статье.
Альфа-2-агонисты, как правило, не оказывают никакого влияния на дыхание, не угнетают дыхательный центр, могут, предположительно, снижать выработку вазопрессина (антидиуретического гормона), что может привести к усилению диуреза. Однако в клинической практике этот эффект, как правило, не выражен (обычно не наблюдается значимого усиления диуреза). При применении ксилазина также бывает рвота, селективные агонисты
рвоту вызывают редко. Альфа-2-агонисты могут снижать выработку инсулина (как и другие препараты, например изофлюран). Однако в большинстве случаев это не играет важного значения, так как не приводит к клинически значимой гипергликемии.
Помимо применения для премедикации, селективные альфа-2-агонисты эффективно используются в виде инфузии с постоянной скоростью во время хирургического вмешательства. Они потенцируют анальгетический эффект других препаратов, снижают потребность в ингаляционных анестетиках и улучшают контроль боли [13–19]. Также их можно использовать для послеоперационной аналгезии в виде инфузии с постоянной скоростью.
В таком режиме они обычно не вызывают значимой седации, при этом могут эффективно обезболивать пациентов. В одном из исследований [14] инфузия с постоянной скоростью дексмедетомидина в послеоперационный период была сопоставима по эффективности с инфузией морфина. Поэтому полезно использовать современные альфа-2-агонисты как в монорежиме, так и в комбинации с другими препаратами (лидокаин системно,
диссоциативные анестетики), как для аналгезии во время хирургического вмешательства, так и в послеоперационный период [14, 19].
Хотя многие годы считалось, что альфа-2-агонисты противопоказаны для использования при кесаревом сечении, т.к. могут снизить кровоток в матке из-за вазоконстрикции, сейчас имеются данные [20,21], что дексмедетомидин можно применять при кесаревом сечении без существенных рисков для матери и плодов. Разумеется, основным способом обезболивания пациентов при кесаревом сечении в настоящее время остается эпидуральная
анестезия, но можно рассмотреть применение дексмедетомидина в тех случаях, когда проведение эпидуральной анестезии невозможно (например, при наличии абсолютных противопоказаний).
При развитии выраженных побочных эффектов или передозировке альфа-2-агонистов используют введение антидота – атипамезола.
Он является антагонистом только альфа-2-адренорецепторов, поэтому побочные эффекты воздействия на альфа-1-рецепторы все равно останутся. С этим может быть связано то, что при передозировке ксилазина побочные эффекты иногда не проходят полностью даже после применения атипамезола – воздействие на альфа-1-рецепторы все равно остается. Эффект атипамезола часто заканчивается быстрее, чем эффект альфа-2-агониста. Особенно это важно помнить, если произошла передозировка препарата. Вероятнее всего, через какое-то время инъекцию атипамезола придется повторить, т.к. его эффект кончится,и побочные эффекты снова появятся. Таких пациентов нужно оставлять под наблюдением в клинике на несколько часов. При повторном введении дозу атипамезола снижают, предполагая, что часть препарата метаболизировалась. Если побочные эффекты случились непосредственно в операционной (например, опасная брадикардия), то можно сделать небольшую дозу атипамезола (1/4 от стандартной), чтобы частично реверсировать эффект альфа-2-агониста, при этом чтобы сохранился хотя бы частично его анальгетический эффект. Надо учитывать, что если мы вводим антидот непосредственно во время хирургического вмешательства, то есть риск пробуждения пациента прямо на
хирургическом столе. Поэтому надо соответственно увеличить дозу других препаратов. При применении дексмедетомидина в виде инфузии с постоянной скоростью нарушений гемодинамики и брадикардии практически никогда не бывает, об этом говорят как результаты исследований [14, 15], так и наш личный опыт.
Из-за возможных побочных эффектов альфа-2-агонисты применяют в меньшей дозе пожилым пациентам, при наличии кардиологических заболеваний, детенышам. Не стоит их применять пациентам с серьезными нарушениями гемодинамики (шок) и избегать применения у нестабильных пациентов (если и использовать, то только в виде инфузии с постоянной скоростью).
Дозы: медетомидин 5–20 мкг/кг в/м, 0,5–2 мкг/кг/ч, дексмедетомидин 0,25–2 мкг/кг/ч.
Диссоциативные анестетики
Являются антагонистами N-метил-D-аспартатных (NMDA) рецепторов. Приводят к диссоциации (разобщению) между таламусом и лимбической системой. Таламус переключает сенсорные импульсы на кору, лимбическая система вовлечена в осознание ощущений. То есть пациент кажется бодрствующим, но отсутствует способность анализировать сенсорные стимулы и реагировать на них.
Самый известный анестетик из этой группы – кетамин. Сейчас большинству врачей доступен его аналог – тилетамин в составе комплексных препаратов (тилетамин + золазепам). Диссоциативные анестетики привлекательны тем, что не имеют угнетающего воздействия на гемодинамику (даже наоборот, могут вызывать тахикардию и по- вышение давления), это делает их препаратами выбора для критических пациентов, когда отрицательное воздействие других препаратов для анестезии на гемодинамику может стать фатальным. Диссоциативные анестетики никогда не применяют в монорежиме, т.к. они могут вызывать психомоторное возбуждение, галлюцинации и дисфорию. Нужно сочетать их с препаратами, обладающими седативным эффектом.
При быстром внутривенном введении или одновременном применении с пропофолом диссоциативы могут вызвать апноэ. Это не значит,
что нельзя применять их вместе. Просто врач, зная такую вероятность, должен быть готов к интубации и искусственной вентиляции легких аппаратом или мешком Амбу. Диссоциативные анестетики обладают анальгетическим эффектом, однако, вопреки распространенному мнению, он достаточно слабый, в том числе плохо контролирует висцеральную боль (от внутренних органов). Это значит, что на одном кетамине или золетиле делать операции нельзя, так как в монорежиме они не обеспечивают адекватный уровень аналгезии (22–25). Необходимо сочетать их с другими препаратами
(опиоиды, альфа-2-агонисты). Исключением являются критические пациенты, у которых есть угрожающие жизни нарушения гемодинамики (например, тяжелый геморрагический шок), тогда можно заходить в операционную на диссоциативе в монорежиме (или в сочетании с бензодиазепином), а после стабилизации (остановки кровотечения) уже ввести дополнительно препараты для аналгезии.
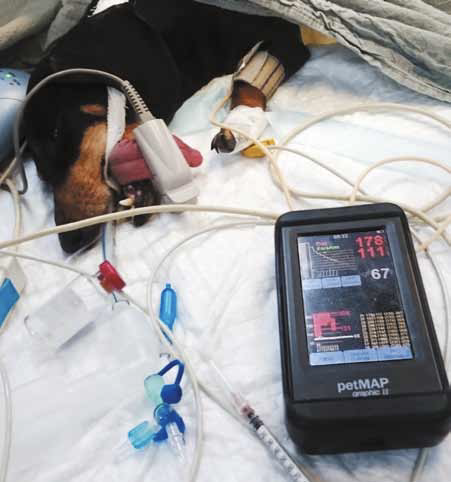
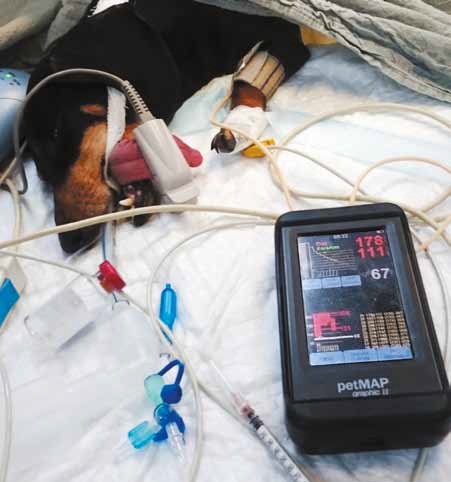
Пациент после премедикации домитором (10 мкг/кг) и золетилом (1 мг/кг),
на изофлюране 0,8 об.% – несмотря на брадикардию, давление даже выше нормы
(хирургическое вмешательство еще не началось)
Тилетамин, по некоторым данным, обладает даже более эффективными анальгетическими свойствами, чем кетамин. Однако недостатком является то,
что тилетамин + золазепам являются готовым комбинированным препаратом, врач не может подобрать индивидуально для своего пациента оптимальную пропорцию диссоциатива и бензодиазепина. Помимо этого, у собак, как правило, быстрее метаболизируется золазепам, поэтому
при пробуждении, когда седативный эффект бензодиазепина уже кончился, а тилетамин еще действует,мы можем наблюдать, как пациент, не реагируя на внешние раздражители, воет в клетке. При этом у кошек, наоборот, дольше метаболизируется золазепам – они могут быть седированы, даже когда эффект тилетамина кончился, и они уже чувствуют боль.
Тилетамин + золазепам используют внутримышечно, болюсно внутривенно (титруя до необходимого эффекта) или в виде инфузии с постоянной скоростью (для поддержания анестезии, для послеоперационной аналгезии). Дозы 1–2 мг/кг в/м, 0,25–4 мг/кг в/в, ИПС 0,5–2 мг/кг/ч.
Пропофол
Механизм действия этого препарата до конца не ясен, считается, что он стимулирует ГАМК-рецепторы. Пропофол является препаратом короткого действия, что делает его эффект очень управляемым, практически сопоставимым с ингаляционной анестезией. Из-за его хорошей управляемости иногда у врача создается впечатление о его абсолютной безопасности. Однако при быстром внутривенном введении пропофол способен вызвать гипо-
тензию, поэтому он не подходит в монорежиме для индукции в анестезию у нестабильных пациентов. Также может вызывать апноэ, особенно при быстром внутривенном введении, поэтому, прежде чем вводить животному пропофол, необходимо на всякий случай приготовить все для интубации.
В зависимости от дозы, пропофол может вызывать как поверхностную седацию, так и глубокую. Однако пропофол не обладает анальгетическим эффектом, поэтому в монорежиме не может быть препаратом для анестезии на хирургические вмешательства, нужно применять совместно с препаратами, обеспечивающими аналгезию.
При индукции или при пробуждении после пропофола можно наблюдать гипертонус мышц. Обычно это не опасно и быстро проходит без дополнительного вмешательства. Дозы пропофола – 4–8 мг/кг для индукции (обычно вводят медленно по 1 мг/кг до нужного эффекта),
8–15 мг/кг/ч ИПС для поддержания анестезии.
Изофлюран
Ингаляционный анестетик, механизм действия которого пока до конца не ясен. Пожалуй, разбору ингаляционных анестетиков стоит
посвятить отдельную статью. Пока лишь обратим внимание, что изофлюран тоже практически не обладает анальгетическим эффектом.
Поэтому, несмотря на то, что многие владельцы просят «газовый наркоз», потому что он им кажется более безопасным, мы с вами должны
понимать, что провести операцию только на ингаляционном анестетике возможно лишь в том случае, если у нас есть эффективная регионарная
анестезия. Если она невозможна – то необходимо добавлять препараты, которые смогут обезболить пациента (например, диссоциативный анестетик и альфа-2-агонист). Также изофлюран не является абсолютно безопасным препаратом и способен вызывать значимую гипотензию, особенно при превышении дозы выше 1 %об.(некачественные испарители могут завышать об.% изофлюрана, это очень опасно, так как может вызывать падение ар-
териального давления).
Системное применение лидокаина
Есть несколько исследований по системному применению лидокаина во время хирургических вмешательств [19], результаты которых показали, что оно приводит к снижению потребности в ингаляционных анестетиках, лучшему контролю боли. Хотя лидокаин системно давно применяется в ветеринарной практике, сейчас интерес к этому методу стал возникать и в человеческой анестезиологии.
В рекомендуемых дозах лидокаин обычно не вызывает никаких побочных эффектов. При передозировке (ошибочном расчете дозы) возможны фатальные аритмии. При применении высоких доз или если метаболизм препарата замедлен (например, у пациентов с печеночной недостаточностью), пациенты могут быть более вялыми, в тяжелых случаях возможны судороги. Антидота у лидокаина нет, но при проявлении его токсических эффектов (как и при системном отравлении другими местными анестетиками) можно применять так называемую «липидную реанимацию» – введение высоких доз растворов липидов. Их эффект объясняется тем, что местные анестетики связываются с жирами и меньше воздействуют на
миокард. В течение одной минуты вводится начальный болюс 20% раствора липидов (интралипид, липофундин и т.д.) из расчета 1,5 мл/ кг массы тела пациента, после чего начинают продленную его инфузию в дозе 0,25 мл/кг/мин, которая должна быть продолжена, по крайней мере, еще 30 минут после восстановления сердечной деятельности. Не забывайте о важности продолжения массажа сердца для обеспечения циркуляции жировой эмульсии. При отсутствии эффекта можно повторить болюсное введение еще один-два раза, а скорость инфузии увеличить до 0,5 мл/кг/ мин.
Лидокаин метаболизируется очень быстро при внутривенном введении, поэтому его имеет смысл использовать только в виде инфузии с постоянной скоростью. При таком режиме терапевтическая концентрация в плазме достигается не сразу, иногда только через несколько часов. Поэтому, если анальгетический эффект нужен быстро, сначала делается болюс внутривенно, потом продолжают инфузию с постоянной скоростью.
Дозы: лидокаин болюс 1–2 мг/кг, далее ИПС 20–30 мкг/кг/мин (к.), 30–50 мкг/кг/мин (соб.).
В следующем номере журнала подведем итог – рассмотрим варианты премедикации и применение препаратов в зависимости от этапов анестезии на примере клинических случаев.
Литература
1. Plumb’s Veterinary Drug Handbook, 8th Edition.
2. McConnell J., et al. Administration of acepromazine maleate to 31 dogs with a history of seizures. J. Vet. Emerg. Crit. Care. 2007; 17(3): 262–7.
3. Tobias K.M., Marioni-Henry K. A retrospective study on the use of acepromazine maleate in dogs with seizures. J. Am. Anim. Hosp. Assoc. 2006; 42 (4): 283-9.
4. Taylor P.M., Robertson S.A. Morphine, pethidine and buprenorphine disposition in the cat. J Vet Pharmacol Therap. 2001; 24: 391–398.
5. Opioids: Which, Why, How, and What’s New? Western Veterinary Conference 2013. Mark E. Epstein, DVM, DABVP (Canine/Feline), DAAPM, CVPP International Veterinary Academy of Pain Management.
6. Gastonia & Charlotte, NC, USA. Wilder-Smith C.H., Hill L., Spargo K., et al. Treatment of severe pain from osteoarthritis with slow-release tramadol or
dihydrocodeine in combination with NSAIDs: a randomised study comparing analgesia, antinociception and gastrointestinal effects. Pain. 2001; 91: 23–31.
7. Katz W.A. Pharmacology and clinical experience with tramadol in osteoarthritis. Drugs. 1996; 52(Suppl 3): 39–47.
8. McMIllan C.J., Livingston A., Clark C.R., et al. Pharmacokinetics of intravenous tramadol in dogs. Can J Vet Res. 2008; 72(4): 325–331.
9. Epstein M.E. Opioids: a practical guide and new developments. North American Veterinary Conference. 2012.
10. Carollo D.S., Nossaman B.D., Ramadhyani U. Dexmedetomidine: a review of clinical applications. Current Opinion in Anesthesiology. 2008.
11. Guo T.Z., Tinklenberg J., Oliker R., Maze M. Central alpha 1-adrenoceptor stimulation functionally antagonizes the hypnotic response to dexmedetomidine,
an alpha 2-adrenoceptor agonist. Anesthesiology. 1991 Aug; 75(2): 252–6.
12. Alpha2-adrenoceptor agonists in small animal practice 1. Why they do what they do Derek Flaherty In Practice, june 5, 2014. Dexmedetomidine Drugs
February. 2000; 59 (2): 263–268.
13. Valtolina C., DVM, MRCVS, Robben J.H., DVM, PhD, Diplomate ECVIM-CA, Uilenreef J., DVM, Diplomate ECVAA, Murrell J.C., BVSc, PhD, Diplomate ECVAA, Aspegrén J., MSc, McKusick B.C. DVM, MS, PhD, Hellebrekers L.J., DVM, PhD, Diplomate ECVAA. Clinical evaluation of the efficacy and safety of a constant rate infusion of dexmedetomidine for postoperative pain management in dogs. Veterinary Anaesthesia and analgesia. July 2009; 36.
14. Uilenreef J.J., DVM, MVRa, Murrell J.C., BVSc, PhD Diplomate ECVAAa, McKusick B.C., DVM, PhDb, Hellebrekers L.J., DVM, PhD, Diplomate ECVAAa. Dexmedetomidine continuous rate infusion during isoflurane anaesthesia in canine surgical patients.
15. Gozalo-Marcillaa M., Steblaja B., Schauvliegea S., Duchateaub L., Gasthuysa F. Comparison of the influence of two different constant-rate infusions (dexmedetomidine versus morphine) on anaesthetic requirements, cardiopulmonary function and recovery quality in isoflurane anaesthetized horses. Research in Veterinary Science. 2013; 95 (3).
16. Lervik A., Haga H.A., Ranheim B., Spadavecchia C. The influence of a continuous rate infusion of dexmedetomidine on the nociceptive withdrawal reflex and temporal summation during isoflurane anaesthesia in dogs. Veterinary Anaesthesia and analgesia. 2012; 39.
17. Sams E.L., DVM, MS, Lerche P. , BVSc, PhD, Bednarski R.M., DVM, MS, Hubbell J.A.E., DVM, MS. Effect of dexmedetomidine, morphine-lidocaine-ketamine, and dexmedetomidine-morphinelidocaine-ketamine constant rate infusions on the minimum alveolar concentration of isoflurane and bispectral index in dogs. American Journal of Veterinary Research. July 2013.
19. Gurney M.A.Pharmacological options for intra-operative and early postoperative analgesia: an update. JSAP. 2012; 53 (7).
20. El-Tahan M.R., Mowafia H.A., Al Sheikhb I.H., Khidra A.M., Al-Juhaimanc R.A. Efficacy of dexmedetomidine in suppressing cardiovascular and hormonal responses to general anaesthesia for caesarean delivery: a dose-response study. International Journal of Obstetric Anesthesia. 2012; 21 (3).
21. Nair A.S., Sriprakash K. Dexmedetomidine in pregnancy: Review of literature and possible use. Journal of Obstetric Anaesthesia and Criticl care. 2013; 3.
22. BSAVA, 2nd Manual of Canine and Feline Anesthesia and Analgesia.
23. AAHA Anesthesia Guidelines for Dogs and Cats. R.Bednarski, MS, DVM, DACVA (Chair), K.Grimm, DVM, MS, PhD, DACVA, DACVCP, R. Harvey, DVM, MS, DACVA, V.M. Lukasik, DVM, DACVA, W. Sean Penn, DVM, DABVP (Canine/Feline), B. Sargent, DVM, DABVP (Canine/Feline), K. Spelts, CVT, VTS, CCRP (Anesthesia). J Am Anim Hosp Assoc. 2011; 47: 377–385.
24. Dugdale A.Veterinary anaesthesia. Willey-Blackwell, 2010.
25. L&J Veterinary Anesthesia and Analgesia, 4th ed. Blackwell, 2007.
26. Pharmacology of detomidine and other alpha-2-adrenoceptor agonists in the brain. Virtanen R Acta Vet Scand Suppl. 1986; 82: 35–46.

Назад в раздел

















