АНЕСТЕЗИОЛОГИЧЕСКОЕ ПОСОБИЕ ПРИ ГЕМОРРАГИЧЕСКОМ ШОКЕ НА ФОНЕ СПОНТАННОГО КРОВОТЕЧЕНИЯ ТИМУСА. КЛИНИЧЕСКИЙ СЛУЧАЙ
Автор (ы): Е. Клепикова, старший врач отделения анестезии, реанимации и интенсивной терапии клиники «Белый Клык», А. Мальцева, руководитель отделения анестезии, реанимации и интенсивной терапии клиники «Белый Клык»
Журнал: №5 - 2018
Абстракт
Кровотечение из тимуса может быть причиной спонтанного гемоторакса у молодых животных. В статье рассматриваются причины, варианты лечения и особенности анестезиологического протокола для таких пациентов на примере клинического случая.
Summary
Thymus bleeding can be the cause of spontaneous hemothorax in young animals. The clinical case of thymus bleeding and anesthesia management are described in this article.
Ключевые слова: гемоторакс, кровотечение из тимуса, геморрагический шок. Key words: hemothorax, thymus bleeding, hemorrhagic shock.
Сокращения: ИПС – инфузия с постоянной скоростью; ОЦК – объем циркулирующей крови; ВСК – время свертывания крови; ВСО – видимые слизистые оболочки; СЗП – свежезамороженная плазма; ЖКТ – желудочно-кишечный тракт; НПВС – нестероидные противовоспалительные средства;ИВЛ – искусственная вентиляция легких.
Кровотечение из тимуса может быть причиной спонтанного гемоторакса у молодых животных. В статье рассматриваются причины, варианты лечения и особенности анестезиологического протокола для таких пациентов на примере клинического случая.
Введение
Тимусовая железа — орган иммунной системы, расположенный в средостении краниальнее сердца. У молодых животных (младше 6 месяцев) он довольно крупного размера, подвергается инволюции и уменьшению размера в процессе взросления и полового созревания. На нормальной рентгенограмме в вентро-дорсальной проекции тимус может визуализироваться левее силуэта сердца и иметь «парусный признак» [2].
У собак описан и встречается необычный синдром спонтанного кровоизлияния в тимус, который может стать причиной смерти. Хотя маловероятно, что имеется специфический патогенез, спонтанное кровоизлияние, судя по всему, ограничивается возрастом инволюции тимуса, так как большинство собак в описанных случаях моложе 1 года. Некоторые исследователи считают, что синдром может быть связан с конкретными гистологическими изменениями, связанными с инволюцией тимуса. Во время инволюции кровеносные сосуды внутри стромы тимуса теряют поддержку тканей, расширяются и становятся тонкостенными. Также в одном из исследований было отмечено, что некоторые пациенты с этим синдромом имели травмы в ближайшем анамнезе (13 из 20 собак имели в анамнезе попадание под машину, резкое поднятие вверх головы хозяином или внезапный рывок поводка). Авторы предположили, что травма, приводящая к внезапному перенапряжению расслабленной шеи, может сопровождаться разрывом небольших сосудов в рыхлых тканях, таких как тимус. При вскрытии наблюдается диффузное кровоизлияние в тимус, краниальный гемомедиастинум и гемоторакс. Лечение спонтанного кровоизлияния в тимус – немедленная заместительная терапия кровью для лечения кровопотери и другая поддерживающая терапия. Хирургическое удаление тимуса, по литературным данным, требуется редко [1].
Клинический случай
В ветеринарную клинику «Белый Клык» поступила собака, некастрированная самка породы короткошерстаня такса, возраст – 5 месяцев, для проведения УЗИ грудной клетки и ЭХОкардиографии из-за подозрения на перикардиодиафрагмальную грыжу.
В анамнезе: утопление 7 дней назад с реанимацией самими владельцами, рвота и диарея последние 4 суток, ухудшение состояния. На рентгене коллегами в другой клинике заподозрена перикардиодиафрагмальная грыжа, пациент направлен в «Белый Клык»
Осмотр при поступлении: вес 6,4 кг, общее состояние критическое.
Ступорозное сознание, выраженная вялость, бледность видимых слизистых оболочек (ВСО), частое поверхностное дыхание 52 ДД/мин, тахикардия 156 уд/мин, тоны сердца аускультативно приглушены, пульс жесткий, гипотермия 36,6 С°, артериальное давление 117/43.
УЗИ брюшной полости: патологий не выявлено
УЗИ грудной клетки: признаки свободной жидкости, коллапса легких, объемное образование в области краниального средостения 7,55*4,86см.
Рентгенография грудной полости в правой латеральной проекции выявила объемный гидроторакс. При торакоцентезе обнаружена кровь (гематокрит плеврального выпота 41%, гематокрит крови 21%).
Цитологическое исследование плеврального выпота: признаков воспаления/септического процесса нет.
Общий клинический анализ крови (отклонения): анемия (эритроциты – 3,5 млн, гематокрит – 21%, гемоглобин – 73г/л), лейкоциты – 22,6 тыс., моноциты – 23%.
Биохимический анализ крови (отклонения): гипопротеинемия 45 г/л (норма – 55-77 г/л), гипоальбуминемия 24 г/л (норма – 25-45 г/л). Время свертывания крови в норме.
Животное помещено в отделение реанимации и интенсивной терапии в состоянии геморрагического шока на фоне гемоторакса.
Дифференциальные диагнозы при госпитализации: травматический гемоторакс; спонтанное кровотечение тимуса; новообразование плевральной полости; гемоторакс на фоне коагулопатии (маловероятно, так как время свертывания крови в норме).
Начато лечение: оксигенотерапия, переливание донорской крови 23 мл/кг, витамин К1 – 5 мг/кг (так как нельзя полностью исключить отравление родентицидами из анамнеза).
Динамика состояния: после гемотрансфузии быстрое восстановление ментального статуса до ясного сознания, стабилизация показателей гемодинамики. Нормотермия, нормотония, ВСО розовые, пульс хорошего наполнения.
Через час после гемотрансфузии ухудшение состояния: угнетение ментального статуса, побледнение ВСО, вялость, тахипное, тахикардия. УЗ-контроль слоя жидкости в грудной полости выявил увеличение количества жидкости в плевральной полости.
Контроль показателей гематокрита в крови и жидкости пациента не позволял быть однозначно уверенными, что кровотечение продолжается.
|
ГЕМАТОКРИТ |
При поступлении |
После гемотрансфузии |
Через час |
|
КРОВЬ |
21 |
31 |
31 |
|
ЖИДКОСТЬ |
41 |
33 |
34 |
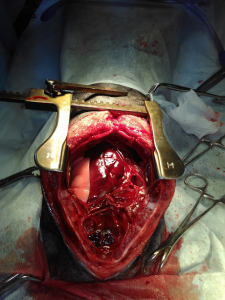
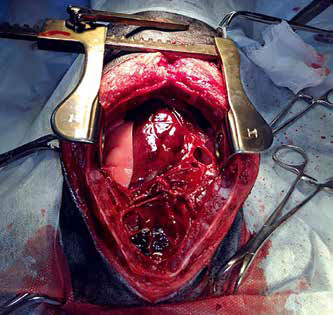
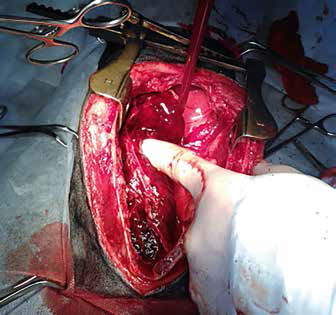
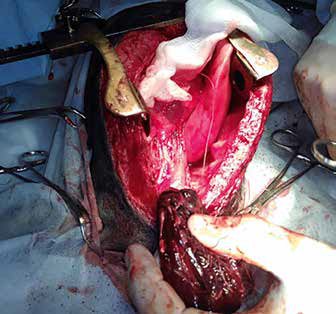
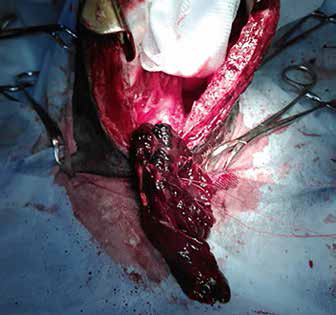
Однако, учитывая увеличение слоя жидкости в грудной полости, быстрое ухудшение состояния с признаками гиповолемии, было принято решение, что кровотечение является продолжающимся, пациент был направлен на диагностическую торакоскопию, на которой обнаружено диффузное кровотечение по всей поверхности тимуса, обширная гематома в каудальном средостении. Проведена стернотомия, удаление тимуса. Материал взят на гистологическое исследование. Установлен торакальный дренаж для контроля скопления жидкости в послеоперационный период, который удален на вторые сутки после операции.
Результат гистологического исследования (Dr. L. Mecklenburg, PhD):
Описание
Ткань тимуса. Вся тимическая архитектура разрушена массивным кровоизлиянием. Строма чрезвычайно расширена и заполнена массивными кровоизлияниями. Кортикальные лимфоциты и лимфоциты мозгового слоев располагаются россыпью и их практически не видно из-за крови. Нет доказательств неоплазии.
Диагноз
Тяжелое кровоизлияние в тимус, совместимое с идиопатическим кровоизлиянием в тимус у молодых собак.
Комментарий
Эта морфология тимуса совместима со спонтанной идиопатической болезнью у молодых собак, которая известна как «идиопатическое кровотечение в тимус». Кровоизлияние затрагивает тимус и ткани средостения. Страдают собаки обычно моложе 1 года. Этиология этого расстройства неизвестна. Можно рассмотреть отравление родентицидами.
Пациент находился в отделении интенсивной терапии в течение 6 суток после операции, выписан домой в удовлетворительном состоянии, через 1,5 года в хорошем состоянии приходил на плановую овариогистерэктомию.
Обсуждение тактики лечения и анестезиологического пособия
Данный пациент является очень интересным не только с точки зрения самой патологии, выбора тактики лечения, но и с точки зрения его ведения анестезиологом.
Первая проблема, с которой мы столкнулись – наличие у пациента геморрагического шока (гипотермия, угнетенное сознание, тахикардия, гипотензия). Идеальным продуктом для лечения геморрагического шока является донорская кровь или эритроцитарная масса. Поскольку в клинике есть банк крови, пациенту сразу проведена гемотрансфузия. Объем трансфузии зависит от объема кровопотери, продолжения кровотечения. Наш пациент получил 23 мл/кг, этого хватило для купирования симптомов шока и нормализации состояния. Если крови в наличии нет, необходимо стабилизировать давление малообъемной инфузией (растворы кристаллоидов, коллоидов, гипертонический раствор натрия хлорида) для поддержания среднего давления около 60 мм рт. ст, чтобы пациент мог дожить до гемотрансфузии. Объемное возмещение кровопотери растворами кристаллоидов и/или коллоидов может усиливать кровопотерю, способствовать развитию коагулопатии. Такой тяжелый шок с объемной кровопотерей без гемотрансфузии имеет очень низкие шансы на выживание. В ситуации, когда донорская кровь не может быть предоставлена в короткие сроки, можно рассмотреть вариант аутогемотрансфузии.
Вторая возможная проблема – дыхательная недостаточность из-за гемоторакса. Обычно при гемотораксе симптомы геморрагического шока проявляются раньше, чем симптомы тяжелой дыхательной недостаточности. Однако объемный гемоторакс может дополнительно ухудшать состояние пациента и требовать торакоцентеза. Но это необходимо не всегда. Если явных нарушений дыхания нет, то полностью удалять кровь из плевральной полости нет необходимости. Нашему пациенту при поступлении был проведен торакоцентез, слито 400 мл геморрагической жидкости для облегчения дыхания.
Третья проблема – возможные осложнения шока. При длительном падении артериального давления снижается перфузия внутренних органов, поэтому даже после успешного лечения шока может развиться шоковый кишечник, острое повреждение почек и другие осложнения, приводящие к синдрому полиорганной недостаточности.
Помимо этого требуется принять решение о тактике лечения такого пациента – хирургической или консервативной. По литературным данным спонтанное кровотечение из тимуса может остановиться самостоятельно, поэтому оправдана выжидательная тактика: переливание крови для восполнения кровопотери и ожидание остановки кровотечения. Этот способ имеет свои минусы: может потребоваться большой объем гемотрансфузии (необходимо наличие донорской крови в достаточном объеме), большая кровопотеря приводит к значимой потере факторов свертывания (необходима свежая донорская кровь и/или свежезамороженная плазма для восполнения факторов свертывания), объемная гемотрансфузия имеет свои побочные эффекты (трансфузионные реакции), может потребоваться торакоцентез для удаления большого количества крови из плевральной полости. Хирургическое лечение позволяет сразу взять кровотечение под контроль, однако тоже имеет свои минусы – это торакальная операция, со всеми рисками хирургического вмешательства и анестезии, требующая определенных навыков у хирурга.
Если выбрана хирургическая тактика лечения, необходимо убедиться, что у пациента нет значимой гипокоагуляции, иначе операция может спровоцировать ещё большее кровотечение. При отсутствии возможности сделать экстренную коагулограмму или тромбоэластографию нужно хотя бы провести тест на время свертывания крови (ВСК). Продленное ВСК (отсутствие полного свертывания крови в пробирке более 7-10 минут (по некоторым данным, до 12 минут)), будет говорить о наличии тяжелой коагулопатии. Идти с таким пациентом на операцию, не нормализовав свертываемость с помощью переливания свежей донорской крови или свежезамороженной плазмы, нельзя.
При поступлении нашего пациента мы начали с консервативной тактики, состояние стабилизировалось после гемотрансфузии. Однако, поскольку симптомы гиповолемии повторились, что говорило о продолжающемся кровотечении, было принято решение о хирургическом лечении.
Подготовка к анестезии у данного пациента заключается в быстрой стабилизации состояния до анестезии (согревание, купирование симптомов шока). Однако, поскольку речь идет о геморрагическом шоке, у врача нет цели полностью нормализовать давление, так как нормальное или повышенное давление будет приводить к более быстрой потере крови. В данном случае задача анестезиолога – поддерживать среднее артериальное давление не менее 60 мм рт. ст. до остановки кровотечения хирургом.
Такие пациенты гемодинамически нестабильны, премедикация им обычно не проводится, сразу проводится внутривенно индукция под контролем состояния. Пациентам в тяжелом состоянии может требоваться меньшая доза препаратов. Основными препаратами выбора в данном случае должны быть анестетики, минимально влияющие на гемодинамику. Оптимальным сочетанием будут опиоиды, бензодиазепины и диссоциативные анестетики (кетамин или тилетамин+золазепам). К сожалению, в отсутствие опиоидов, на одном тилетамине/золазепаме невозможно обеспечить адекватную аналгезию на подобной операции. Применения альфа2-агонистов таким нестабильным пациентам лучше избегать, однако их можно добавить в виде инфузии с постоянной скоростью (меньше риск нарушений гемодинамики) после хирургической остановки кровотечения, или если пациент стабилен.
Для поддержания анестезии можно с осторожностью использовать пропофол и/или изофлюран. Эти препараты могут вызывать гипотензию, однако, они легко управляемы, поэтому при аккуратном применении и тщательном мониторинге могут быть использованы в составе анестезиологического пособия.
Также в некоторых случаях при торакальных операциях возможно применение деполяризующих миорелаксантов, хотя при операциях у мелких домашних животных в их применении не всегда есть необходимость.
Как и для любой другой торакальной операции, необходима искусственная вентиляция легких.
Протокол анестезии данного пациента включал:
-
антибиотикопрофилактика: цефазолин 30 мг/кг внутривенно;
-
индукция: золетил 2 мг/кг внутривенно, пропофол 2 мг/кг внутривенно;
-
интубация трахеи трубкой №6,0;
-
поддержание анестезии: золетил 2 мг/кг болюсно однократно, ИПС 1 мг/кг/ч, изофлюран 1 об%, тракриум 0,5 мг/кг однократно перед проведением хирургического доступа, ИПС дексдомитор 0,5 мкг/кг/час, ИПС лидокаин 40 мкг/кг/мин.
-
дыхание: ИВЛ pressue control;
-
инфузия: раствор Рингера 40 мл/кг, волювен 5 мл/кг, цельная кровь 17 мл/кг, после стабилизации гемодинамики р-р Рингера ИПС 5 мл/кг/час;
-
длительность анестезии: 3 часа 20 минут;
-
осложнения анестезии: не возникло.
У пациента была массивная кровопотеря (не менее 50% ОЦК) с объемной гемотрансфузией (около 40% ОЦК), в такой ситуации велик риск развития коагулопатии потребления из-за большой потери факторов свертывания (консервированная донорская кровь факторов свертывания не содержит), поэтому после операции также была проведена трансфузия СЗП в объёме 15 мл/кг для профилактики коагулопатии.
Послеоперационное лечение
Наш пациент пережил несколько проблем: геморрагический шок, объемная кровопотеря, стернотомия.
Таким пациентам необходим тщательный послеоперационный мониторинг для своевременного выявления осложнений. Проблемы, которые можно ожидать: болевой синдром, развитие шокового кишечника, острое повреждение почек, острая сердечная недостаточность, коагулопатия.
Также важно помнить о необходимости адекватного питания для более успешного восстановления данных пациентов. Необходимо как можно раньше начинать энтеральное питание (в том числе с использованием назогастрального зонда или эзофагостомической трубки при отсутствии самостоятельного аппетита), при невозможности энтерального питания (например, неукротимая рвота) – рассмотреть вариант парэнтерального питания.
Аналгезия данного пациента требует мультимодального подхода (стернотомия относится к операциям с очень высокой степенью послеоперационного болевого синдрома). Разумеется, в развитых странах при обезболивании таких пациентов обязательно используются опиоиды, применение которых, к сожалению, ограничено в России. При отсутствии опиоидов таким пациентам можно применять ИПС диссоциативных анестетиков для контроля болевого синдрома. Также из-за риска шокового кишечника таким пациентам необходимо ограничить применение НПВС, хотя бы в первые сутки-трое после операции (до восстановления аппетита).
Данный пациент получал в качестве аналгезии ИПС дексдомитора 0,5-1 мкг/кг/ч, лидокаина 30-50 мкг/кг/мин, золетила 0,25-1 мг/кг/ч, метамизол 20 мг/кг 1р/8 ч.
Также у пациента развился гастроэнтерит (последствие шока, усугубление имеющейся патологии (рвота в анамнезе)) – отсутствие аппетита, тошнота, снижение перистальтики ЖКТ по УЗИ, что потребовало применения гастропротекторов (омепразол), прокинетиков (метоклопрамид), антиэметиков (маропитант).
В первые сутки после операции у пациента наблюдалась умеренная гипокоагуляция по данным коагулограммы (вероятно, на фоне объемной кровопотери), в последующем – гиперкоагуляция. Был добавлен фрагмин 150 МЕ/кг 1 р/12 ч для тромбопрофилактики.
Также проводился контроль водно-электролитного баланса, энтеральное питание.
Выписка на 6-е сутки в удовлетворительном состоянии.
Обсуждение
Спонтанное кровотечение тимуса у собак достаточно редкая, но описанная патология. В наше клинике за последние несколько лет было диагностировано 3 случая спонтанного кровотечения тимуса, включая описанного пациента. Всем проведено хирургическое лечение с последующей успешной выпиской. Все 3 собаки имели те или иные нарушения коагуляционного статуса, однако хирургическое лечение совместно с консервативной терапией приводили к полному клиническому выздоровлению пациентов.
По литературным данным, хирургическое лечение требуется не всегда, нередко патология ассоциирована с отравлением антикоагулянтами [4]. В литературе были также представлены случаи отравления антикоагулянтами, проявившиеся у молодой собаки кровоизлиянием именно в тимус. Случай не потребовал хирургического лечения, однако может указывать на то, что тимус у молодых собак является «слабым местом» [3].
Выбор метода лечения остается на усмотрение врача в каждом конкретном случае, исходя из данных анамнеза, доступности препаратов крови (цельная кровь и донорская плазма), наличия необходимого оборудования для проведения торакальной операции, наличия хирурга, обладающего достаточным опытом для подобного хирургического вмешательства. Также следует подробно обсуждать с владельцем все варианты лечения, плюсы и минусы консервативной терапии и хирургического лечения.
Выводы
Диагноз «спонтанное кровотечение тимуса» следует включать в список дифференциальных диагнозов при выявлении гемоторакса у животных младше 12 месяцев.
Невозможно достоверно исключить кровотечение вследствие коагулопатии (5)
Хирургическое лечение показало эффективность в нашей практике, однако не является 100% рекомендованным методом по литературным данным.
Терапевтическое лечение в мировой практике показало эффективность, однако следует всегда учитывать доступность препаратов крови, так как может требоваться более 1 трансфузии за время лечения.
При проведении анестезиологического пособия необходим адекватный контроль геморрагического шока, тщательный мониторинг, восполнение потери факторов свертывания и выбор препаратов, минимально влияющих на гемодинамику.
В зависимости от исходной тяжести состояния и длительности шока, пациенту может потребоваться лечение в условиях клиники в течение нескольких дней.
Литература
1.Small Animal Pediatric Medicine Tufts Animal Expo 2002 Johnny D. Hoskins, DVM, Ph.D. DocuTech Services, Inc. Baton Rouge, Louisiana, USA) 1.
2.1 Measurement of Thymic Output and Evidence of Immunosenescence in Labrador Retriever Dogs 23rd ECVIM-CA Congress, 2013 A.L. Holder; S. Mella; D. Palmer; B. CatchpoleRoyal Veterinary College, Hatfield, UK.
2.2 Radiology of The Mediastinum WSAVA 2002 Congress Amalia Agut, DVM, PhD, DipECVDI Departamento de Patología Animal. Facultad de Veterinaria. Campus de Espinardo Murcia, Spain
3.Thymic haemorrhage due to ingestion of human anticoagulant medication in a puppy Vet Rec Case Rep. November 2017; 5 (4):e000552. Emilie Vangrinsven, Maud Girod, Anne-Laure Etienne, Kris Gommeren).
4. Acute Thymic Hemorrhage and Hemothorax in a Dog J Am Anim Hosp Assoc. 1993 Nov-Dec;29 (6):489-491. 12 Refs Tony M Glaus 1, Clarence A Rawlings, Edward A. Mahaffey, Mary B Mahaffey
5. Thymic hematoma in juvenile dogs associated with anticoagulant rodenticide toxicosis. Alan D. Liggett, Larry J. Thompson, Ken S. Frazier, Eloise L. Styer, Lowell T. Sangster.

Назад в раздел


















