Безопасность циклоспорина при длительном лечении атопического дерматита. Обзор. Часть 1
Еще фото
Автор (ы): T. Nuttall, D. Reece, E. Roberts
Журнал: №4 - 2014
УДК 619:616.5-002
Перевод с английского A.H. Герке
Ключевые слова: циклоспорин, атонический дерматит
Key words: ciclosporin, atopic dermatitis
Аннотация
Циклоспорин (Atopica; Novartis Animal Health) был лицензирован для лечения собак с атопическим дерматитом (АД) в 2002 г. Побочные эффекты (ПЭ) были зарегистрированы у 55% из 759 собак, принявших участие в 15 клинических исследованиях, однако, по данным производителя, они редки (71,81 ПЭ / млн проданных капсул). Наиболее часто отмечены желудочно-кишечные расстройства, тем не менее, они протекали легко и не требовали вмешательства. Другие ПЭ встречались реже (<1% в клинических исследованиях, <10 / млн проданных капсул). Гипертрихоз, гиперплазия десен и гиперпластический дерматит редко имеют клиническое значение и регрессируют при снижении дозы. Использование циклоспорина снижает риск развития стафилококковой и малассезиозной инфекций при АД, в рекомендованной дозе не является фактором риска для других инфекций, новообразований, почечной недостаточности или гипертонии. Воздействие на метаболизм глюкозы и кальция не является клинически значимым для собак. Сопутствующее применение большинства препаратов является безопасным. Воздействие на активность цитохрома Р450 и MDR1 P-гликопротеина может повышать концентрации в плазме циклоспорина, но краткосрочные изменения не являются клинически значимыми. Мониторинг общего анализа крови, анализ мочи или концентраций циклоспорина не всегда оправданы, кроме случаев применения более высоких, чем рекомендуются, доз и/или долгосрочного одновременного использования иммунодепрессантов. Применение циклоспорина не является противопоказанием для проведения вакцинации убитыми вакцинами (в том числе против бешенства), однако, по лицензированным рекомендациям, следует избегать использования живых вакцин во время лечения. Подводя итог, можно сказать, что циклоспорин имеет низкий уровень риска при долгосрочном лечении АД собак.
Summary
Ciclosporin (Atopica; Novartis Animal Health) has been licensed for canine atopic dermatitis (AD) since 2002. Adverse events (AEs) have been reported in 55 per cent of 759 dogs in 15 clinical trials, but are rare in pharmacovigilance data (71.81 AEs/million capsules sold). Gastrointestinal reactions were most common, but were mild and rarely required intervention. Other AEs were rare (<1 per cent in clinical trials; <10/million capsules sold). Hirsutism, gingival hyperplasia and hyperplastic dermatitis were rarely significant and resolved on dose reduction. Ciclosporin decreases staphylococcal and Malassezia infections in AD, and at the recommended dose is not a risk factor for other infections, neoplasia, renal failure or hypertension. The impact on glucose and calcium metabolism is not clinically significant for normal dogs. Concomitant treatment with most drugs is safe. Effects on cytochrome P-450 and MDR1 P-glycoprotein activity may elevate plasma ciclosporin concentrations, but short-term changes are not clinically significant. Monitoring of complete blood counts, urinalysis or ciclosporin levels is not justified except with higher than recommended doses and/or long-term concurrent immunosuppressive drugs. Ciclosporin is not a contraindication for killed (including rabies) vaccines, but the licensed recommendation is that live vaccination is avoided during treatment. In conclusion, ciclosporin has a positive risk-benefit proile for the long-term management of canine AD.
|
СОКРАЩЕНИЯ | |||
|
АД |
атопический дерматит |
ПЭ |
побочные эффекты |
|
|
|
|
|
Циклоспорин (cyclosporine, cyclosporin А или CsA) является циклическим олигопептидом – макролидом, ингибирующим цитоплазматическую фосфатазу кальциневрина (Steffan с соавторами, 2006). Циклоспорин блокирует индукцию генов различных цитокинов и рецепторов к цитокинам, проявляя иммуномодулирующую активность. Его воздействие на цитокины, влияющие на активацию, пролиферацию и продолжительность жизни клеток, участвующих в иммунном ответе кожных покровов и аллергических реакциях, в том числе клеток Лангерганса, лимфоцитов, тучных клеток и эозинофилов, было предпосылкой использования его для лечения собак с атопическим дерматитом (АД). Небольшое открытое исследование, показавшее эффективное воздействие на клинические проявления АД, в том числе на зуд, было опубликовано в 2001 г. (Fontane и Olivry, 2001). С тех пор были проведены другие многочисленные исследования в США, Европе, Японии и Австралии. Циклоспорин был лицензирован для лечения собак с АД в 2002 г. под названием Атопика (Atopica®, Novartis Animal Health) и в настоящее время зарегистрирован и доступен в 23 странах по всему миру. В 2006 г. мета-анализ 10 исследований, в которых участвовали 799 собак, показал, что оральное использование циклоспорина было так же эффективно, как и системные глюкокортикоиды (Steffan с соавторами, 2006). Другие мета-анализы и систематические обзоры также подтвердили, что циклоспорин обладает высокой эффективностью при лечении собак с АД (Olivry и Mueller, 2003, Olivry с соавторами, 2010, Olivry и Bizikova, 2013). В 2010 г. Международная целевая группа по атопическому дерматиту собак (сейчас Международный комитет по аллергическим болезням животных [ICADA]) опубликовала рекомендации по лечению собак с АД, в которых циклоспорин специально рекомендуется при лечении хронического АД (Olivry с соавторами, 2010).
АД собак является болезнью молодых животных, характерные проявления которой бывают в возрасте от 6 месяцев до 3 лет (Favrot с соавторами, 2010). Это хроническая рецидивирующая болезнь, и большинство собак нуждается в терапии, как правило, на протяжении всей жизни. Поэтому важно понять долгосрочную безопасность терапевтических вмешательств, чтобы сбалансировать эффективность и побочные эффекты с целью поддержания хорошего качества жизни. Данные по безопасности для регистрации, как правило, включают в себя только данные клинических испытаний на относительно небольшой группе собак, получавших препарат от нескольких недель до нескольких месяцев. Следовательно, мониторинг безопасности и эффективности на рынке лекарственных средств через Фармаконадзор (PV) является важным и эффективным инструментом для оценки безопасности и эффективности препарата. Побочные эффекты, которые развиваются медленно, а также породные особенности и лекарственные взаимодействия могут быть не очевидными во время клинических испытаний. С позиции Фармаконадзора, при возникновении любых побочных эффектов, токсичности или реакции гиперчувствительности при использовании препарата для животных необходимо доказать их связь с воздействием препарата, примененного в соответствии с утвержденной инструкцией. За 10 лет доступности Атопики было продано 142 млн доз циклоспорина (Roberts с соавторами, 2012), что позволило получить большой объем данных о его безопасности у собак с АД. Целью данного обзора является анализ опубликованных работ и данных Фармаконадзора о распространенности побочных эффектов, связанных с лечением циклоспорином. Эти данные будут полезны для клиницистов при обсуждении вариантов лечения с владельцами собак с АД.
Анализ побочных эффектов, связанных с лечением циклоспорином
При лечении циклоспорином был отмечен широкий спектр побочных эффектов. В данном обзоре эти ПЭ сгруппированы по системам организма и/или тканям, подробно рассмотрена сила связи этих явлений с использованием циклоспорина и относительность ПЭ. При подготовке этого обзора использован ряд различных отчетов, которые содержат данные Фармаконадзора, экспериментальные исследования, отдельные тематические исследования, клинические испытания, мета-анализы и систематические обзоры. В частности, трудно определить значимость побочных эффектов в исследовании без контрольной группы, чтобы проанализировать связь с ПЭ и рассчитать вероятность риска. Это неоправданно повышает вероятность развития конкретных нежелательных явлений при использовании циклоспорина при АД, по мнению Фармаконадзора, однако вероятность их возникновения соизмерима со случайным возникновением в контрольной группе и популяции собак в общем. Данные об отдельных клинических случаях достаточно ограничены, могут быть случайными проявлениями, часто не связанными с заболеваниями или сопутствующей терапией, поэтому такая ассоциация является гипотетической. Вполне убедительная связь с циклоспорином может быть установлена в случаях, например, когда нежелательные эффекты возникают в начале лечения и их проявления снижаются при уменьшении дозы или прекращении терапии. Тем не менее, возможными трудностями для выявления причинно-следственной связи может быть сопутствующая терапия или состояние собаки, которое также может объяснить наличие возникших клинических признаков. Основой доказательства связи между воздействием препаратов и их побочными эффектами является детализированное медицинское наблюдение при использовании препарата, однако не существует конкретных диагностических критериев. Несколько методов (например, шкала Нараньо, система ABОN, метод RUCAM, модифицированный алгоритм Крамера и др.) были использованы для определения причинной связи или оценки ПЭ. К сожалению, очень мало опубликованных ветеринарных отчетов используют эти шкалы для оценки. Важно также отметить, что анализ побочных эффектов и соотношения риска и пользы при пожизненном применении препарата будет считаться приемлемым, несмотря на высокую распространенность легких побочных эффектов, но было бы неприемлемо для тяжелых побочных эффектов, даже при низкой их распространенности.
Побочные эффекты, связанные с лечением циклоспорином собак с атопическим дерматитом
В этой статье проанализированы и рассмотрены данные исследований, проведенных рецензируемыми специалистами в данной области и опубликованных отчетов клинических испытаний циклоспорина при АД собак в стандартных дозах (т.е. начальная доза составила примерно 5 мг/кгодин раз в день,с постепенным снижением при достижении клинического эффекта). Была использована мелкодисперсная эмульсия циклоспорина Атопика для перорального применения. Неопубликованные исследования, экспериментальные исследования на здоровых собаках, исследования на других видах животных и случаи применения препарата для лечения болезней, не указанных в инструкции, а также использование в других условиях, в других дозах и/или в сочетании с другими препаратами не были включены в анализ. Тем не менее, эти данные могут быть использованы в случае необходимости при обсуждении некоторых побочных эффектов. В обзоры, предоставленные Фармаконадзором, были включены данные о применении препарата при состояниях, не указанных в инструкции (off-label), а также в других дозах и в сочетании с другими препаратами.
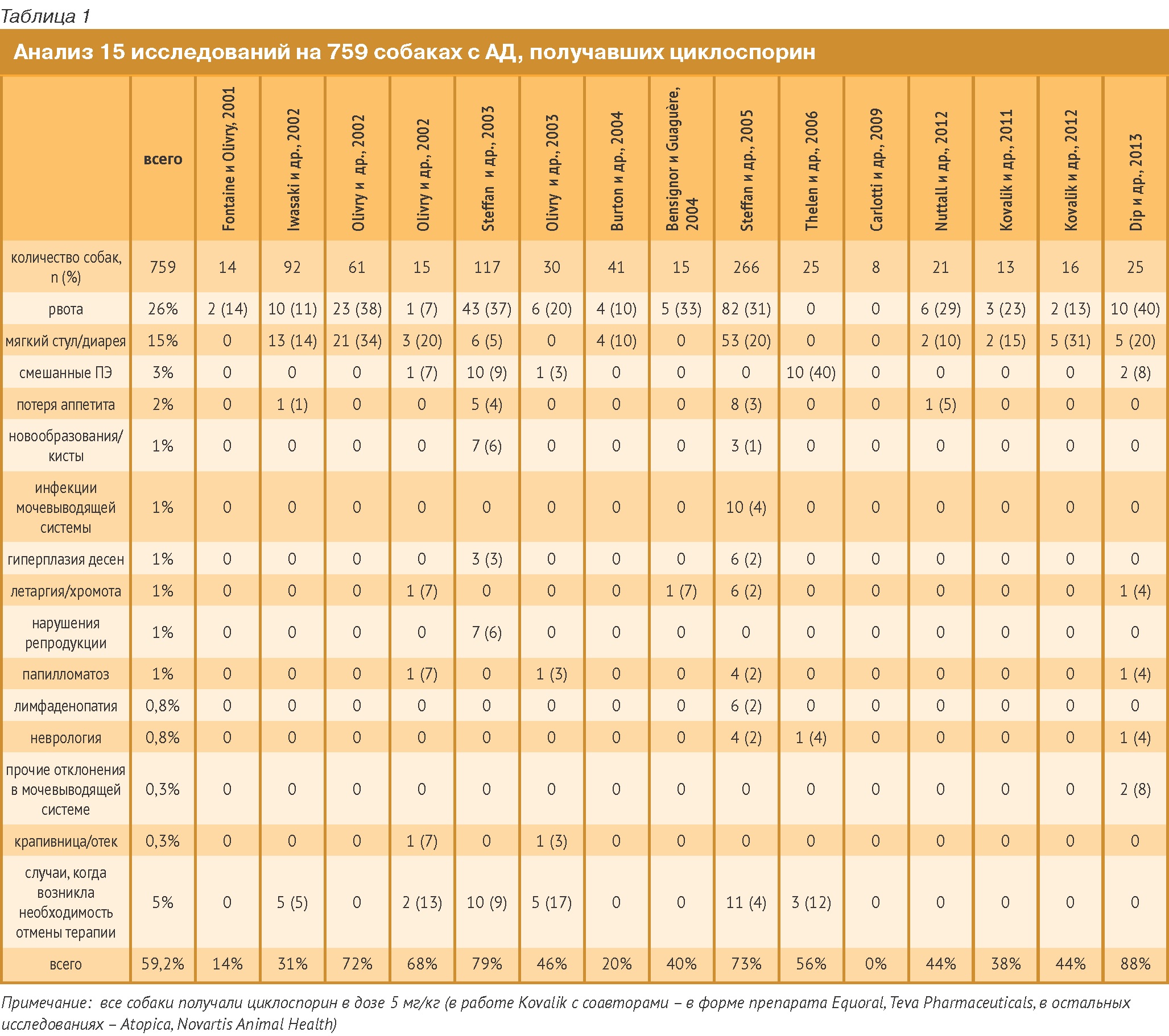
В результате был проведен мета-анализ 15 исследований на 759 собаках. Во всех, за исключением одного исследования, была использована Атопика, мелкодисперсная эмульсия циклоспорина для орального применения. Исключение составило одно исследование (Kovalik с соавторами, 2011), где был применен дженерик Equoral (производитель Teva Pharmaceuticals). Полученные данные представляют собой отчет, где учтены все собаки, у которых был отмечен какой-либо ПЭ (Табл. 1). Эти данные приблизительны, поскольку не всегда было ясно, наблюдалось ли у некоторых собак более одного ПЭ (и, следовательно, они были подсчитаны более одного раза), или было несколько эпизодов одного и того же ПЭ у одной собаки (которые уже были посчитаны в предыдущий раз). Наконец, побочные эффекты, которые были явно не связаны с лечением, были проигнорированы (например, дорожно-транспортные происшествия, травмы, инородные тела и т.д.). Был использован мета-анализ (Roberts с соавторами, 2012) для оценки последовательности и завершенности данных Фармаконадзора (Табл.2).
У 420 из 759 собак, получавших циклоспорин (55%, с диапазоном от 0 до 88% среди отдельных исследований), по крайней мере, однократно были зарегистрированы какие-либо ПЭ. Тем не менее, большинство из них были незначительными и самопроизвольно прекращались, лишь в 4% случаев (диапазон от 0 до 17%) требовалось прекращение лечения.
Наиболее частыми побочными эффектами были желудочно-кишечные (51%, диапазон от 0 до 60%), что согласуется с данными Фармаконадзора, другие ПЭ зарегистрированы не более чем у 1% собак. Отмечены значительные различия между исследованиями, которые, вероятно, связаны с количеством собак и продолжительностью лечения. Также присутствовали некоторые различия в терминологии ПЭ (например, между различными нарушениями желудочно-кишечного тракта и клиническими признаками патологии мочевыводящих путей). Клинически незначимые отклонения в гематологии, биохимии и других параметрах не были описаны в виде отдельных ПЭ, но были учтены при расчете средних значений, что будет обсуждаться ниже.
Желудочно-кишечные побочные эффекты
Желудочно-кишечные расстройства являются наиболее частыми побочными эффектами, возникающими при использовании циклоспорина. Они наблюдались у 46% из 759 собак, причем, по данным большинства исследований, это было единственным ПЭ. По данным Фармаконадзора, также наиболее частыми ПЭ были рвота и диарея (Табл.2). В другом мета-анализе, проведенном на 672 собаках с атопическим дерматитом, получавших циклоспорин, желудочно-кишечные нарушения были зафиксированы у 306 (45%) собак, в то время как другие неблагоприятные эффекты наблюдались менее чем у 2,1% (Steffan с соавторами, 2006). Тем не менее, эти значения распространенности желудочно-кишечных расстройств могли быть преувеличены, поскольку у отдельных собак одни и те же ПЭ были учтены несколько раз. Рвота, отмеченная у 25-31% собак, встречалась в три-четыре раза чаще у животных, получавших циклоспорин, по сравнению с контрольной группой. Мягкий стул, диарея и/или другие ПЭ наблюдались у 18-20% собак, получавших циклоспорин, что примерно вдвое превышает аналогичный показатель в контрольных группах (Табл. 1) (Steffan с соавторами, 2006). Частота возникновения этих ПЭ, по-видимому, зависит от дозы и может быть связана с обратимым повреждением микроворсинок, вызванным наполнителями микроэмульсии препарата для орального применения (Nerurkar с соавторами, 1996). Желудочно-кишечные расстройства в большинстве случаев протекали легко, проявлялись в виде повторяющихся или длительных эпизодов рвоты, случаи других ПЭ были редки (Steffan с соавторами, 2006). Два исследования были специально посвящены желудочно-кишечным ПЭ у собак (Olivry с соавторами, 2002, Steffan с соавторами, 2005).У животных с минимальными проявлениями желудочно-кишечных ПЭ (от 53 до 73% собак с ПЭ) наблюдались эпизоды рвоты от 1 до 3 раз в течение трех месяцев, как правило, в первый месяц лечения. Только у 10% собак наблюдались повторяющиеся спорадические эпизоды рвоты, которые были тяжелыми ПЭ только в 1% случаев (Steffan с соавторами, 2005).
В одном крупном исследовании диарея наблюдалась у 53 из 266 собак (20%), в том числе у 10 – с сопутствующей рвотой. Как правило, эти ПЭ развивались в первый месяц лечения (Steffan с соавторами, 2005), у большинства животных эти симптомы прошли без лечения (за исключением двух) и были признаны тяжелыми только у одной собаки. Отдельные эпизоды были замечены у 43% собак, в то время как повторяющиеся случаи – в 28%. Чаще всего эти ПЭ прекращались спонтанно, при этом клинические проявления продолжались более семи дней только у 13% животных. Потеря аппетита наблюдалась только у 2% собак (Табл.1) (Steffan с соавторами, 2006) и, как правило, была связана с рвотой или диареей (Steffan с соавторами, 2005). Потеря веса встречалась реже, чем у 1% животных (Steffan с соавторами, 2006); в одном исследовании только у одной из 266 собак наблюдалась потеря веса, которая была вызвана гепатопатией, несвязанной с лечением (Steffan с соавторами, 2005). Тяжелые желудочно-кишечные проблемы были редки, по данным Steffan с соавторами (2005), только двум из 266 собак требовалось прекращение лечения.
Выводы и рекомендации
Желудочно-кишечные реакции являются наиболее частыми ПЭ у собак, получавших циклоспорин. Как правило, эти проявления протекают легко и не требуют лечения. Отмена лечения циклоспорином была необходима редко.
По литературным данным, для снижения вероятности рвоты и/или диареи, рекомендуется начинать лечение с низкой дозы (от 1 до 2 мг/кг каждые 24 часа) с постепенным увеличением до терапевтической дозы (5 мг/ кг каждые 24 часа) или увеличением интервала между приемами препарата (например, от ежедневного до 1 раза в 2 дня или 2-х раз в неделю). Другие варианты включают охлаждение или замораживание циклоспорина за 30-60 мин. до введения (Palmeiro, 2013). Прием циклоспорина с кормом также может быть эффективен (Palmeiro, 2013), хотя в другом небольшом исследовании побочные эффекты встречались с одинаковой частотой, вне зависимости от кормления (Thelen с соавторами, 2006). При необходимости для контроля рвоты можно использовать противорвотные препараты (например, маропитант или метоклопрамид) (Palmeiro, 2013) или гастропротекторы (например, сукральфат, циметидин или ранитидин). Сукральфат следует давать не менее чем за час до приема циклоспорина, чтобы избежать снижения всасывания и биодоступности. Добавки в корм продуктов с высоким содержанием клетчатки (например, консервированной тыквы) и пробиотиков помогают снизить такие ПЭ, как мягкий стул или диарея (Palmeiro, 2013). Использование цинк-карнозина и витамина Е (Gastri-Calm;Teva Animal Health) не снижало проявления желудочно-кишечных побочных эффектов, связанные с терапией циклоспорином (Wilson с соавторами, 2011).
Папилломатоз, псориаформный и веррукозный дерматиты
Папилломатоз и другие гиперпластические поражения кожи были отмечены у 5 из 672 (0,7%) собак в одном мета-анализе (Steffan с соавторами, 2006). Пролиферативные кожные поражения отмечены в 1% случаев из 759 собак (Табл. 1). Также было описано три случая псориаформного лихеноидного дерматоза (Werner, 2003). При отмене циклоспорина и проведении лечения антибиотиками наблюдалась регрессия этих ПЭ. Возникшие на фоне лечения циклоспорином папилломы и бородавки рассасывались при снижении дозы или отмене препарата (Seibel с соавторами, 1989, Olivry с соавторами, 2002, Favrot с соавторами, 2005). Частота и тяжесть этих проявлений зависят от дозы препарата, так, в одном исследовании (Donatsch и Ryffel, 1986) генерализованный папилломатоз развился у 5 из 8 собак, получавших 45мг/кг ежедневно в течение 12 месяцев. Эти поражения редко были связаны с папилломавирусной инфекцией (Donatsch и Ryffel, 1986, Favrot с соавторами, 2005). По результатам другого исследования, у 7 из 9 собак с клинической картиной псориаформного лихеноидного дерматоза не было обнаружено вируса папилломы при иммуногистохимическом исследовании и ПЦР (Favrot с соавторами, 2005). Гистологическое доказательство присутствия стафилококков поддерживает предположение, что эти повреждения, по крайней мере, частично представляют собой реакцию на бактериальную колонизацию и/или инфекцию (Werner, 2003).У двух других собак с веррукозными поражениями присутствовали гистопатологические доказательства вирусной инфекции, в том числе койлоцитоз и ядерные вирусные включения. В этих повреждениях методом ПЦР были выделены ДНК вирусов оральной папилломы и папилломы собак 2 типа. При отмене циклоспорина эти поражения регрессировали без дополнительного лечения. Еще был зарегистрирован один случай вирусного папилломатоза ротовой полости у собаки с атопическим дерматитом (Radowicz и Power, 2005), при котором одиночную папиллому успешно удалили хирургически без рецидива, несмотря на продолжающееся лечение циклоспорином.
Выводы и рекомендации
На фоне лечения циклоспорином могут развиваться различные гиперпластические поражения кожи у собак. Они достаточно редки, как правило, не имеют большого клинического значения, не требуют снижения дозы или приостановки лечения. Это утверждение также согласуется с данными, представленными Фармаконадзором.
Гиперплазия десен
Гиперплазия десен в этом обзоре отмечена у 1% (Табл. 1), у 1,7%, по данным мета-анализа, проведенного на 609 собаках (С. Favrot, неопубликованные данные), и у 1,3%, по данным другого исследования, проведенного на 672 собаках (Steffan с соавторами, 2006). В большинстве случаев степень гиперплазии десен была слабой, что не требовало прекращения терапии циклоспорином. Гиперплазия, вероятно, связана с трансформирующим фактором роста бета (TGFP) – медиатором пролиферации внеклеточного матрикса (Stabellini с соавторами, 2002). Этот эффект, по-видимому, зависит от дозы, хотя наблюдаемые индивидуальные различия могли отражать особенности обмена веществ и фармакодинамики у некоторых собак (Seibel с соавторами, 1989). Гиперплазия десен была достаточно сильно выражена в группе собак, получавших 45 мг/кг в день в течение 12 месяцев (Donatsch и Ruffel, 1986). В экспериментальном исследовании по трансплантации у 3 из 4 собак, получавших циклоспорин в дозах, скорректированных по концентрации препарата в цельной крови от 400 до 700 нг/мл, спустя 20 недель от начала терапии развилась гиперплазия десен от умеренной до тяжелой степени. Несмотря на это, эти собаки также получали азатиоприн и в течение первых трех месяцев преднизолон для предотвращения отторжения трансплантата (Nam с соавторами, 2008).
Выводы и рекомендации
Гиперплазия десен развивается редко при использовании стандартных доз циклоспорина, применяемых для лечения собак с АД. В большинстве случаев гиперплазия десен протекает легко и не имеет клинического значения, но в редких случаях может развиться значительная окклюзия зубов и гингивит. Гиперплазия десен подвергается обратному развитию при снижении дозы или прекращении лечения. В легких случаях для предотвращения гингивита может потребоваться дополнительная гигиена полости рта. Был установлен положительный эффект при сопутствующем применении азитромицина у людей (Ramalho с соавторами, 2007). В одном исследовании на 36 собаках с гиперплазией десен, вызванной циклоспорином, чистка с зубной пастой, содержащей 8,5% азитромицина, или системное использование азитромицина (10 мг/кг) каждые 24 часа снижало глубину борозды десен при субъективной оценке по сравнению с группой плацебо. Только у одной собаки, получавшей азитромицин системно, отмечена полная ремиссия (Rosenberg с соавторами, 2013).
Гирсутизм или гипертрихоз
О гирсутизме или гипертрихозе редко сообщается как о ПЭ, их встречаемость составляет менее 1% в одном неопубликованном мета-анализе, проведенном на 609 собаках (С. Favrot, неопубликованные наблюдения). По другим данным, гирсутизм и/или гипертрихоз встречается достаточно часто у собак на фоне лечения циклоспорином (Seibel с соавторами, 1989, Robson и Burton, 2003). В начале лечения, примерно в течение 4-6 недель от начала терапии циклоспорином, у некоторых животных наблюдалось выпадение шерсти. Циклоспорин оказывает влияние на волосяной фолликул, продлевая фазу анагена, и побуждает фолликулы, находящиеся в катагене и телогене, к переходу в анаген. Это приводит к синхронизации фазы телогена и усилению линьки. Затем рост шерсти возобновляется, вероятно, в связи с циклоспорин-индуцированным ингибированием кальцинейрина-NFATl в фолликулах, что приводит к росту более густого и глянцевого шерстного покрова (Gafter-Gvili с соавторами, 2003).
Выводы и рекомендации
Гирсутизм или гипертрихоз является положительным ПЭ при терапии циклоспорином. Этот эффект редко клинически значим, однако некоторым собакам может потребоваться более частый уход, особенно в межпальцевых областях.
Инфекции
Долгосрочное использование иммуномодулирующих препаратов может увеличить риск заражения бактериальной, грибковой, вирусной инфекциями, а также простейшими и другими паразитами, такими как Demodex. Иммуносупрессивная активность циклоспорина зависит от дозы и продолжительности лечения, связана с подавлением интерлейкинов (IL-2, IL-4), интерферона IFN-y, CD25 и CD95 при активировании Т-клеток (Fellman с соавторами, 2011), несмотря на то что у здоровых собак только воздействие на ИЛ-2 и IFN-y были значительными (Archer с соавторами, 2011). Одно исследование с использованием 5 мг/кг циклоспорина (Equoral) в день в течение 42 дней у 13 собак не показало никаких существенных воздействий на метаболизм или функциональную активность фагоцитов по сравнению с 1 мг/кг преднизолона (Kovalik с соавторами, 2011). Дальнейшие исследования in vitro с использованием культуры клеток кератиноцитов собак показали, что циклоспорин влияет на IL-8 и вызывает экспрессию мРНК фактора некроза опухолей-а, что, вероятно, может положительно влиять на факторы врожденного иммунитета в коже (Hendricks с соавторами, 2012).
Стафилококковые и Mallassezia-инфекции кожи и ушей
Стафилококковые и Mallassezia-инфекции кожи и ушей часто осложняют течение АД собак. В то время как они могут поддерживать воспаление, считается, что колонизация и инфекция являются следствием измененной барьерной функции кожи и кожного иммунитета, присущих собакам с АД (Nuttall и Halliwell, 2001, Bexley с соавторами, 2013). В одном исследовании при лечении циклоспорином у собак значительно снижалась частота возникновения вторичных инфекций (Steffan с соавторами, 2003). Предполагается, что эффективный контроль АД собак снижает частоту и тяжесть инфекций. Псориаформный лихеноидный дерматоз (см. выше) был связан со стафилококками и, возможно, с необычной реакцией на бактериальную колонизацию и/или инфекцию у некоторых собак на фоне терапии циклоспорином (Werner, 2003, Favrot с соавторами, 2005). Эти поражения, как правило, разрешались при отмене циклоспорина, но некоторые собаки могут также нуждаться в лечении антибиотиками.
Инфекции мочевыводящих путей
Имеются сообщения о бактериурии и инфекциях нижних мочевыводящих путей, выявленные у 1,3% из 759 собак. По данным другого клинического исследования, бактерии присутствуют хотя бы в одном образце мочи у 51% из 89 собак, получавших циклоспорин (Steffan с соавторами, 2005). При этом только у одной собаки наблюдались клинические признаки цистита, еще у девяти собак подозревались бессимптомные инфекции мочевых путей (Steffan с соавторами, 2006). Однако у 24% собак в этом исследовании бактериурия была обнаружена еще перед началом лечения и оставалась стабильной на протяжении всего наблюдения, с некоторыми колебаниями с положительного на отрицательный, и наоборот. Вполне возможно, что высокая распространенность бактериурии является следствием предшествующего курса лечения системными глюкокортикоидами и не связана с циклоспорином. Еще одно исследование, проведенное на 38 собаках, показало, что на протяжении двух лет лечения лишь у трех собак развилась бактериурия, что было подтверждено выделением культуры (Radowicz и Power, 2005). Еще в 18 пробах мочи результаты бактериологических исследований были отрицательными, при микроскопии осадка мочи признаков инфекций не выявлено, при этом клинические признаки воспаления мочевыводящих путей отсутствовали у всех собак. По данным одного ретроспективного исследования, у 26 из 87 собак с хроническими воспалительными заболеваниями кожи, получавших циклоспорин с глюкокортикоидами и без них не менее пяти месяцев, выявляли, по крайней мере, один положительный посев мочи (Peterson с соавторами, 2012). Однако не было никаких существенных различий между контрольной группой и собаками, получавшими только циклоспорин или комбинацию циклоспорина и глюкокортикоидов. Клинических признаков инфекции мочевых путей не было отмечено ни у одной из собак. Посев мочи был более чувствителен, чем микроскопия осадка, поэтому, возможно, более ранние исследования недооценили распространенность бактериурии. Тем не менее, трудно дифференцировать ПЭ глюкокортикоидов и циклоспорина в этом исследовании.
Другие инфекции
Другие бактериальные инфекции (в том числе гингивит, пиометра и инфекции дыхательных путей) были зарегистрированы у собак, получавших циклоспорин, но не чаще, чем в общей популяции собак (Steffan с соавторами, 2006). Энтерит, вызванный клостридиями, был диагностирован у одной из 266 собак (Steffan с соавторами, 2005), а еще у одной собаки развилась неспецифическая диарея, отвечающая на метронидазол. Нокардиоз был подтвержден у одной собаки с АД, получавшей циклоспорин и кетоконазол (Paul с соавторами, 2010). Другие инфекции были редки. Одна собака после трансплантации почки, получавшая циклоспорин в высокой дозе, заболела токсоплазмозом, однако она получала дополнительно преднизолон и азатиоприн для предотвращения отторжения трансплантата (Bernsteen с соавторами, 1999). Возможно, этот случай был связан с серопозитивным донором или реактивацией цист Toxoplasma в почечном аллотранс-плантате. Зарегистрирован один случай рецидива лейш-маниоза у четырехлетней чау-чау, получавшей 5 мг/кг циклоспорина ежедневно в связи с АД, за год до этого успешно прошедшей курс лечения меглумина антимонатом с аллопуринолом. При отмене циклоспорина и возобновлении лечения меглумина антимонатом и аллопуринолом у собаки наблюдалась ремиссия лейшманиоза (Navarro с соавторами, 2008). Другое исследование показало, что лечение собаки с лейшманиозом циклоспорином в дозе 3,5 мг/ кг и глюкантимом в течение шести дней хорошо переносилось без признаков клинического рецидива (Pugliese с соавторами, 1997). Случаи вирусной, грибковой и вызванной Neospora инфекций также отмечены у собак, получавших циклоспорин вместе с преднизолоном или метилпреднизолоном, азатиоприном или хлорамбуцилом при иммунноопосредованных болезнях. Несколько случаев множественных папиллом и плоскоклеточного рака in situ, ассоциированных с вирусом папилломатоза собак, было зарегистрировано у собак на фоне длительного лечения преднизолоном и циклоспорином (Callan с соавторами, 2005). В другом исследовании одновременная терапия циклоспорином (5 мг/кг каждые 24 часа) и преднизолоном (1 мг/кг каждые 24 часа в течение семи дней и затем 1 мг/кг каждые 48 часов в последующие 14 дней) незначительно увеличивала частоту неблагоприятных эффектов, по сравнению с использованием только циклоспорина. ПЭ были ограничены теми, которые ожидаются от циклоспорина (т.е. желудочно-кишечные расстройства от легкой до умеренной степени) и преднизолона (т.е. повышение аппетита, полиурия/полидипсия и других системные эффекты); при этом не было ни одного достаточно серьезного их проявления, что могло бы потребовать прекращения терапии. Никаких инфекций также не было отмечено (Dip с соавторами, 2013).
Выводы и рекомендации
По всей вероятности, эффективный контроль АД собак снижает риск развития секондарных инфекций кожи и ушей, вызванных стафилококками и Malassezia. Следовательно, присутствие этих инфекций не является противопоказанием к использованию циклоспорина. Тем не менее, должна быть использована местная или системная противомикробная терапия (Весо с соавторами, 2013).
Случаи других оппортунистических инфекций редки. Проведение клинического анализа мочи собакам, получающим циклоспорин в дозе 5 мг/кг в течение длительного периода, желательно, но не является обязательным, однако это предположение требует дальнейших исследований. Для снижения риска восходящих инфекций мочевыводящей системы (например, распространения инфекции от бактериального цистита до пиелонефрита, требующего пожизненного лечения) у иммуносупрессивных собак, потенциально возможно (хотя и нечасто), что периодически бактериологическое исследование может быть уместно. Также серологическое исследование на лейшманиоз может быть рекомендовано для собак, проживающих в эндемических областях. Сопутствующее использование преднизолона в первые три недели лечения циклоспорином не противопоказано. Тем не менее, использование высоких доз циклоспорина в течение продолжительного времени, особенно совместно с другими иммуномодуляторами и иммуносупрессивными препаратами, должно проводиться с осторожностью!
Материал опубликован: http://veterinaryrecord.bmj.com/ Veterinary Record 2014;174:3-12 doi:10.1136/vr.l02471
Продолжение в следующем номере.


Назад в раздел

















