Дерматомикоз у голубей, вызванный плесневым грибом Penicillium polonicum

Еще фото
Автор (ы): Р.С. Овчинников, М.Г. Маноян, А.Г. Гайнуллина
Организация(и): Федеральное государственное бюджетное учреждение «Всероссийский государственный Центр качества и стандартизации лекарственных средств для животных и кормов» (ФГБУ «ВГНКИ»)
Журнал: №6 - 2012
Введение
Грибковые болезни у птиц протекают, как правило, в глубокой форме (респираторной или системной), в то время как поверхностные микозы (дерматомикозы) встречаются относительно редко. Возбудителями глубоких микозов птиц являются грибы родов Aspergillus, Candida, Histoplasma, Cryptococcus, Mucor, Rhizopus, Absidia и ряд других [1]. Практически все виды грибов, вызывающие микозы птиц, являются оппортунистическими патогенами, и для возникновения заболевания необходимым условием является снижение резистентности макроорганизма [2].
Среди поверхностных микозов птиц наиболее известен фавус (парша) – дерматомикоз, вызываемый Microsporum gallinae и другими видами дерматофитов. Однако в последние годы эти возбудители встречаются довольно редко, в то время как клиническая значимость недерматофитных плесневых и дрожжевых грибов возрастает. Так, в качестве возбудителей дерматомикозов птиц описаны дрожжевые грибы родов Candida [3-5], Rhodotorula [6,7], Trichosporon [8], Cryptococcus, а также липофильных дрожжей рода Malassezia [9].
«Плесневые» грибы, способные вызывать кожные поражения птиц, представлены в основном видами рода Aspergillus: Aspergillus spp. [10], А. glaucus, A. niger [11], A. fumigatus [12, 13], A. flavus [4].
Клинически дерматомикозы у птиц часто ассоциированы с образованием алопеций, выпадением перьев [6, 14, 15, 7, 12]. Также они могут проявляться в форме эпидермальных цист на гребешках, узелковых опухолей, депигментации перьев [13, 16]. Известны также микогенные поражения глаз у птиц [17].
Наиболее полно в литературе описаны дерматомикозы продуктивных видов птиц – кур, индеек и т.д. Лишь единичные публикации посвящены видам, не имеющим значение для промышленного птицеводства, например туканам (Aho et al.) [18], попугаям (Bengoa et al.) [19]. Этиология микозов комнатных декоративных птиц изучалась M. Mayahi et al. [20]. Микозы диагностированы у 0,4% птиц с кожными поражениями (попугаи, канарейки), выделены виды C. albicans, A. fumigatus.
Что касается голубей, то имеющиеся в литературе сведения о грибковых болезнях у крайне скудны. В данной статье мы описываем вспышку дерматомикоза среди высоколетных голубей из одной голубятни, сопровождавшегося массированным выпадением перьев и обусловленного плесневым грибом Penicillium polonicum.
Клинический случай
Два взрослых голубя, иранской высоколётной породы, были представлены для лабораторного микологического исследования в лабораторию ветеринарной микологии ФГБУ «ВГНКИ» в ноябре 2011 года. Первые клинические симптомы отмечены владельцем за 3 недели до обращения. Лечение не проводилось.
При клиническом осмотре у обеих птиц обнаружены кожные поражения – массированное выпадение перьев в области шеи и головы у одной птицы и в области спины – у другой. Перья на периферии поражений частично обломаны, легко выдергиваются. Кожа с признаками гиперкератоза и лихенизации, что свидетельствует о хроническом воспалительном процессе (см. рис. 1). Общее физическое состояние голубей было удовлетворительным.
Птицы содержатся в городской голубятне, численность стаи 17 пар (34 птицы). Со слов владельца, это не первый случай подобного заболевания в его голубятне. Обычно поражения наблюдаются в теплое влажное время года (в данном случае, осенью), заболевает около 30% поголовья. Течение хроническое, обычно после линьки наступает самовыздоровление. Общее клиническое состояние заболевших птиц (аппетит, тонус, подвижность) в пределах нормы. Птицы обеспечены полноценным питанием и уходом, изменений в рационе за последнее время не было.
Для микологического исследования были отобраны перья с периферии очагов поражений. Для анализа использовали только корневые участки перьев, которые перед посевом на питательные среды обрабатывали 70º этанолом для исключения поверхностной контаминации. Для прямой микроскопии готовили препараты в 10% растворе КОН. Посев материала проводили на сусло-агар и сусло-агар с селективными добавками Chloramphenicol и DermatoSupplement (HiMedia Laboratories, Индия). Посевы инкубировали при 28ºС в течение 21 суток Для изучения морфологических свойств выделенные культуры грибов пересевали уколом на агар Чапека. Чувствительность изолятов к антифунгальным препаратам проводили диско-диффузионным методом, включая нистатин, клотримазол, флуконазол, кетоконазол, итраконазол (производства HiMedia Laboratories, Индия). Для бактериологического исследования были взяты мазки с кожи пораженных участков и посеяны на дифференциально-диагностические питательные среды.
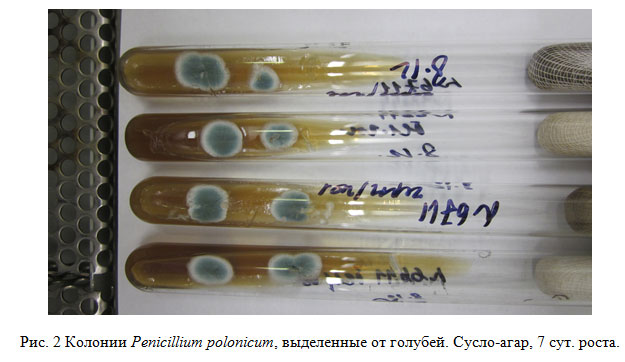
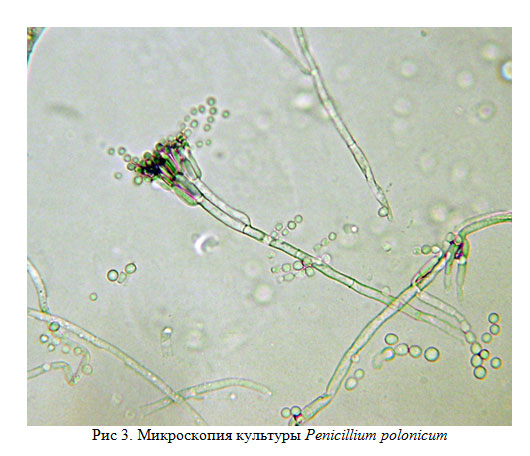
При прямой микроскопии пораженных перьев были обнаружены ветвящиеся светло-зеленые грибные гифы. На 7-е сутки на сусло-агаре наблюдали рост однотипных грибных колоний во всех посеянных образцах материала. Колонии округлые, плоские, бархатистые, зеленые с белым краем, диаметр 1-2 см (см. рис. 2). На среде Чапека наблюдали красноватую окраску реверса колоний. При микроскопии культуры обнаружены светло-зеленые грибные гифы, ветвящиеся конидиеносцы, заканчивающиеся фиалидами, несущими цепочки микроконидий (см. рис. 3).
Выделенные культуры были идентифицированы как Penicillium polonicum (в соответствии с руководством Frisvad et al.) [21]. Морфологически идентичные колонии были получены также на сусло-агаре с хлорамфениколом. На сусло-агаре с добавкой DermatoSupplement рост грибов не обнаружен. Гриб был чувствителен к клотримазолу, кетоконазолу, итраконазолу и устойчив к нистатину и флуконазолу. При бактериологическом исследовании был выявлен скудный рост Staphylococcus epidermidis (представитель кожной нормофлоры).На основании выделения гриба в чистой культуре и обнаружения в пораженных перьях морфологически тождественных грибных элементов в данном случае был диагностирован микоз, вызванный Penicillium polonicum.
Обсуждение
Грибы рода Penicillium, как свидетельствуют литературные данные, очень редко вызывают микозы птиц. Так, Aho R. et al. (1990) описан респираторный микоз у туканов, вызванный Penicillium griseofulvum. Bengoa A. et al. (1994) приводят описание микоза клюва у попугая ара, обусловленного видом Penicillium cyclopium. Что касается выделенного в данном исследовании вида Penicillium polonicum, то в доступной литературе нам не удалось найти сведений о его этиологической значимости при микозах птиц, а также других животных. Примечательно, что современные данные молекулярных исследований показывают близкое филогенетическое родство P. polonicum и P. cyclopium [22].
Penicillium polonicum известен как убиквитарный сапротрофный вид, средой обитания которого являются почва, растительные субстраты. Он часто контаминирует продукты питания и корма для животных, может являться причиной микотоксикозов [23]. Можно предположить, что в качестве резервуара гриба в данном случае служили подстилка в голубятне или корм для птиц.
Следует отметить массовость заболевания и сезонный характер – пик заболеваемости голубей, как отметил владелец, приходился на влажные теплые периоды (весной и осенью). Такие условия благоприятны для активного роста и размножения плесневых грибов, увеличению их популяции во внешней среде, что вероятно способствовало инфицированию птиц. Вместе с тем, очевидно, что развитию дерматомикоза способствовали еще какие-либо предрасполагающие факторы, вызвавшие снижение резистентности организма голубей.
Насколько нам известно, это первое описание плесневого гриба Penicillium polonicum в качестве этиологического агента дерматомикозов у птиц. Данный клинический случай является еще одним свидетельством расширения видового состава возбудителей микозов животных, ростом клинической значимости грибов-оппортунистов. Учитывая трудности диагностики грибковых заболеваний нельзя исключать, что роль грибов в этиологии кожных болезней часто остаётся не выявленной.
Литература
1. Conkova E., Cellarova E., Sutiak V., Neuschl J. Avian mycotic infections - prophylaxis and treatment. Veterinarstvi 2002; 52(3):114-116
2. Reavill D.R. Fungal and Bacterial Diseases. In: Rosskopf W., Woerpel R. (eds). Diseases of cage and aviary birds. Williams & Wilkins, Philadelphia, 1996
3. Kuttin, E.S., Beemer, A.M. and Meroz, M. Case Report - Chicken dermatitis and loss of feathers from Candida albicans. Avian Diseases 1976; 20: 216-218
4. Mohammed M., Sokkar S., Batrawi A. Natural and experimental nodular dermatomycosis in chickens. Avian Pathology 1980; 9:185-192
5. Osorio C., Fletcher O., Dykstra M. J., Post K., Barnes H. J. Comb Candidiasis Affecting Roosters in a Broiler Breeder Flock. Avian Diseases 2007; 51(2):618-622
6. Beemer A.M., Schneerson-Porat S., Kuttin E.S. Rhodotorula mucilaginosa dermatitis on feathered parts of chickens: An epizootic on a poultry farm. Avian Diseases1970; 14: 234-239
7. Page R.K., Fletcher O.J., Eidson C.S. and Michaels, G.E. Case Report – Dermatitis produced by Rhodotorula glutins in broiler-age chickens. Avian Diseases 1976; 20: 416-421
8. Gartrell B. D., Rogers L., Maurice R., Alley M.R. Eosinophilic Dermatitis Associated With Trichosporon asahii in a Cockatiel (Nymphicus hollandicus). Journal of Avian Medicine and Surgery 2005; 19(1): 25-29
9. Mycotic Diseases of Pet Birds. The Merk Veterinary Manual. www.merkmanuals.com/vet/index.html
10. Grewal G. S., Brar R. S. Mycotic Dermatitis in Domestic Fowl. A Case report./Pilzdermatitis am Haushuhn. Ein Fallbericht. Mycoses 1987; 30: 440–442
11. Chute H.L. Aspergillosis. In: Diseases of Poultry. Hofstad et al (eds); 7th ed. The Iowa State Univ. Press, Ames, 1978
12. Yamada S., Kamikawa S., Uchinuno Y., Tominaga A., Matsuo K., Fujikawa, Takeuchi K. Avian dermatitis caused by Aspergillus fumigatus. Journal of the Japanese Veterinary Medical Association 1977; 30:200-202
13. Suedmeyer W., Bermudez A., Fales W. Treatment of Epidermal Cysts Associated With Aspergillus fumigatus and Alternaria Species in a Silky Bantam Chicken. Journal of Avian Medicine and Surgery 2002; 16(2):133-137
14. Beneke E.S. Mycotic infections. In: Isolation and Identification of Avian Pathogens. Ed. Hitchner et al (eds); pp.133-141. Arnold Printing Corporation. Ithaca, New York, 1975
15. Kuttin E.S., Beemer A.M., Meroz M. Case Report - Chicken dermatitis and loss of feathers from Candida albicans. Avian Diseases 1976; 20: 216-218
16. Clubb S.L., Herron A. Feather discoloration due to saprophytic fungal growth. Proc Annu Conf Assoc Avian Vet. 1998; 71–75
17. Dalton J. R., Ainsworth H. Mycotic keratoconjunctivitis in 12-day-old red-legged partridges (Alectoris rufa) . Veterinary Record 2011; 168:590
18. Aho R., Westerling B., Ajello L., Padhye A.A., Samson R.A. Avian penicilliosis caused by Penicillium griseofulvum in a captive toucanet. Medical Mycology 1990; 28(5):349-354
19. Bengoa A., Briones V., Lopez M., Paya M. Beak infection by Penicillium cyclopium in a Macaw (Ara ararauna). Avian Desiases 1994; 38:922-7.
20. Mayahi M., Ghorbanpour Najafabadi M., Fatahina M., Shirali S. A survey on the causes of cutaneous mycosis in pet birds in Ahvaz city. Scientific-research Iranian veterinary journal 2009; 4(4 (21)):56-60
21. Frisvad J. C., Samson R. A. Polyphasic taxonomy of Penicillium subgenus Penicillium. A guide to identification of food and air-borne terverticillate Penicillia and their mycotoxins. Stud. Mycol. 2004; 49:1-173.
22. Kim W., Hwang Y., Yu S.H. Two Species of Penicillium Associated with Blue Mold of Yam in Korea. Mycobiology 2008; 36(4):217-221
23. Mantle P. G., McHugh K.M., Fincham J.E. Contrasting Nephropathic Responses to Oral Administration of Extract of Cultured Penicillium polonicum in Rat and Primate. Toxins 2010; 2:2083-2097


Назад в раздел


















