Гиперальдостеронизм кошек: действительно ли болезнь настолько редка, что не заслуживает нашего внимания?
Еще фото
Автор (ы): О.О. Смирнова, к.б.н, ветеринарный врач-терапевт (pacivik@yandex.ru) / O. Smirnova, veterinary internist
Организация(и): Ветеринарная клиника неврологии, травматологии и интенсивной терапии, г. Санкт-Петербург / Veterinary Hospital of Neurology, Traumatology and Intensive Therapy, Saint-Petersburg
Журнал: №6 - 2014
УДК 619:616.4:616.15-07:616.15:636.8
Ключевые слова: гиперальдостеронизм, электролитные нарушения, гипокалиемия, гипертензия
Key words: hyperaldosteronism, electrolyte imbalance, hypopotassemia, hypertension
Аннотация
Гиперальдостеронизм до недавнего времени считался достаточно редкой патологией эндокринной системы. В 1983 г. появились первые сообщения о многочисленных зарегистрированных случаях первичного гиперальдостеронизма, или болезни Конна, давая доказательства того, что эта болезнь может быть более частой, чем ее оценивали в прошлом [18]. В последние годы появляется все большее количество сообщений о выявлении данной болезни у кошек. Это обусловлено и тем, что все больше внимания уделяется диагностике вторичной патологии (вторичного гиперальдостеронизма), и тем, что развивается диагностика первичной патологии. Но до сих пор эту эндокринную болезнь (как первичную, так и вторичную) нельзя назвать широко распространенной. Гиперальдостеронизм – это заболевание, при котором патофизиологические механизмы обусловлены высокой концентрацией циркулирующего в крови альдостерона. В данном случае название болезни говорит само за себя. В ходе изучения этой болезни следует вернуться к азам физиологии и рассмотреть компоненты и механизмы работы РААС. Эти основы крайне важны для правильного понимания патогенеза гиперальдостеронизма, а соответственно, и для понимания правильного диагностического и лечебного подхода к пациенту.
Summary
Until recently hyperaldosteronism was considered as a quite rare endocrine pathology. In 1983 there appeared the first numerous recorded mentions of true hyperaldosteronism or Conn's syndrome , and this justifies the fact that this disease can be more frequent than it was supposed before [18]. In recent years there has been a growing number of observed cases among cats. This fact is determined by increasing attention to diagnosis of secondary pathology (secondary hyperaldosteronism) as well as by developing of diagnosis of primary pathology. Nevertheless this disease (both primary and secondary) still cannot be defined as widely held. Hyperaldosteronism is characterized by high concentration of circulating aldosterone stipulating pathophysiological mechanisms. In this case the name of the disease speaks for itself. In the course of studying this disease it is recommended to return to the basics of physiology and to explore components of the RAAS's working mechanisms. They are crucial for genuine understanding of hyperaldosteronism pathologies and, consequently, for proper understanding of diagnosis and therapeutic approach to a patient.
|
СОКРАЩЕНИЯ | |||
|
CA++ |
кальций |
ФИЗ. РАСТВОР |
физиологический раствор (0,9% раствор хлорида натрия) |
|
K+ |
калий |
ЭКГ |
электрокардиограмма |
|
NA++ |
натрий |
СД |
сахарный диабет |
|
ПУ/ПД |
полиурия, полидипсия |
ЭХОКГ |
эхокардиография |
|
ГК |
глюкоза крови |
РААС |
ренин-ангиотензин-альдостероновая система |
|
ЕД |
единица действия |
ОЦК |
объем циркулирующей крови |
|
ЖКТ |
желудочно-кишечный тракт |
КТ |
компьютерная томография |
|
АПФ |
ангиотензинпревращающий фактор |
МРТ |
магнитнорезонансная томография |
|
ИАПФ |
ингибиторы ангиотензинпревращающего фактора |
МВП |
мочевыводящие пути |
|
НПВС |
нестероидные противовоспалительные средства |
НО |
новообразования |
|
ОКА |
общий клинический анализ крови |
ХБП |
хроническая болезнь почек |
|
Т4О |
общий тироксин |
КПВ |
каудальная полая вена |
Альдостерон и РААС
Альдостерон – это минералокортикоидный стероидный гормон, синтезирующийся в клубочковой зоне коры надпочечников из холестерола через ряд промежуточных метаболитов. На долю альдостерона приходится 95% всех гормонов, вырабатываемых клубочковой зоной коры надпочечников [8].
Важно понимать, что регуляция синтеза альдостерона в коре надпочечников обусловлена двумя ведущими механизма. Первый механизм – это влияние РААС. При этом альдостерон следует рассматривать не как отдельно существующий гормон, а как неотъемлемый компонент этой сложноорганизованной системы. РААС активируется в ответ на снижение объема циркулирующей крови и почечного кровотока. Это приводит к снижению доставки натрия и хлорида к клеткам дистальных канальцев почек и стимулирует секрецию ренина в клетках юкстагломерулярного комплекса. Именно поэтому сниженное кровяное давление, которое воспринимается сначала клетками почек, индуцирует биосинтез и секрецию ренина. Ренин, в свою очередь, расщепляет ангиотензин до ангиотензина I, который затем гидролизуется с образованием ангиотензина II в легких с помощью АПФ и выполняет роль вазоконстриктора. АПФ имеется также в подавляющем большинстве других тканей и в крови. Но наиболее его активность выражена именно в легких. Непосредственно ангиотензин II, образовавшийся в конце этой цепочки, стимулирует секрецию аль-достерона. Образующийся альдостерон поступает в кровь и вызывает экскрецию калия и задержку натрия, чем косвенно способствует накоплению воды и повышению кровяного давления. Такой, казалось бы на первый взгляд, сложный механизм, схематически можно проиллюстрировать достаточно короткой последовательностью реакций (Схема 1).
Таким образом, гиперальдостеронизм в случае вторичной патологии станет последним звеном в цепи реакций РААС.
Кроме снижения кровяного давления в афферентных артериолах на фоне снижения ОЦК и почечного кровотока, пусковыми механизмами для синтеза ренина являются:
• снижение концентрации натрия в плазме крови;
• уменьшение осмотического давления в дистальных извитых канальцах;
• стимуляция симпатических нервных волокон, иннервирующих афферентные артериолы [8].
С тех пор как было показано, что снижение перфузии почек провоцирует секрецию ренина и, как результат, повышение кровяного давления, ренин считается одним из патогенетических факторов гипертензии [4].
Второй, не менее важный механизм регуляции синтеза альдостерона в коре надпочечников – это прямая регуляция через ионы калия, циркулирующие в плазме крови. Увеличение калия в сыворотке крови стимулирует выработку альдостерона корой надпочечников, поскольку этот гормон осуществляет его экскрецию с мочой.
Для чего необходим альдостерон?
Главная физиологическая функция альдостерона – это регуляция гомеостаза натрия и калия в сыворотке крови и поддержание нормального внутрисосудистого объема жидкости. Циркулирующий в крови альдостерон оказывает свое основное физиологическое влияние на почки. Это приводит к реабсорбции натрия, в результате чего задерживается вода, но экскретируются ионы калия и водорода. По мере экскреции калия в моче концентрация калия в плазме снижается. Вследствие этого объемы плазмы и экстраклеточной жидкости увеличиваются совместно с общим периферическим сопротивлением из-за вазоконстрикции, вызванной ангиотензином II, что приводит к повышению кровяного давления. Увеличение объема экстраклеточной жидкости приводит к усилению кровотока в почках, за счет чего снижается секреция ренина.
Как и в первый раз, данная цепочка на первый взгляд может показаться сложным физиологическим механизмом. Поэтому схематическое упрощение реакций может помочь воспринять каскад реакций (Схема 2).
На основании приведенных данных о физиологическом действии альдостерона можно прийти к выводу о том, какие ведущие клинические последствия будут сопровождать повышенные концентрации альдостерона. Избыточное высвобождение альдостерона из клубочковой зоны приведет к различной степени электролитных, жидкостных и метаболических расстройств. Основными клиническими последствиями избыточной продукции альдостерона становятся, таким образом, усиленная задержка натрия и воды, вызывающая системную артериальную гипертензию, и повышенная экскреция калия почками, приводящая к гипокалиемии.
Далее в тексте неоднократно будет идти речь об артериальной гипертензии кошек. В статье использованы категории артериальной гипертензии по классификации IRIS (Табл. 1).
Причины болезни
Гиперальдостеронизм дифференцируется на первичный и вторичный. Первичный гиперальдостеронизм также носит название болезни или синдрома Конна. Он характеризуется автономной повышенной продукцией альдостерона патологически измененной клубочковой зоной при одновременном наличии низкой концентрации ренина в плазме. Для животных, страдающих первичным гиперальдостеронизмом, характерно неадекватное увеличение секреции альдостерона, независимое от РААС и концентрации ионов калия в сыворотке крови. Избыток альдостерона в этом случае приводит к угнетению РААС. Увеличение количества внеклеточной жидкости и плазмы воспринимается рецепторами растяжения юкстагломерулярного аппарата, а задержка натрия в сыворотке крови – так называемым «плотным пятном», что приводит в итоге при первичной патологии к снижению биосинтеза и продукции ренина. Подавление активности рениновой системы служит маркером первичности патологии.
Первичный гиперальдостеронизм ассоциирован с новообразованием/ ями коры надпочечников, продуцирующим альдостерон. Новообразование может быть представлено унилатеральной (что наиболее часто характерно для кошек) или билатеральной аденомой или аденокарциномой. В некоторых случаях к болезни приводит билатеральная гиперплазия клубочковой зоны коры надпочечников. «Унилатеральная адренокортикальная неоплазия является наиболее часто описываемой причиной первичного гиперальдостеронизма у кошек, причем аденомы и карциномы у них возникают с примерно одинаковой частотой» [2].
Гистопатологические результаты исследования коры надпочечников при первичном гиперальдостеронизме у кошек могут соответствовать следующим диагнозам:
• унилатеральные или билатеральные адренокортикальные аденокарциномы;
• унилатеральные или билатеральные аденомы;
• идиопатическая билатеральная нодулярная гиперплазия надпочечников.
При вторичном гиперальдостеронизме клетки коры надпочечников не изменены, но обладают повышенной биосинтетической активностью. Вторичный гиперальдостеронизм встречается относительно чаще, и основной его отличительной особенностью является постоянная активация РААС, которая и становится стимулом коры надпочечников для повышенной продукции альдостерона. Предполагать эту болезнь можно у пациентов с развитием, например, сердечной недостаточности, заболеваниями почек, тяжелой гепатоцеллюлярной дисфункцией, которые сопровождаются генерализованным отеком или активацией юкстагломерулярного аппарата. Также одной из причин патологии способно стать низкое содержание натрия в рационе [1]. Эти группы первичных патологий приводят к гиповолемии, снижению ОЦК, что становится непосредственной причиной для синтеза ренина и активации всех звеньев РААС. Следовательно, вторичный гиперальдостеронизм можно встретить также и при многих других заболеваниях, сопровождающихся дегидратацией, гипотензией, сниженной перфузией почек или дефицитом натрия. И в этом случае повышение уровня циркулирующего альдостерона будет напрямую коррелировать с активностью ренина.
Клинические признаки
Болеют гиперальдостеронизмом обычно кошки среднего-пожилого возраста. Половая и породная предрасположенность к болезни при этом не отмечена. Как упоминалось выше, основными клиническими последствиями избыточной продукции альдостерона становятся усиленная задержка натрия и воды, вызывающая системную артериальную гипертензию, и повышенная экскреция калия почками, приводящая к гипокалиемии. Гиперальдостеронизм, как первичный, так и вторичный, является достаточно ярким примером болезни-причины клинически значимой гипокалиемии умеренно-тяжелого характера, развивающейся по причине потери ионов калия с мочой. Гипокалиемия сопровождается не только снижением концентрации циркулирующих ионов калия, но и приводит также к снижению запасов калия с потерей общего калия организма. Перемещение ионов калия из внутриклеточного пространства во внеклеточную жидкость, в свою очередь, приводит к внутриклеточному движению водородных ионов, повышенной экскреции ионов водорода и развитию метаболического алкалоза. Тяжелый метаболический алкалоз, в свою очередь, способен привести к гипокальциемии и, как следствие, к депрессии сердечно-сосудистой системы, вялости, тетании и судорогам. Неспецифические симптомы, связанные с метаболическим алкалозом, представлены слабостью и дегидратацией.
Физиологический эффект гипокалиемии – это гиперполяризация мембранного потенциала отдыхающей клетки. При гипокалиемии повышается клеточный мембранный потенциал покоя, приводя к увеличенной разнице между потенциалом покоя и пороговым потенциалом, необходимым для потенциала действия и мышечного сокращения. Это вызывает неспособность мышц нормально сокращаться, следовательно, ведущим клиническим признаком является так называемая миопатия, выражающаяся в слабости гладкой и поперечно-полосатой мускулатуры. Проявляться слабость поперечно-полосатой мускулатуры будет эпизодическими или постоянными симптомами, в том числе цервикальной вентрофлексией (Рис. 1), «стопохождением», слабостью тазовых конечностей. Владельцы нередко интерпретируют последнюю проблему как нарушение поведения, так как видят неспособность или нежелание кошки запрыгнуть на те поверхности, которые ранее были для нее легко доступными. Сильная гипокалиемия (<1.5 ммоль/л) может привести к слабости дыхательной мускулатуры и неадекватной вентиляции легких или даже остановке дыхания. В наиболее тяжелых случаях возможны ишемия и последующий некроз поврежденных мышц.
Слабость гладкой мускулатуры характеризуется другими проявлениями: илеусом, задержкой мочи вследствие нарушения тонуса мочевого пузыря, неспособностью концентрировать мочу. Неспецифическим симптомом гипокалиемии являются общие вялость и угнетение. Гораздо реже можно отметить дисфагию, коллапс. В некоторых клинических случаях мышечные симптомы являются малозаметными и эпизодическими, тогда как в других ситуациях они приобретают характер быстро прогрессирующих и тяжелых, иногда даже при первом проявлении.
Кроме нарушения работы мышечной ткани, при развитии гипокалиемии могут быть также отмечены симптомы поражения следующих систем органов и метаболических этапов:
• влияние на сердце регистрируется не часто, для этой патологии иногда характерны нарушения проводимости: суправентрикулярные и желудочковые аритмии, удлинение интервала Q-T и появление зубцов U;
• влияние на почки: умеренная гипокалиемия приводит к снижению восприимчивости канальцев почек к антидиуретическому гормону (вазовпрессину), повышению аммони-огенеза.
Давление крови у больных кошек может варьировать у пациентов от нормального до очень высокого. Симптомы артериальной гипертензии менее специфичны и их сложнее интерпретировать у наших пациентов, нежели в гуманной медицине. Относительно часто встречается субклиническая гипертензия. Также нередко последствия артериальной гипертензии выражаются в офтальмологических патологиях, которые владельцы кошек способны отметить невооруженным взглядом.
В этом случае заметными для владельцев могут стать:
• снижение зрения (но при этом стоит учитывать, что владелец, как правило, не в состоянии заметить незначительные нарушения зрения у кошки);
• внезапная слепота, развивающаяся в результате внутриглазных кровотечений или отслоения сетчатки;
• кровоизлияния, видимые невооруженным глазом (Рис. 3);
• мидриаз;
• изменение цвета рефлекса глазного дна.
Гораздо реже, но тем не менее владельцы больных гиперальдостеронизмом кошек могут отметить полиурию, полидипсию, снижение массы тела, полифагию. Данные симптомы являются неспецифичными и нередко регистрируются и при многих других болезнях старых кошек.
Поскольку у старых кошек возможен комплекс сразу нескольких заболеваний, нам могут потребоваться знания о распространенности основных симптомов, специфичных для наиболее часто встречаемых эндокринных патологий. В статье не рассматриваются подробно такие болезни, как СД и гипертиреоз. Но, поскольку эти болезни относятся к разряду более распространенных, чем гиперальдостеронизм, автор статьи привела данные патологии для сравнения основных специфических и неспецифических клинических признаков (Табл. 2).
Как правильно провести дифференциальную диагностику?
Иногда в клинической практике встречаются такие случаи, при которых единственным заметным для владельцев симптомом становится офтальмологическая патология. В подобных ситуациях грамотная диагностика не должна ограничиваться только лишь офтальмологическим исследованием.
Офтальмолог может исключить следующие патологии, характерные для артериальной гипертензии:
• отслоение сетчатки;
• субретинальные, интраретинальные и интравитреальные кровотечения, связанные с системной гипертензией;
• отек диска зрительного нерва;
• различные дегенерации сетчатки;
• чрезмерную извитость сосудов сетчатки;
• атрофию сетчатки, диска зрительного нерва в тяжелых случаях. Для клинициста офтальмологические признаки артериальной гипертензии должны обозначать в первую очередь необходимость поиска первопричины.
Заподозрить гиперальдостеронизм следует у любой кошки, у которой диагностируется гипокалиемия и/или артериальная гипертензия. НО: ни в коем случае при этом нельзя забывать, что далеко не у каждой кошки будет обязательным набор всех симптомов из сипмтомокомплекса гипертензия+гипокалиемия. Не обнаружение электролитных расстройств, ровно как и отсутствие последствий артериальной гипертензии, не должно отталкивать нас от дифференциации диагноза.
Пренебрежение физикальными данными также способно навести на ложный диагностический путь или «замаскировать» неочевидный диагноз гиперальдостеронизм.
Так, в достаточно редких случаях, когда размеры надпочечников при неоплазии значимо увеличиваются, большую помощь в выявлении данной патологии нам может оказать тщательная пальпация брюшной полости.
Сердечный шум и нерегулярный сердечный ритм, являющиеся последствием гипертрофической кардиомиопатии на фоне артериальной гипертензии, можно объяснить рядом других патологий, характерных для пожилых кошек. Гипокалиемию также можно принять за последствие, например, ХБП или гипертиреоза. Поэтому крайне важно не забывать о том, что не исключено сочетание в организме одной кошки сразу нескольких патологий. Особенно учитывая тот факт, что кошка с гипе-ральдостеронизмом – это все-таки часто пожилая кошка. В противовес сказанному, гипердиагностика также способна навести нас на ложный путь и предоставить почву для ненужных рассуждений. В связи с этим, крайне важной задачей клинициста становится поиск некой «золотой середины» при обследовании пожилой кошки без специфических симптомов.
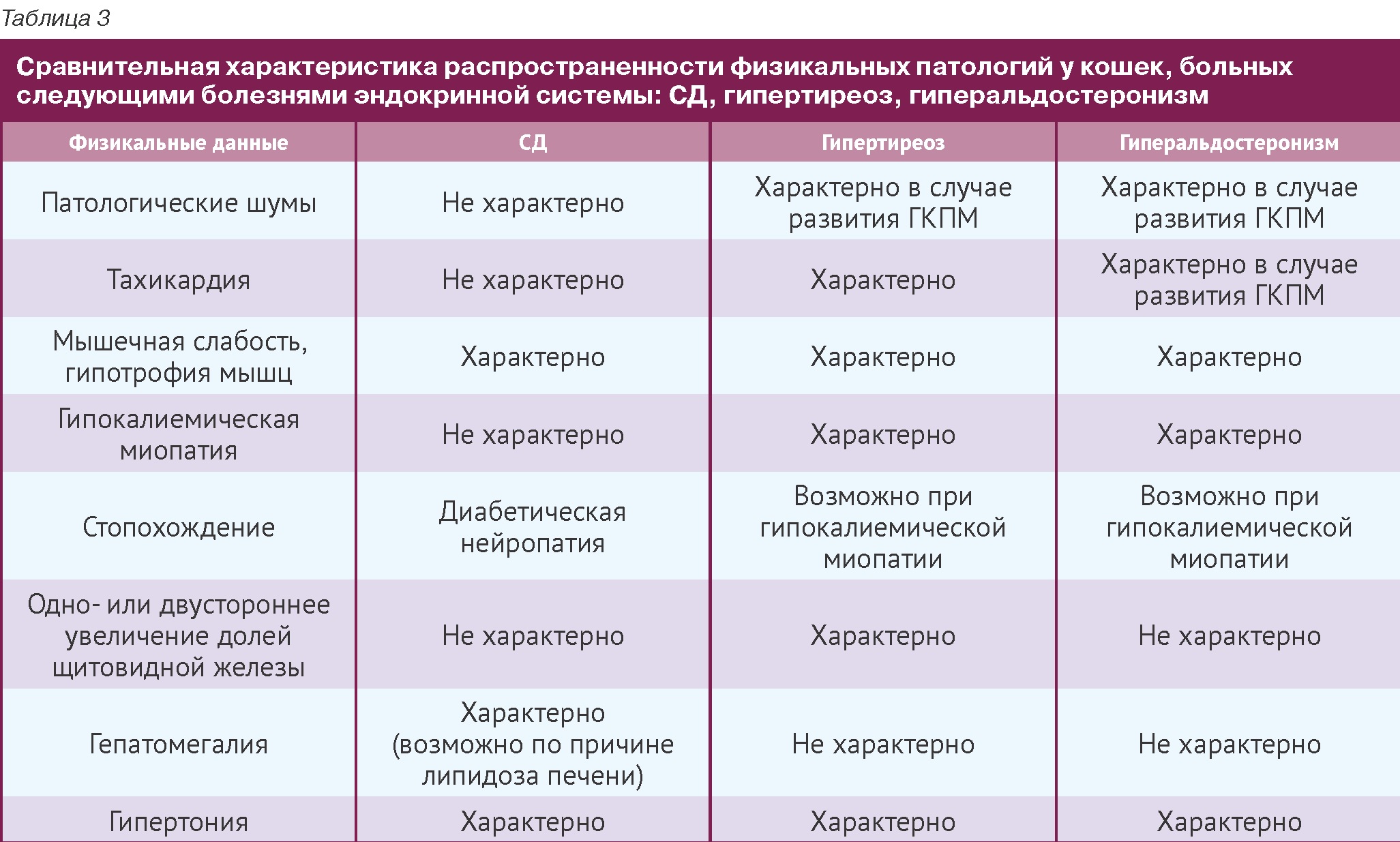
Как было указано выше, в данной статье не рассматриваются подробно такие болезни, как СД и гипертиреоз. Но поскольку эти эндокринные патологии более распространены, чем гиперальдостеронизм, автор статьи привела сравнительные данные по физикальным находкам при этих болезнях, помогающие провести дифференциацию в ходе проведении тщательного осмотра пациента (Табл. 3).
Все методы лабораторной диагностики, которые мы рассмотрим в статье, преследуют цель помочь клиницисту подтвердить или опровергнуть свои предположения в отношении возможности гиперальдостеронизма, а также провести дифференциальную диагностику (особенно это актуально в случае наличия сочетанных патологий или сопутствующих заболеваний).
Типичными биохимическими аномалиями у кошек с гиперальдостеронизмом являются умеренная или тяжелая гипокалиемия и нормальные или слегка повышенные концентрации натрия. При этом всегда следует правильно интерпретировать концентрации ионов калия, способные привести к симптомам гипокалиемии. Биохимическая гипокалиемия не всегда тождественна клинически значимой. Так, концентрация калия в сыворотке крови < 3,5 мг-экв/л соответствует биохимической гипокалиемии. При этом симптомы гипокалиемической миопатии у кошек проявятся при концентрации ионов калия в сыворотке крови < 3.0 мг-экв/л.
Немаловажно, что под воздействием альдостерона усиливается экскреция калия при одновременной активации при этом перемещения калия из внутриклеточного пула во внеклеточную жидкость. Это становится компенсаторным механизмом для поддержания нормокалиемии. Данный механизм способен маскировать потери ионов калия. Но при этом усиливается и внутриклеточный транспорт и потеря почками ионов водорода, что, в свою очередь, способствует метаболическому алкалозу. Прогрессия гипокалиемии приводит к прогрессии жажды и алкалоза.
Также осторожно следует интерпретировать результаты определения концентрации ионов натрия в сыворотке крови. Вторично по отношению к задержке натрия реаб-сорбируется вода. Следовательно, повышенные концентрации натрия «разбавляются», и уровень этого электролита редко бывает повышен. Иногда повышается общее содержание натрия в организме при нахождении концентрации ионов натрия в референтом диапазоне на верхней его границе.
Эти данные делают необходимой крайне осторожную и тщательную интерпретацию концентрации электролитов в сыворотке крови. Ни в коем случае при получении цифр, находящихся в референтных диапазонах, такая информация не должна стать поводом для окончательного исключения диагноза. К сожалению, восприятие гипокалиемии и гипернатриемии как обязательных последствий гиперальдостеронизма кошек является одной из причин ошибок диагностики.
При наличии такого симптома, как гипокалиемическая миопатия, концентрации креатинкиназы в сыворотке также обычно заметно повышены у кошек. Могут также иметься признаки болезни почек, к которым относятся гипостенурия, протеинурия и повышенные концентрации креатинина и мочевины в сыворотке крови. У кошек, которые первоначально не имели данных за ХБП, она может прогрессировать в связи с тем, что гиперальдостеронизм является важным медиатором прогрессирующей болезни почек [2].
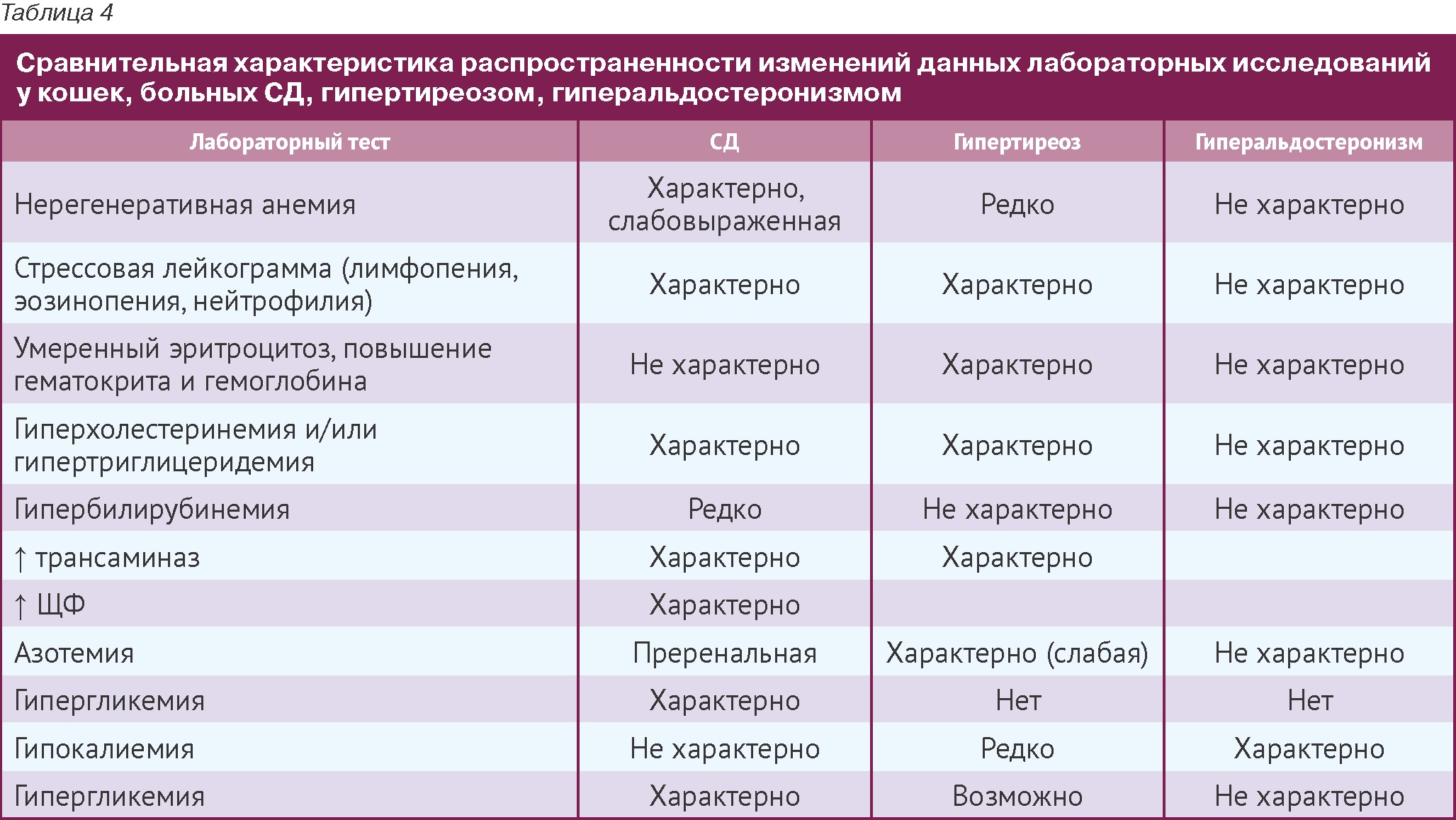
По аналогии с предыдущими таблицами, ниже в Таблице 4 приведены основные лабораторные данные, помогающие при дифференциальной диагностике.
Альдостерон – не видоспецифичный гормон. Референтный диапазон у кошек составляет 194-388 нг/дл [10]. На практике его исследование может проводиться в адаптированных медицинских лабораториях, поскольку в ветеринарных лабораториях проведение данного теста не распространено. Для исследования пригодна гепаринизированная плазма или сыворотка с ЭДТА. Плазма крови стабильна до 7 суток при температуре 2-8°C [15]. У здоровых кошек и у кошек с вторичным гиперальдостеронизмом могут быть значительные суточные колебания концентрации альдостерона в сыворотке крови. Но обычно его содержание увеличивается и при первичном, и при вторичном заболевании. В случае сочетания гипокалиемии и высокой концентрации альдостерона с достаточно высокой долей вероятности можно подозревать у кошки гиперальдостеронизм, но этих данных не может быть достаточно для определения характера патологии. Максимально высокие концентрации альдостерона характерны для кошек с первичным гиперальдостеронизмом [2]. В одном из исследований концентрация альдостерона в плазме у 10 кошек с первичной патологией варьировала от 1253 до 3329 нг/дл [10].
При вторичном гиперальдостеронизме, поскольку патология обусловлена чрезмерной стимуляцией РААС, увеличивается концентрация не только альдостерона, но и ренина. Таким образом, при обнаружении сочетания повышенного содержания альдостерона и ренина, следует подозревать возможность вторичного гиперальдостеронизма. При этом необходимо отбирать достаточно большой объем крови и немедленно замораживать отделенную плазму. Следует избегать применения гепарина, но можно использовать пробирки с ЭДТА. Эти особенности не позволяют использовать данный тест широко в ветеринарной медицине. Как и в случае с исследованием уровня аль-достерона, в ветеринарных лабораториях проведение данного теста не распространено. На активность ренина также могут влиять различные лекарственные препараты, которые получает пациент (например, ингибиторы АПФ, бета-блокаторы), а также потребление соли с пищей. По данным Jepson R.E., Syme H.M., Elliott J., референтные диапазоны активности ренина плазмы составили от 0,5 до 1,52 нг/мл/час [12].
К сожалению, на сегодняшний день мы очень далеки от идеальных лабораторных возможностей. Но, тем не менее, как клиницисты, мы должны понимать, что невозможность определения ренина не должна приводить к безысходности в диагностике, так как нет ни одного универсального и идеального лабораторного теста, способного заменить суждение врача и объективные данные на наличие патологии.
Также следует упомянуть об изменении концентрации других гормонов в сыворотке крови пациентов с гиперальдостеронизмом. По мере усиления синтеза минералокорти-коидов происходит активирование всего пути биосинтеза стероидов. В результате можно отметить повышение концентрации в сыворотке крови пациентов с гиперальдостеронизмом не только альдостерона, но и стероидов-предшественников: например, дезоксикортикостерона, кортикостерона, 18-гидроксикорти-костерона. На сегодняшний день эти данные представляют более научный, нежели практический интерес. Безусловно, если у кошки есть новообразование надпочечника/ов смешанного характера, одновременно секретирующее, например, альдостерон и прогестерон, то при проведении лабораторного исследования уровня циркулирующих гормонов мы можем столкнуться также и с превышением референтных диапазонов прогестерона.
Методы визуализации, которые мы можем использовать в ходе проведения дифференциальной диагностики, также способны дать немало подсказок клиницисту как в случае заболевания первичным, так и в случае заболевания вторичным гиперальдостеронизмом.
Визуальная диагностика особенно важна при подозрении на первичный гиперальдостеронизм, так как только она способна дать более точную информацию, поражен один надпочечник или оба. Этот вопрос особенно важен в связи с тем, что унилатеральный первичный гиперальдостеронизм потенциально можно излечить хирургически, тогда как билатеральное или подтвержденное метастатическое заболевание следует лечить медикаментозно.
При обнаружении новообразования надпочечника/ов визуальные методы должны быть использованы также для выявления отдаленных и регионарных неопластических поражений других органов и тканей. «Опухоли надпочечников редко видны при использовании рентгенографии, и если опухоль видна, то она наиболее вероятно является адрено-кортикальной карциномой» [2]. При рентгенографическом исследовании грудной полости следует обратить внимание на наличие новообразований, при проведении УЗИ, КТ, МРТ брюшной полости также – на возможность инвазии опухоли правого надпочечника в КПВ и окружающие структуры.
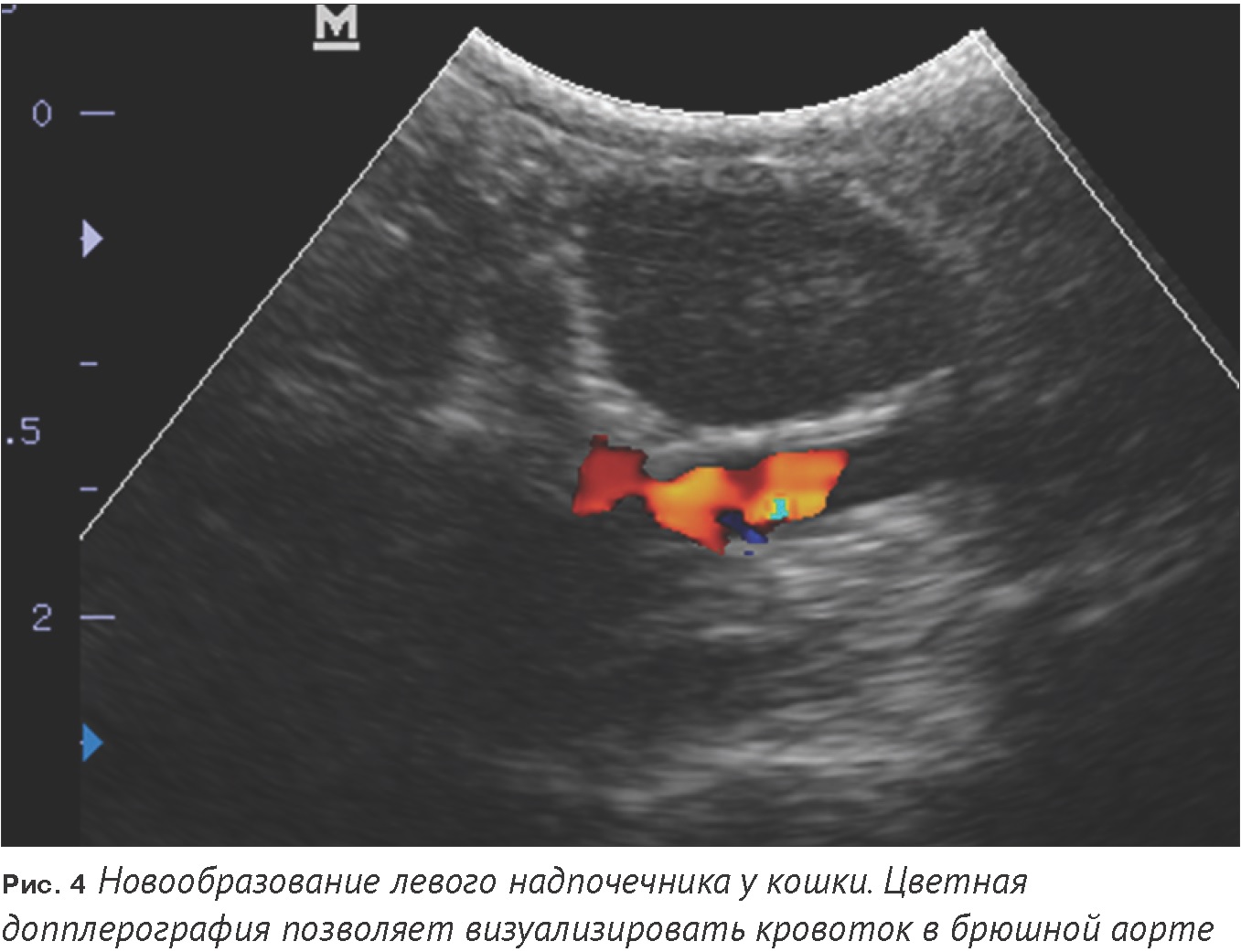
По данным BSAVA [1], поперечный размер надпочечников у кошек составляет 2,8-5,5 мм. Медианный дорсовентральный размер левого надпочечника составляет от 3 до 5,3 мм; правого надпочечника – от 2,9 до 4,5 мм [2]. По данным Penninck D., cTAndre M., продольный размер надпочечников кошек составляет 10-11 мм, максимальный диаметр - 4,3 +/- 0,3 мм [19]. Референтные диапазоны применимы ко всем кошкам, независимо от их размера или возраста. Самыми частыми находками при первичном гипераль-достеронизме у кошек становятся: новообразования надпочечников, кальцификация надпочечников и изменения их эхогенности (Рис. 4). В случае одностороннего поражения надпочечника контралатеральный надпочечник может быть или нормальным, или гипотрофированным. В случае уменьшения размеров такой надпочечник не всегда обнаруживается при проведении УЗИ. При этом крайне важно понимать, что обнаружение измененного надпочечника не является дефинитивным параметром для постановки окончательного диагноза «первичный гиперальдо-стеронизм». Дифференциальными диагнозами, способными привести к исходным изменениям, являются нефункциональные новообразования надпочечников, феохромоцитомы, кортизол-секретирующие и прогестерон-секретирующие опухоли. Наряду с этим, при использовании доступных методов визуализации (КТ, МРТ, УЗИ) надпочечники могут выглядеть абсолютно нормально и их размеры могут соответствовать референтным диапазонам даже при наличии функциональных новообразований и/или клинически значимой гиперплазии.
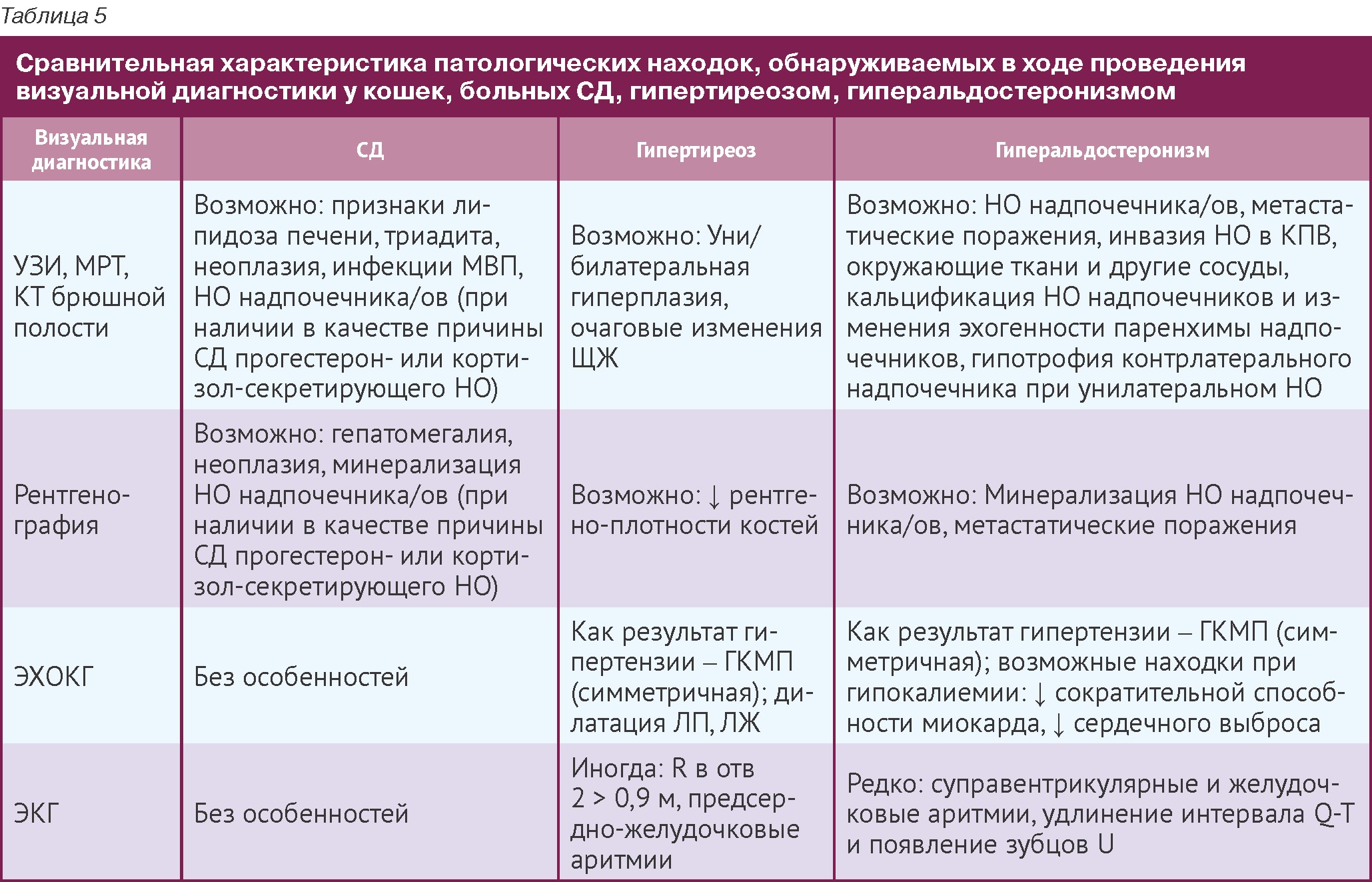
Возможные находки, которые характерны для гиперальдостеронизма и могут быть обнаружены врачом визуальной диагностики, приведены в Таблице 5. Сравнение с данными, обнаруживаемыми при заболевании кошек СД и гипертиреозом, может помочь провести дифференциальную диагностику.
Дифференциальные диагнозы
Безусловно, гиперальдостеронизм – не единственное заболевание, которое можно заподозрить у кошки при наличии сочетания гипокалиемии и артериальной гипер-тензии. При наличии гипокалиемии следует учитывать следующий список болезней, способных привести к данной патологии:
• ХБП;
• СД при начале инсулинотерапии;
• Быстро растущие новообразования;
• Алиментарные патологии;
• Гипертиреоз.
Среди указанных патологий к артериальной гипертензии нередко приводят ХБП, СД, гипертиреоз. Таким образом, порой перед нами может возникнуть сложная задача: определить, какая из болезней стала истинной причиной для того или иного симптома (особенно это касается клинических случаев, сопровождающихся неспецифическими симптомами).
В статье «Изменения концентрации калия: что опаснее?» (Vetpharma, 2014, №4) был предложен и обсужден общий диагностический план, если наш пациент – взрослая кошка старше 8-летнего возраста. Там же был приведен перечень патологий, способных (помимо гипокалиемии) привести к мышечной слабости. Стоит уточнить, что в протокол исследования пациента с подозрением на гиперальдостеронизм или при наличии сомнительных симптомов, наводящих на подозрение о возможности артериальной гипертензии, обязательно должно быть включено измерение артериального давления.
Осложнения и последствия
Осложнения и последствия, связанные с гиперальдостеронизмом, обусловлены в первую очередь артериальной гипертензией. К ним можно отнести следующие патологии:
• ГКМП. Заподозрить данную патологию можно, услышав патологические шумы при аускультации, обнаружив признаки кардиомегалии при проведении рентгенографии грудной клетки (но данные находки совсем не являются обязательными для кошек с ГКМП).
Подтверждается патология только путем проведения ЭХОКГ и носит обычно симметричный характер. Изменения сердца соответствуют повреждению, вызванному гипертензией, вторичной по отношению к увеличенному внутрисосудистому объему.
• ХБП. Альдостерон способен участвовать в развитии и прогрессии повреждения почек, способствуя тромбозу сосудов и фиброзу. Кроме того, как альдостерон, так и ангиотензин II способствуют поддержанию гипертензии и дальнейшей фибропролиферативной деструкции почек [2].
Лечение
Контроль гипокалиемии: в статье «Изменения концентрации калия: что опаснее?» (Vetpharma, 2014, №4) было подробно рассмотрено симптоматическое лечение гипокалиемии кошек. В случае тяжелой гипокалиемии необходимо внутривенное введение солей калия, в других ситуациях возможно использование пероральных препаратов калия.
Сохранение гипокалиемии невыясненной этиологии, несмотря на суплементацию калием, должно навести на подозрение о возможности гиперальдостеронизма у кошек и расширить диагностические манипуляции, используемые для данного пациента. Безусловно, в этом случае мы не сможем рассчитывать на успех лечения, если своевременно не выявим и не попытаемся устранить первопричину гипокалиемии. В случае заболевания первичным гиперальдостеронизмом одно медикаментозное лечение вряд ли может нормализовать концентрации калия в циркулирующей крови. Но в подобных ситуациях обычно удается обеспечить контроль клинических симптомов, связанных с миопатией. В любом случае, как при первичном, так и при вторичном гиперальдостеронизме следует устранять первоисточник болезни.
В качестве дополнительных средств корректировки гипокалиемии при гиперальдостеронизме рекомендовано использовать также ИАПФ и калийсберегающие диуретики (антагонисты альдостерона). Применение этих препаратов возможно как в режиме монотерапии, так и совместно с препаратами калия, если их недостаточно для контроля концентрации ионов калия.
Спиронолактон – это конкурентный антагонист альдостерона, вызывающий задержку калия и экскрецию натрия. Рекомендованная доза для кошек – 2-5 мг/кг орально 1-2 раза в сутки.
С целью контроля артериальной гипертензии можно использовать амлодипина бесилат (амловас, амлодипин, нормодипин, вероамлодипин). Этот препарат первого выбора – антагонист кальция, блокирующий входящий трансмембранный поток ионов кальция и являющийся вазодилататором, снижающим периферическое сосудистое сопротивление, а за счет этого – кровяное давление. Инотропный эффект амлодипина очень слабый. Доза составляет на кошку от 0,625 до 1,25 мг 1 раз в сутки, но некоторым кошкам требуется увеличение дозы. Также нередко в рекомендациях можно встретить дозу 0,125-0,25 мг/кг 1 раз в сутки. Со временем подобранная доза может стать недостаточной, и тогда кошке потребуется применение дополнительно ИАПФ в сочетании с амлодипином.
Контроль пациента с симптомами гипертензии и гипокалиемии
Эффективные дозы препаратов калия и гипотензивных средств всегда должны подбираться индивидуально. Следует проводить тщательный мониторинг электролитов и артериального давления в течение 5-7 дней ежедневно после каждого изменения дозы используемых лекарственных средств или после начала применения новых лекарственных средств, пока показатели калия и артериального давления у кошки не достигнут границ нормы. Целью лечения является сначала снижение, а затем и устранение клинических симптомов и последствий гипокалиемической миопатии и артериальной гипертензии.
Хирургическое лечение
Летальность при проведении унилатеральной адреналэктомии составляет порядка 33%. Такая летальность может быть обусловлена тяжелым кровотечением из КПВ. Относительно высокий процент периоперационных летальных исходов ограничивает выбор данного метода лечения в качестве первостепенного. Но выбор терапевтического лечения в данном случае приведет лишь к паллиативной терапии.
Тем не менее, при унилатеральном поражении надпочечника новообразованием, адреналэктомия может стать самым предпочтительным вариантом лечения. Естественно, это лечение актуально при отсутствии видимых метастатических поражений. Успешная адреналэктомия способна вылечить пациента, в том числе без необходимости применения последующей терапии. Подготовка пациента к хирургическому лечению включает в себя обязательное устранение последствий и симптомов, связанных с ведущими последствиями гиперальдостеронизма: гипока-лиемии и артериальной гипертензии.
Кроме кровотечения из КПВ также сообщается о следующих осложнениях: интраабдоминальное кровотечение, острая почечная недостаточность, сепсис, тромбоэмболия.
Контроль концентрации электролитов в сыворотке крови и АД должен проводиться регулярно во время адреналэктомии, а также в ближайший послеоперационный период. Также подобные исследования могут оказаться полезными на протяжении нескольких послеоперационных дней. В случае сохранения гипертензии или гипокалиемии после адреналэктомии, стоит продолжать симптоматическую терапию до купирования этих патологий.
В заключение хочется отметить, что редкая диагностируемость гиперальдостеронизма может быть обусловлена не только редкой встречаемостью патологии, но и тем, что в некоторых случаях болезнь остается невыясненной, а диагноз не верифицирован в виду ограничения лабораторных и технических возможностей. Вероятно, пропаганда информации о болезни среди врачей и расширение границ лабораторной диагностики поспособствует большей инцидентности данной патологии кошек.
Литература
1. Бенчкроун Г, Розенберг Д. Атипичные эндокринные заболевания собак и кошек // Veterinary Focus. – 2011. - №1. - С 35-40.
2. Бэксфилд Н. Гиперальдостеронизм у кошек // Материалы Санкт-Петербургской ветеринарной терапевтической конференции. – 2013. - Р 38-47.
3. Макинтайр Д., Дробац К., Хаскингз С., Саксон У. Скорая помощь и интенсивная терапия мелких домашних животных. - М.: Аквариум, 2013. - 560 с.
4. Нельсон Р., Фельдман Э. Эндокринология и репродукция собак и кошек. - Софион, 2008. - 1256 с.
5. Современный курс ветеринарной медицины Кирка / под ред. Дж. Д. Бонагура; пер. с англ. - М.: Аквариум-Принт, 2005. - 1376 с.
6. Торранс Э.Д., Муни К. Т. Эндокринология мелких домашних животных. - М.: Аквариум, 2006. – 311 с.
7. Burkitt Creedon.М., Davis Н.Advanced Monitoring and Procedures for Smalt Animal Emergency and Critical Care. - Wiley-Blackwell, 2011. - 888 р.
8. Cochran Phillip E. Veterinary Anatomy & Physiology: A Clinical Laboratory Manual, 2nd Edition. - Delmar Cengage Learning, 2011. - 380 p.
9. Ettinger S., Feldman E. Textbook of Veterinary Internal Medicine Expert Consult, 7th Edition. - W.B. Saunders Company, 2009. - 2208 р.
10. Frances J. Barr, Lorrie Gaschen. BSAVA Manual of Canine and Feline Ultrasonography. - Publisher: British Small Animal Veterinary, 2011. - р. 222.
11. Gough А. Differential Diagnosis in Small Animal Medicine. - Blackwell Publishing Ltd, First published, 2007. - 464 р.
12. Jepson R.E, Syme H.M., Elliott J. Plasma Renin Activity and Aldosterone Concentrations in Hypertensive Cats with and without Azotemia and in Response to Treatment with Amlodipine Besylate // J Vet Intern Med. - 2014, - № 28. - Р. 144-153.
13. Kenneth J. Drobatz, Merilee F. Costello. Feline Emergency and Critical Care Medicine, 2010. - 672 p.
14. Lo A.J., Holt D.E., Brown D.C., Schlicksup M.D, Orsher R.J., Agnello K.A. Treatment of Aldosterone-Secreting Adrenocortical Tumors in Cats by Unilateral Adrenalectomy: 10 Cases (2002-2012) //J Vet Intern Med. - 2014; - №28. - Р. 137-143.
15. Mooney C. T., Peterson M. E. Canine and Feline Endocrinology. - BSAVA, 2004. - 248 p.
16. De Morais H.A., Bach J.F., DiBartola S.P. Metabolic Acid-Base Disorders in the Critical Care Unit // Vet Clin Small Anim. - 2008, - №38. - Р. 559-574.
17. Norkus С. Veterinary Technician's Manual for Small Animal Emergency and Critical Care. - Wiley-Blackwell. - 2012. - 567 р.
18. Norsworthy G.D., Grace S.F., Crystal M.A., Tilley L.P. The feline patient / editor, Gary D. Norsworthy. - Wiley-Blackwell, 4th ed. - 2011. - 1052 р.
19. Penninck D., d "Andre M. Small Animal Ultrasonography. - Blackwell Publishing Ltd. - 2008. - 502 р.
20. Silverstein D.C., Hopper K. Small Animal Critical Care Medicine, 2nd Edition. Saunders. - 2009. - 1152 p.
21. Steinbach S. Die chronische Nierenerkrankung der Katze // Kompendium Kleintier. - 2014. - Р17-25.
22. Textbook of Small Animal Medicine. Editor, John K. Dunn. - W.B. Saunders, 1999. - 1065 p.




Назад в раздел

















