Клинический случай использования оклацитиниба при генерализованной дискоидной красной волчанке у голой китайской хохлатой собаки /The clinical case of oclacitinib treatment of generalized discoid lupus erythematosus in a hairless Chinese crested dog
Еще фото
Автор (ы): Герке А.Н., к.в.н., врач-дерматолог ветеринарной клиники «СовВет», член Европейского общества ветеринарных дерматологов (ESVD), Санкт-Петербург
Журнал: №3–2021
Ключевые слова: голая китайская хохлатая собака, генерализованная дискоидная красная волчанка (ГДКВ), оклацитиниб
Keywords: hairless Chinese crested dog, generalized discoid lupus erythematosus (GDLE), oclacitinib
Сокращения:
ГДКВ – генерализованная дискоидная красная волчанка; СКВ – системная красная волчанка; ККВ – кожная красная волчанка
Аннотация
Генерализованная дискоидная красная волчанка является разновидностью хронической кожной красной волчанки (ККВ) у собак. Цель этой статьи – представить клинический случай успешного лечения оклацитинибом собаки c ГДКВ. Диагноз был поставлен на основании клинической картины, гистопатологии, лабораторных исследований. Владелец 8-летней голой китайской хохлатой собаки обратился с жалобами на болезненные язвенные поражения кожи на протяжении четырех месяцев. На туловище, животе, шее, в паху, медиальной поверхности задних конечностей, грудной клетке отмечено изменение пигментации (чередование гипер- и депигментированных участков), эритема, эрозии, сливающиеся корочки, язвы, струп. Клинический диагноз был подтвержден гистологически наличием высоко клеточного лимфоцитарного пограничного дерматита. Отсутствие системных признаков и отклонений в лабораторных тестах исключили системную красную волчанку. Лечение было начато с оклацитиниба 0,46 мг/кг два раза в день, было рекомендовано ограничение пребывания на солнце. В течение двух месяцев наблюдалась полная ремиссия, и прием оклацитиниба был сокращен до одного раза в сутки. Побочных эффектов при использовании этого режима не наблюдалось. Еще через месяц лечение было прекращено. На момент написания статьи спустя два месяца после отмены лечения, рецидива болезни не было.
Summary
Generalized discoid lupus erythematosus is a variant form of chronic cutaneous lupus erythematosus (CLE) in dogs. The purpose of this report is to describe a dog with GDLE that was treated with oclacitinib successfully. The diagnosis was made based on the clinical presentation, histopathology, and laboratory values. The owners of a 8-year-old hairless Chinese crested dog reported ulcerative painful skin lesions observed for four months. There was a change in pigmentation (alternation of hyper- and depigmented areas), erythema, erosion, crusts, ulcers, and a scab on the trunk, abdomen, neck, groin, medial surfaces of the
hind limbs, and chest. The clinical diagnosis of GDLE was supported by histology with the lymphocyte-rich interface dermatitis. The absence of systemic signs and unremarkable laboratory tests excluded concurrent systemic lupus erythematosus. The treatment was initiated with oclacitinib 0,46 mg/kg twice daily along and restriction of sun exposure. Over the two months, complete remission was maintained and administration oclacitinib was reduced to once daily. After next month the treatment was discontinued. At the time of writing, two months later, disease flares and adverse drug events with this regimen were not seen.
Введение
Красная волчанка – термин, охватывающий группу болезней, проявляющихся разными клиническими синдромами и связанный с различными аутоиммунными механизмами. Красные волчанки подразделяются на две группы – с системными проявлениями (СКВ) и кожные красные волчанки (ККВ). Впервые кожная красная волчанка у собак была описана в 1979 г. Позже выяснилось, что у собак встречаются несколько вариантов кожной волчанки, причем некоторые виды схожи с волчанками у человека, а некоторые – видоспецифичны для собак. Основываясь на классификации волчанок Гиллиама-Зонтхаймера, принятой в медицине человека, с учетом клинических появлений, отклонений в лабораторных анализах, включая гистопатологию, а также ответе на лечение, в настоящее время различают следующий варианты кожной красной волчанки (CLE) у собак: везикулярную (VCLE), эксфолиативную (ECLE), волчанку границ кожи и слизистых (MCLE), дискоидную волчанку (DLE), в том числе в области морды и генерализованную дискоидную красную волчанку [11, 15]. Кроме того, выделяют группу неспецифических кожных болезней, которые могут наблюдаться не только у собак с красной волчанкой, но и как самостоятельные заболевания. К этой группе относятся волчаночный васкулит, лимфоцитарный панникулит, буллезная СКВ типа I, связанная с аутоантителами, приобретенный буллезный эпидермолиз, возникающий в сочетании с СКВ [22] и др.
Патогенез
Кожная красная волчанка относится к группе аутоиммунных болезней, обусловленных лимфоцитами. В настоящее время мало что известно об этиологии и патогенезе развития кожных поражений при красной волчанке у собак. В соответствии с гипотезой, базальные кератиноциты, поврежденные цитотоксичными лимфоцитами, подвергаются гиперпролиферации, что индуцирует экспрессию р-53, который, в свою очередь, активирует патологические механизмы, приводящие к апоптозу эпидермиса [18].
Недавние исследования показали, что активация рецепторных путей распознавания патогенов посредством нуклеиновых кислот является потенциальным ключевым механизмом при кожной красной волчанке у собак. Установлено, что иммунные реакции при ККВ обусловлены интерферон-ассоциированным воспалением, пролиферацией лимфоцитов с преобладанием Th1, активацией сигнального пути JAK-STAT-киназ (JAK – Janus-киназа; STAT – сигнальный трансдуктор и активатор транскрипции, – прим. ред.) и цитотоксичностью NK-клеток [5].
Половой предрасположенности при ГДКВ не выявлено. Отмечена склонность к развитию ГДКВ у некоторых пород собак, в том числе китайской хохлатой, лабрадоров-ретриверов, миниатюрных пинчеров, леонбергеров, ши-тцу, той-пуделей. В отличие от эксфолитативной кожной красной волчанки, описанной у короткошерстных пойнтеров, и красной волчанки кожно-слизистых зон, чаще встречающейся у немецких овчарок, у собак этих пород не зарегистрировано случаев генерализованной дискоидной красной волчанки. Как правило, ГДКВ развивается у взрослых собак в возрасте от 5 до 12 лет. В большинстве случаев эти животные не имеют каких-либо хронических болезней. Также не установлена связь развития ГДКВ с лекарственными препаратами, в отличие от мультиформной эритемы [2].
Клиническая картина
Генерализованная дискоидная красная волчанка характеризуется хроническим или рецидивирующий течением. Нередко кожные поражения развиваются за 3 – 24 месяца до визита к врачу. Первоначальные поражения, о которых чаще всего сообщают владельцы, проявляются эритематозными пятнами, папулами и бляшками с эрозиями и шелушением. Обычно они располагаются на шее, туловище, спине, боковой части грудной клетки, голове, брюшной стенке, а также медиальных и латеральных поверхностях проксимальной части конечностей. На момент осмотра кожные поражения представляют собой генерализованные или мультифокальные, от кольцевидной (дискоидной) до полициклической формы бляшки с эритематозным краем, слипчивым шелушением, корками, центральной алопецией. Часто бляшки превращаются в язвы с центральными атрофическими или гипертрофическими рубцами. Классические бляшки «в форме монеты» имеют участки центральной депигментации, рубцы и периферическую гиперпигментацию. Характерно диффузное изменение пигментации (чередование участков депигментации и гиперпигментации). Также нередко отмечают сетчатую гиперпигментацию, развивающуюся в результате слияния кожных поражений. Возможна закупорка фолликулов, особенно на внутренней поверхности ушной раковины. Кожные поражения могут сопровождаться зудом или болью у 40% собак [2].
Системные нарушения не характерны для ГДКВ, в отличие от системной красной волчанки, возможно развитие регенеративной анемии легкой степени и умеренное повышение ферментов печени. Нефропатия, сопровождающаяся протеинурией, также не развивается при этой форме ККВ, в отличие от СКВ.
У людей, пораженных генерализованной дискоидной волчанкой, часто обнаруживается положительный титр антинуклеарных антител (ANA), который представляет собой фактор риска развития системной красной волчанки в течение 5 лет после появления первых поражений кожи и постановки диагноза. У собак, в отличие от людей, в редких случаях отмечают положительный ANA-титр сыворотки, при этом прогрессирование болезни до проявления дополнительных критериев СКВ не наблюдалось в течение среднего периода наблюдения 2,5 года (диапазон от 0,5 до 6 лет) [2].
Гистопатология
Характерные гистопатологические изменения включают лимфоцитарный пограничный (интерфейс-) дерматит с высоким содержанием клеток, дегенерацию базальных кератиноцитов от умеренной до выраженной, а также вакуолизацию кератиноцитов и апоптоз. Распространение этих поражений может варьироваться от диффузного до очагового; при тяжелом повреждении базального слоя клеток возможно образование микроскопической щели. Апоптоз в надбазальных слоях эпидермиса наблюдался часто, от легкой до умеренной степени. Характерен лимфоцитарный сателлитоз апоптотических базальных клеток. Очаги эпидермальной атрофии встречаются редко, и в большинстве случаев наблюдается диффузная эпидермальная гиперплазия от легкой до умеренной степени и ортокератический гиперкератоз с периодическим прерыванием очагами паракератоза. Во всех очагах эпидермальной депигментации и/или участках эпидермальной гиперпигментации отмечается недержание пигмента от умеренного до выраженного. Часто наблюдается легкое периваскулярное воспаление в поверхностной дерме, тогда как в средней и глубокой дерме оно минимально или отсутствует. В области рубцовой ткани гистологически отмечают легкий или выраженный поверхностный фиброз кожи, который может распространяться до зоны базальной мембраны.
Воспалительный процесс охватывает и придатки кожи, часто отмечается лимфоплазмоцитарный перифолликулит и фолликулит, проявляющийся инфильтрацией скоплениями лимфоцитов внешней корневой оболочки волос в стадии анагена, телогена, а также атрофических фолликулов. Редко отдельные лимфоциты могут проникать в волосяную луковицу в анагене. Характерна атрофия волосяных фолликулов и сальных желез. Воспаление внутри желез ограничивается стенками сальных протоков, которые могут содержать единичные лимфоциты; инфильтрация долек сальных желез не наблюдается [2].
Диагноз
Основные диагностические критерии при ГДКВ включают:
o хроническое течение (наличие кожных поражений на протяжении более чем 2 месяцев);
o характерные клинические признаки: эрозии и язвы, имеющие тенденции к заживлению с рубцеванием (что является важным отличием от красной волчанки кожно-слизистых зон при поражении в области морды), корочки, фигурная или сетчатая гиперпигментация, отсутствие системных нарушений;
o отсутствие клинического ответа на местные или системные антибиотики и антисептики;
o гистопатология: интерфейс-дерматит с выраженной лимфоцитарной инфильтрацией с вовлечением базальных кератиноцитов.
Важно отметить, что при гистологическом исследовании такой важный диагностический критерий как апоптоз кератиноцитов может привести к путанице с мультиформной эритемой и морфологически связанными состояниями. Поэтому важна оценка данных истории болезни с учетом хронического характера течения и отсутствия лекарственного анамнеза. Также учитывают клиническую картину: быстро распространяющиеся эритематозные макулы, волдыри, мишеневидные поражения и эрозивные поражения, гистологически сопровождающиеся цитотоксическим лимфоцитарным пограничным дерматитом с апоптозом кератиноцитов во многих эпидермальных слоях, указывают на мультиформную эритему.
Неудивительно, что при наличии язв часто развивается сопутствующая бактериальная инфекция. В этом случае отмечают нейтрофильную инфильтрацию под корочками, пустулы, перифолликулит и фолликулит, а также присутствие бактерий в поверхностных экссудатах. Наличие инфекции усложняет оценку гистологического препарата, поэтому перед биопсией необходимо провести лечение пиодермии.
Чтобы исключить сопутствующую системную красную волчанку (СКВ), дальнейшие исследования включают биохимический профиль сыворотки, общий анализ крови, анализ мочи и ANA-тест сыворотки крови.
Лечение и прогноз
Спонтанного разрешения кожных поражений при ГДКВ не описано ни в одном случае, несмотря на хороший прогноз при своевременно начатом лечении [2, 15].
После исключения сопутствующей СКВ и гистологического подтверждения диагноза ГДКВ рекомендуют избегать чрезмерного пребывания на солнце и назначают иммуносупрессивную терапию [21].
Традиционно, терапию аутоиммунных болезней начинают с кортикостероидов в иммуносупрессивных дозах до достижения контроля заболевания, а затем уменьшают дозу медленно и поэтапно для поддержания ремиссии.
Преднизолон и дексаметазон являются наиболее часто используемыми глюкокортикоидами при иммуносупрессивной терапии. Основные различия между этими препаратами заключаются в их относительной активности: дексаметазон примерно в семь раз более эффективен, чем преднизолон [21]. Начальная доза преднизолона не должна превышать 2,0 ± 4,0 мг/кг перорально в сутки, за исключением очень маленьких собак, у которых доза может быть больше. При назначении этих начальных высоких доз можно вводить препарат в разделенных суточных дозах.
Альтернативой является пульсовая терапия кортикостероидами, когда преднизолон вводится орально или парентерально в дозе 10 мг/кг в сутки в течение 3 суток, далее в обычной противовоспалительной дозе 1 мг/кг. Курсы «пульсовой» терапии повторяют еженедельно до достижения ремиссии. Наиболее распространенными побочными эффектами глюкокортикоидов являются диарея, рвота, агрессия, полиурия, полидипсия, полифагия.
В дополнение к стероидам часто используют другие иммуносупрессивные препараты. К сожалению, нестероидные иммунодепрессанты обычно не работают так же хорошо, как глюкокортикоиды в качестве единственного препарата. Поэтому комбинированная терапия используется:
o когда есть частичный ответ на стероидную терапию;
o когда болезнь можно контролировать только с помощью высоких доз стероидов, опасных для здоровья животного;
o когда необходимо сократить сроки достижения ремиссии;
o с целью снижения дозировки каждого препарата в отдельности.
Использование комбинации нескольких препаратов снижает токсичность при сохранении или даже повышении общей терапевтической эффективности.
Возникает очевидный вопрос: «Когда следует использовать глюкокортикоиды по отдельности, а когда следует начинать комбинированную иммуносупрессивную терапию?». Это решение основано на опыте использования этих препаратов и опыте ветеринарного врача по лечению данного заболевания.
Помимо фотозащиты и глюкокортикоидов при лечении ГДКВ успешно использовались различные схемы лечения, включая ингибиторы кальциневрина (системно циклоспорин и местно – такролимус), противомалярийный препарат гидроксихлорохин, оклацитиниб, тетрациклиновые антибиотики в сочетании с никотинамидом и без него [2].
С 1992 г. было высказано предположение, что антибиотики группы тетрациклинов наряду с ниацинамидом могут быть использованы для лечения иммуноопосредованных кожных заболеваний собак, включая варианты кожной красной волчанки. С тех пор доксициклин, антибиотик тетрациклинового ряда, широко используется в дерматологии не только в качестве антибиотика, но и как иммуномодулирующее средство, обладающее противовоспалительными свойствами и имеющее хороший профиль безопасности. Доксициклин воздействует на воспалительные цитокины (TNF-α, IL-8, MCP-1, NF-kB, TACE, IL-6, IL-1β), металлопротеиназы (ММР-2, ММР-3, ММР-8, ММР-9, ММЗ-13), подавляет хемотаксис лейкоцитов и апоптоз, Ig E, фосфолипазу А2 и др. Доксициклин назначают совместно с ниацинамидом (никотинамидом), являющимся эндогенным ингибитором (аденозиндифосфат[ADP]-рибоза) полимеразы 1 (PARP-1). Ниацинамид подавляет секрецию провоспалительных цитокинов (IL-1β, IL-6, IL-8, IL-12 и TNF-α, хемотаксис нейтрофилов и эозинофилов, дегрануляцию тучных клеток, высвобождение вазоактивных аминов, пролиферацию В-лимфоцитов, секретирующих антитела, а также воздействует на главный комплекс гистосовместимости типа II (MHC-II) [10].
В одной публикации описана полная ремиссия у собаки с ГДКВ с использованием исключительно комбинации тетрациклина/ниацинамида (в дозе 45 мг/кг каждого лекарства три раза в день). В другом исследовании, напротив, не наблюдалось клинического улучшения на комбинации доксициклина и ниацинамида в течение 4 месяцев в дозе 250–500 мг на собаку каждого препарата три раза в сутки) [2, 20, 23].
В другом клиническом случае лечение было начато с перорального приема дексаметазона и циклоспорина. Через 1 месяц прием дексаметазона был прекращен, и к терапевтическому режиму был добавлен пероральный кетоконазол. Через четыре месяца зуд и эритема исчезли, и большинство кожных повреждений перестали пальпироваться. В течение последних 6 месяцев у пациента поддерживалась ремиссия при пероральном приеме циклоспорина и кетоконазола в комбинации каждые 3 дня.
Полагают, что ингибиторы кальциневрина ввиду медленного развития эффекта целесообразно сочетать с коротким курсом глюкокортикоидов в начале лечения, возможно, в меньших дозах, чем при терапии одними стероидами. В ряде публикаций отмечено заметное улучшение или полная ремиссия кожных поражений после лечения циклоспорином (в диапазоне доз 3,3 – 6 мг/кг, в среднем 4,8 мг/кг один раз в сутки) в сочетании с преднизолоном (в дозах 1 – 2 мг/кг/день, с постепенным снижением в течение месяца) и кетоконазолом (дозы в диапазоне 1 – 3,3 мг/кг, в среднем 2,3 мг/кг один раз в сутки) у трех собак с ГДКВ [3, 9].
Еще одним иммуномодулятором, который использовался для лечения собак с ГДКВ, является антималярийное средство гидроксихлорохин. Исследование показало, что пероральный прием гидроксихлорохина в дозе 5 мг/кг один раз в день в сочетании с местным применением 0,1% такролимуса в течение 2 недель помог достичь ремиссию кожных поражений и поддержать ее у двух собак с этим заболеванием. Хотя токсичность сетчатки ограничивает использование этого препарата у людей, она не наблюдалась у собак [14].
Возможно, в перспективе может быть полезным использование микофенолята мофетила, поскольку имеются данные о положительном результате использования его в монорежиме у собак с эксфолиативной кожной волчанкой. Стартовая доза составила 22 мг/кг дважды в сутки в течение 3 недель до клинического улучшения, затем доза была снижена до 10 мг/кг дважды в сутки. Через четыре месяца была достигнута полная ремиссия [8, 13].
Последнее время ведутся исследования, предварительные результаты которых позволяют предположить, что оклацитиниб, ингибитор Янус-киназы (JAK) первого поколения, одобренный во многих странах для лечения атопического дерматита и аллергического зуда у собак, обладает также иммуносупрессивными свойствами. Помимо своего противозудного действия, которое, в первую очередь, опосредуется ингибированием передачи сигналов через рецептор интерлейкина (IL)-31, оклацитиниб также проявляет противовоспалительную активность с ингибированием in vitro IL-2, IL-4, IL-6 и IL-13. Недавнее исследование продемонстрировало, что оклацитиниб при применении в дозах, превышающих рекомендованные, обладает и иммуносупрессивной активностью in vitro с ингибированием пролиферации Т-клеток и секреции IL-2, IL-15, интерферона-гамма (IFN-c), IL-18 и IL-10. Последнее время появился ряд публикаций об успешном использовании оклацитиниба у собак при различных иммуноопосредованных болезнях [1, 4, 6, 7, 12, 19], таких как мультиформная эритема, ювенильная ишемическая дерматопатия, субэпидермальный буллезный дерматоз. Кроме того, описывается его благоприятный эффект при идиопатическом васкулите у собак, даже не поддающемся традиционной терапии.
Как долго проводить лечение после наступления клинической ремиссии?
После исчезновения клинических признаков уровень глюкокортикоидов следует снизить в течение нескольких недель до поддерживающего уровня (например, преднизолон в дозе 1,0 мг/кг перорально через день или, если возможно, реже). Не стоит прекращать терапию глюкокортикоидами в течение, как минимум, одного – трех месяцев после того, как болезнь перешла в стадию ремиссии; при этом, чем больше времени требуется для достижения ремиссии, тем медленнее надо снижать дозу. Если прием лекарств прекращается слишком рано, вероятность рецидива заболевания выше. При комбинированной терапии, включающей кортикостероиды и вспомогательные иммуносупрессоры, достигнув клинической ремиссии, сперва постепенно отменяют кортикостероид, затем и вспомогательные препараты.
Согласно статистике, полная ремиссия клинических признаков (возможно наличие рубцовой алопеции в некоторых очагах поражения) у собак с ГДКВ после лечения произошла через 3 – 6 месяцев (в среднем 4,5 месяца) у 50% собак, тогда как частичная ремиссия (разрешение приблизительно 75% поражений) наблюдалась через 1 – 6 месяцев (в среднем 5,5 месяцев) у других 50% собак. Попытка прекратить или сократить лечение привела к быстрому рецидиву типичных кожных повреждений у 60% животных. Повторное частичное возобновление схемы лечения (например, с более низкой частотой введения – циклоспорин через день; местный такролимус два раза в неделю) было достаточным для полного контроля клинических признаков [2].
Клинический случай
На дерматологический прием поступил кастрированный кобель голой китайской хохлатой собаки в возрасте 8 лет. Первые поражения возникли около четырех месяцев назад, в ноябре, на тот момент собаке никакие противопаразитарные обработки и вакцинации не проводились. Основными клиническими признаками был зуд в области ушей, шеи и живота, эритема, корочки и эпидермальные воротнички, церуменозная гиперсекреция, в цитологии наблюдалась нейтрофильная лейкоцитарная реакция с фагоцитозом кокковой микрофлоры. Предварительным диагнозом была поверхностная пиодермия на фоне блошиного аллергического дерматита, было назначено лечение амоксициллин-клавуланатом и оклацитинибом совместно с купанием с шампунем с 4% хлоргексидином. Также были рекомендованы обработки от блох всех животных, содержащихся совместно, которые, тем не менее, не были сделаны в связи с холодным временем года. На фоне лечения зуд снизился, но поражения кожи прогрессировали. Лечение было прекращено, и владелец обратился в другую клинику. В сторонней клинике врач назначил местные обработки спреем с 4% хлоргексидином и кремом с бетаметазоном, однако, поражения кожи распространялись, усилился зуд, проявляющийся чрезмерным вылизыванием области паха, конечностей и живота. В связи с этим был назначен преднизолон в дозе 1 мг/кг 1 раз в сутки в течение недели, возобновлен курс амоксициллин-клавуланата в дозе 25 мг/кг дважды в сутки. При этом зуд не был взят под контроль, а поражения кожи прогрессировали. В другой клинике врач заменил преднизолон на дексаметазон в дозе 0,1 мг/кг, а амоксициллин-клавуланат на цефовецин трехкратно с интервалом 14 дней. Собака была обработана от блох пероральным сароланером, также была проведена дезинсекционная обработка окружающей среды. Тем не менее, поражения прогрессировали, появилась болезненность, местные обработки стали затруднительны.
На момент осмотра (в марте): кастрированный кобель голой китайской хохлатой собаки нормальной упитанности, не дегидратирован, видимые слизистые оболочки бледно-розовые, без патологий. При осмотре наблюдались признаки боли, при прикосновении к очагам поражения кожи собака вела себя агрессивно. При отоскопии наружные слуховые проходы проходимы, не гиперемированы, барабанные перепонки интактны, визуализируются темно-коричневые мажущиеся выделения в умеренном количестве. Кожа области спины лишена шерсти, пигментирована, присутствуют единичные комедоны, наблюдается ксероз легкой степени. Область морды без особенностей. На туловище, животе, шее, в паху, медиальной поверхности задних конечностей, грудной клетке отмечено изменение пигментации (чередование гипер- и депигментированных участков), эритема, эрозии, корочки, язвы, струп (фото 1, 2). Доступные лимфатические узлы не изменены.
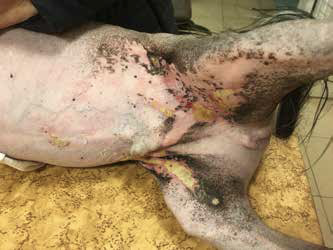
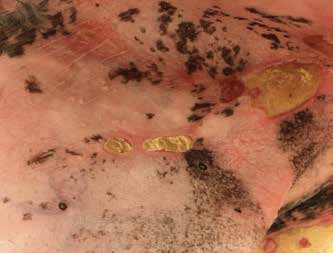
Фото 1, 2. Изменение пигментации, эритема, эрозии, корочки, язвы, струп в области живота, паха, внутренней поверхности задних конечностей
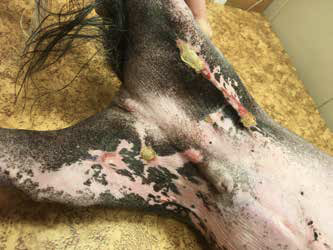
Фото 3. Поражения в области паха, внутренней поверхности задних конечностей (эрозии, струп, изменение пигментации) через 3 недели от начала терапии. Отмечено значительное уменьшение площади поражений и болезненности. Поражения заживают с образованием хорошо пальпируемых рубцов
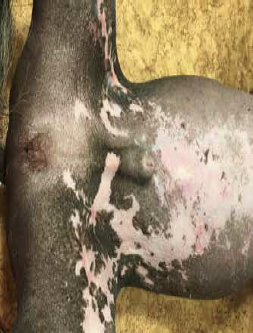
Фото 4. Через 2 месяца на фоне терапии оклацитинибом. Клиническая ремиссия. Изменение пигментации и рубцы на местах, где были наиболее глубокие поражения
Поскольку направивший ветеринарный врач ранее подозревал пиодермию, и собаке был проведен курс цефовецина на протяжении шести недель без значимого улучшения кожных повреждений, было принято решение о гистологическом исследовании кожи. Были получены два биоптата кожи с использованием 8-миллиметрового панча из пораженной кожи области паха и живота, и один эллиптический кожный биоптат со стороны бедра на границе пораженных и здоровых тканей. Образцы были помещены в 10% нейтральный забуференный формалин для заливки парафином и рутинного гистопатологического исследования.
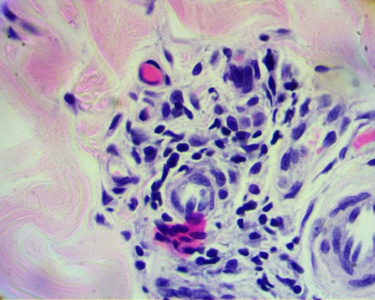
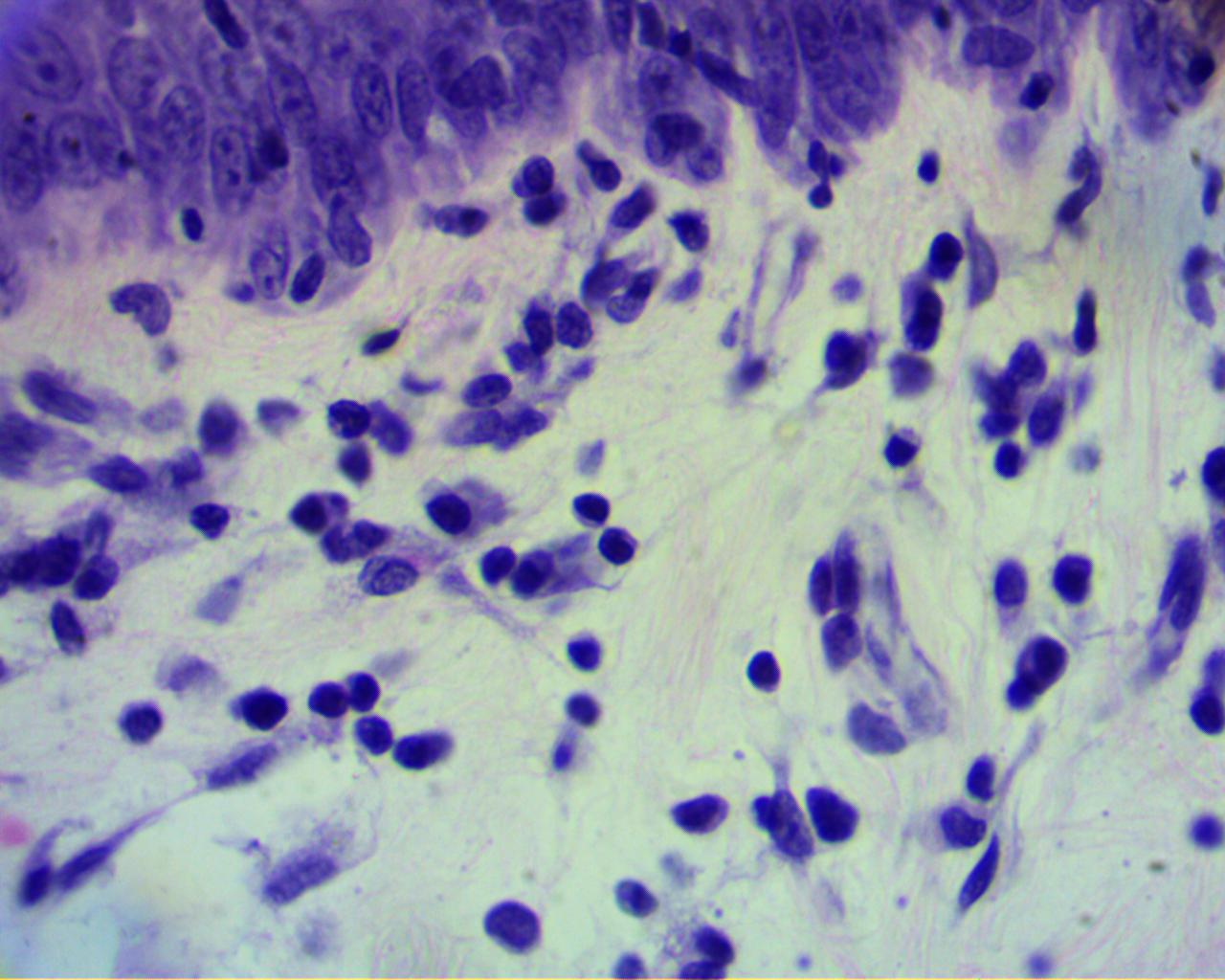
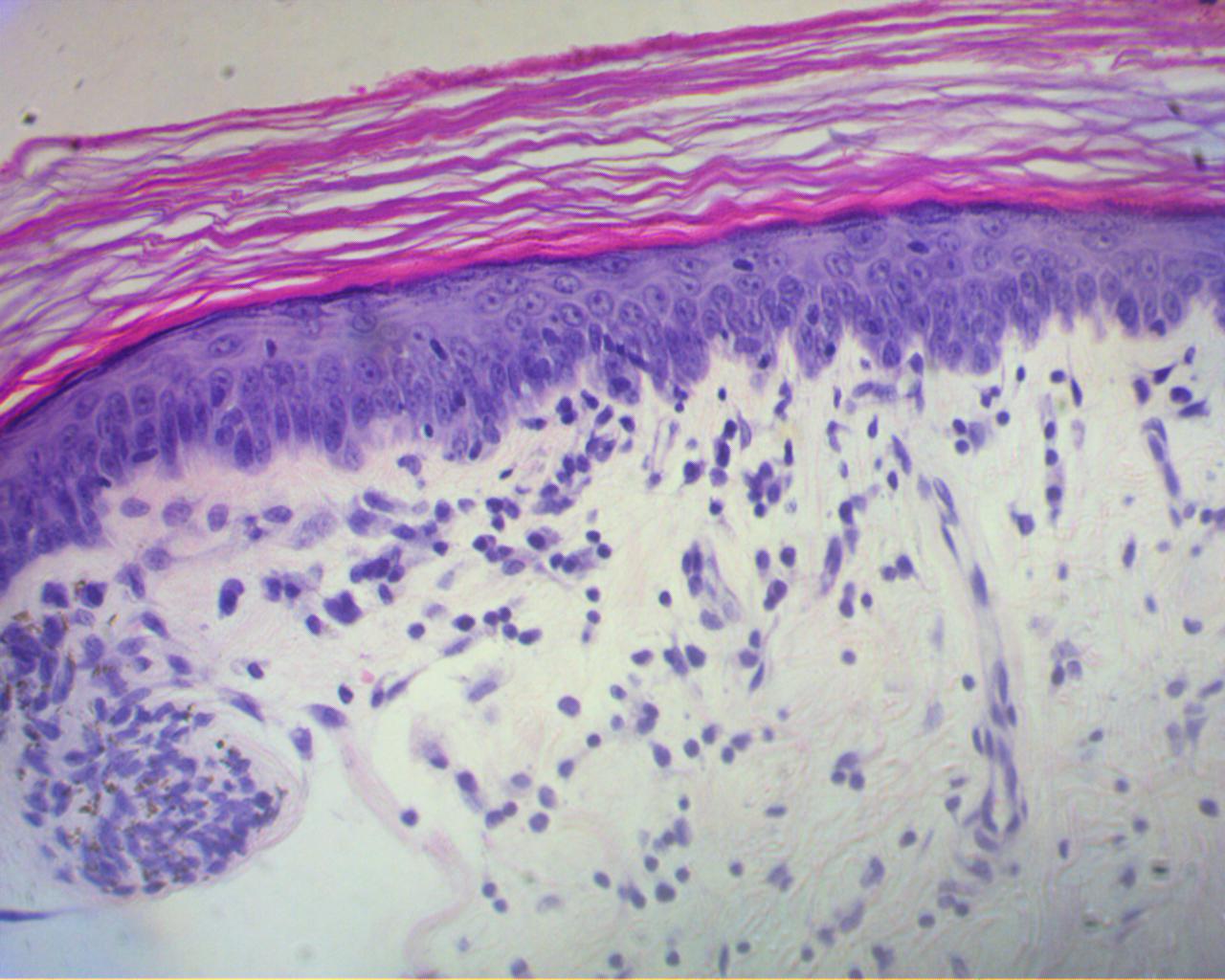
При гистологическом исследовании установлена выраженная (высоко-клеточная) лимфоцитарная инфильтрация, связанная с ней вакуолизация базальных кератиноцитов, нечастый апоптоз, недержание пигмента. Наблюдается утолщение зоны базальной мембраны. Эпидермис гиперплазирован и частично разрушен (фото 5, 6, 7, 8).
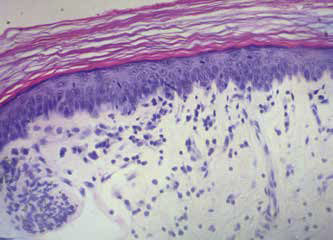
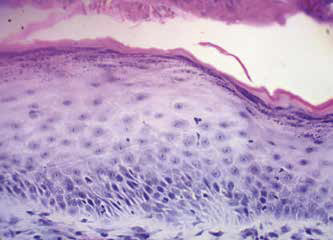
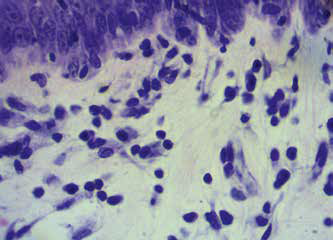
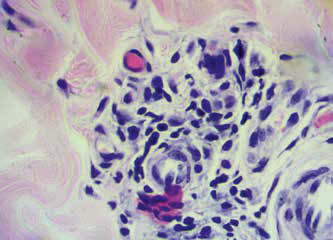
Фото 5, 6, 7, 8. Гистология. Субэпидермальный лимфоцитарный инфильтрат (лимфоцитарный пограничный дерматит), вакуолизация базальных кератиноцитов, редкий апоптоз, недержание пигмента. Утолщение зоны базальной мембраны. Гиперплазированный эпидермис частично разрушен. Окраска гематоксилин и эозин, увеличение 400х
До результатов гистологического анализа был назначен оклацитиниб в дозе 0,46 мг/кг дважды в сутки и местные обработки пеной с декспантенолом. Через 3 недели от начала терапии оклацитинибом наблюдалась положительная динамика, поражения в области паха, внутренней поверхности задних конечностей (эрозии, струп) значительно сократились по площади, снизилась болезненность, но сохранялся зуд (без воротника собака пыталась лизать). На месте эрозий развивалась депигментация с образованием плотных рубцов (фото 3). Никаких отклонений в общем состоянии не отмечено. Были взяты рутинные анализы крови и мочи для исключения системных нарушений, характерных для системной красной волчанки, результаты оказались в пределах референсных значений. Было принято решение продолжить терапию оклацитинибом 2 раза в сутки на протяжении месяца, далее перейти на режим 1 раз в сутки. Дополнительно был назначен Витамин Е (токоферола ацетат) в дозе 400 мг в сутки. Через 2 месяца отмечена клиническая ремиссия (фото 4), только наблюдается изменение пигментации (чередование участков гиперпигментации и гипопигментации), пальпируются рубцы на местах наиболее глубоких очагов. Зуд не выражен. На период наблюдения в течение 2-х месяцев после отмены оклацитиниба новых поражений не отмечено.
Обсуждение
Генерализованная дискоидная красная волчанка – редкая аутоиммунная болезнь кожи. В литературе имеются данные о породной предрасположенности, в том числе описано 2 случая у китайских хохлатых собак [15]. Отмечено, что средний возраст первых проявлений ГДКВ – от 5 до 12 лет, этот диапазон соответствует возрасту данного пациента. Не выявлено половой предрасположенности, соотношение самцы: самки составило 1,0 [2].
По литературным данным [3, 14, 15, 20], наиболее частыми клиническими признаками являются нарушение пигментации, эритема, эрозии, язвы, шелушение и корки, заживающие с образование рубцов, в области туловища, проксимальной части конечностей и живота, а также зуд и боль в половине случаев [2]. В нашем клиническом случае первыми клиническими признаками была эритема и зуд, далее быстро образовались эрозии и язвы, покрытые корками, а позже образовался струп. Поражения прогрессировали, несмотря на системную и местную антимикробную терапию. Для ГДКВ типично отсутствие системных нарушений, в данном клиническом случае не было отмечено отклонений в общем состоянии, за исключением боли. Результаты рутинных анализов крови также были в пределах нормы.
В списке дифференциальных диагнозов при ГДКВ рассматриваются гиперкератотическая мультиформная эритема и генерализованные ишемические дерматопатии. При этом характерных для васкулопатий поражений в области ушных раковин, подушечек лап, кончика хвоста не наблюдалось. Ожидаемо, что при генерализованной ишемической дерматопатии, дистальные участки тела в первую очередь вовлекаются в воспалительный процесс.
В отличие от мультиформной эритемы, не было никакого лекарственного анамнеза, в том числе противопаразитарных обработок, процесс развивался длительно, на протяжении более трех месяцев.
Поскольку предварительно собаке была проведена противомикробная терапия, на первичном приеме было возможным получить образцы гистобиоптатов кожи и начать пробную терапию оклацитинибом. Гистопатология показала пограничный дерматит с высоким содержанием лимфоцитов, характерный для ГДКВ. Гиперплазированный эпидермис был частично разрушен, в средней и глубокой дерме имелись признаки минимального периваскулярного лимфоцитарного воспаления, по-видимому, связанного с сопутствующим волчаночным васкулитом.
В данном случае, анамнез, клинические проявления, локализация поражений, а также ответ на терапию наряду с гистопатологией соответствовали ГДКВ собак.
Хороший и быстрый клинический ответ на оклацитиниб в период ожидания результатов гистологического исследования позволил получить данные о возможности его использования не только для контроля зуда у собак с аллергией, но и в качестве иммуномодулирующего средства при аутоиммунных болезнях кожи собак. Лечение оклацитинибом было продолжено и привело к стойкой ремиссии.
Заключение
Генерализованная дискоидная красная волчанка – редкая аутоиммунная болезнь кожи собак. При диагностике следует обращать внимание на основные диагностические критерии ГДКВ, которые включают хроническое медленно прогрессирующее течение, характерную клиническую картину, в том числе эрозивно-язвенные дефекты, заживающие с образованием рубцов, отсутствие клинического ответа на антибактериальную терапию [2]. В этом случае обязательным диагностическим шагом должно быть гистологическое исследование до начала какой-либо иммуносупрессивной терапии. ГДКВ хорошо отвечает на применение иммунодепрессантов, однако схемы лечения и дозы препаратов могут сильно варьироваться от случая к случаю. У половины собак возможна полная ремиссия на протяжении длительного времени, поэтому при достижении клинического выздоровления следует попробовать отменить терапию постепенно. В случае возникновения рецидива стоит подбирать режим поддерживающей терапии в минимальных, но достаточных для поддержания клинической ремиссии, дозах.
Литература
1. Aymeric E., Bensignor E. A case of presumed autoimmune subepidermal blistering dermatosis treated with oclacitinib/ Vet. Dermatol. 2017; 28: 512 – e123. 1.
2. Banovic F., Linder K.E., Uri M., Rossi M.A., Olivry T. Clinical and microscopic features of generalized discoid lupus erythematosus in dogs (10 cases)/Vet Dermatol. 2016; 27: 488–e131.
3. Banovic F., Olivry T., Linder K.E. Ciclosporin therapy for canine generalized discoid lupus erythematosus refractory to doxycycline and niacinamide/ Vet Dermatol. 2014; 25: 483– e79.
4. Banovic F., Tarigo J., Gordon H. et al. Immunomodulatory in vitro effects of oclacitinib on canine T-cell proliferation and cytokine production. /Vet Dermatol. 2019; 30: 17– e6.
5. Banovic F., Blubaugh A., Denley T. and al. Transcriptome profiling of canine chronic cutaneous lupus erythematosus skin lesions using deep RNA sequencing/ Proceeding 3st European Veterinary Dermatology Congress. 26 - 28 September 2019. Liverpool. Р.113.
6. Colombo S., Cornegliani L., Vercelli A., Fondati A. Ear tip ulcerative dermatitis treated with oclacitinib in 25 dogs: a retrospective case series/Vet Dermatol. 2021; 32: 363-e100.
7. Endya J.H., Linder K.E., Mamo L.B. et al. Rapid response of hyperkeratotic erythema multiforme to oclacitinib in two dogs/ Vet Dermatol. 2020; 31: 330– e86.
8. Ferrigno A., Hoover K., Blubaugh A. et al. Treatment of exfoliative cutaneous lupus erythematosus in a German shorthaired pointer dog with mycophenolate mofetil/Vet Dermatol. 2019; 30: 350– e102.
9. Font A., Bardagi M., Mascort J., Fondevila D. Treatment with oral cyclosporin a case of vesicular cutaneous lupus erythematosus in a rough collie/Vet Dermatol. 2006; 17: 440–2.
10. Henehan M., Montuno M., De Benedetto A. Doxycycline as an anti-inflammatory agent: updates in dermatology/JEADV. 2017; 31 (11): P. 1800-1808.
11. Jackson H.A. Eleven cases of vesicular cutaneous lupus erythematosus in Shetland sheepdogs and rough collies: clinical management and prognosis. /Vet Dermatol. 2004; 15: 37–41.
12. Levy B.J., Linder K.E., Olivry T. The role of oclacitinib in the management of ischaemic dermatopathy in four dogs /Vet Dermatol. 2019; 30: 201– e63.
13. Manzuc P.J., Koch S.N., Benzoin L., Grandinetti J. Mycophenolate mofetil in the therapy of vesicular cutaneous lupus erythematosus: a case report/Vet Dermatol. 2016;27(Suppl. 1):87. (abstract).
14. Oberkirchner U., Linder K.E., Olivry T. Successful treatment of a novel generalized variant of canine discoid lupus erythematosus with oral hydroxychloroquine/Vet Dermatol. 2012; 23: 65,70 - e16.
15. Olivry T., Linder K.E., and Banovic F. Cutaneous lupus erythematosus in dogs: a comprehensive review/BMC Veterinary Research. 2018, 14(1):132. В свободном доступе: https://bmcvetres.biomedcentral.com/articles/10.1186/s12917-018-1446-8
16. Olivry T., Rossi M.A., Banovic F., Linder K.E. Mucocutaneous lupus erythematosus in dogs (21 cases)/Vet Dermatol. 2015; 26: 256–e55.
17. Olivry T. Auto-immune skin diseases in animals: time to reclassify and review after 40 years/ BMC Veterinary research. 2018; 14. В свободном доступе: https://bmcvetres.biomedcentral.com/articles/10.1186/s12917-018-1477-1
18. Pedersen N.C. A review of immunologic diseases of the dog. / Veterinary Immunology and Immunopathology. 1999; 69: 251- 342.
19. Pulsoni D., Freire A., Ferreira D.R. Juvenile-onset ischaemic dermatopathy in two dogs treated with oclacitinib (abstract)/Vet Dermatol. 2018; 29: 371.
20. Rossi M.A., Messinger L.M., Linder K.E., Olivry T. Generalized canine discoid lupus erythematosus responsive to tetracycline and niacinamide therapy/J Am Anim Hosp Assoc. 2015; 51:171–5.
21. Scott D.W., Miller W.H., Griffin C.E., eds. Muller and Kirk’s Small Animal Dermatology, 6th ed. Philadelphia: WB Saunders (2000).
22. Scott D.W., Walton D.K. Canine lupus erythematosus. Systemic lupus erythematosus. /J Am Anim Hosp Assoc. 1983;19: 462–79.
23. White S.D., Rosychuk R.A.W., Reinke S.I. et al. Use of tetracycline and niacinamide for treatment of autoimmune skin disease in 31 dogs / J Am Vet Med Assoc. 1992; 200: 1497–1500.


Назад в раздел


















