Патогенез и новые методы диагностики астмы лошадей/Pathogenesis and new methods for diagnosis of equine asthma
Автор (ы): Ковач М., Алиев Р.У., Ипполитова Т.В., Иванятов Е.Ю., Дракул Н., Высоцкая С.
Организация(и): Ветеринарная клиника «Новый Век», филиал Московской государственной академии ветеринарной медицины и биотехнологии им. К.И. Скрябина
Аннотация
В течение 2008-2020 гг. в ветеринарной клинике «Новый Век» было диагностировано и подвергнуто лечению 890 лошадей с хроническим обструктивным бронхитом, который по новой номенклатуре называется «астма лошадей». В данной обзорной статье описаны новые аспекты причин, механизмы развития болезни и новые методы диагностики.
Summary
At a veterinary clinic «New Century» from 2008 to 2020 were diagnosed and treated 890 horses with equine asthma. This review article describes new aspects of the pathogenesis as well as new methods for diagnosis of the equine asthma.
Ключевые слова: лошадь, астма, патогенез, диагностические методы
Кey words: equine asthma, pathogenesis, diagnostic methods
Введение
Самое частое заболевание лошадей – это хроническое несептическое воспаление нижних дыхательных путей, которое решением 6-го всемирного симпозиума по болезням дыхательной системы лошадей (2017 г.) стало называться «астма лошадей» (2,17). В среднем 20% лошадей северного полушария, в том числе и в России, страдают от этого заболевания (31). В неблагополучных конюшнях в больших промышленных городах заболеваемость достигает 50%.
Термин астма (греч.: «затрудненное дыхание») был впервые использован в сборнике сочинений древнегреческого философа «Корпусу Гиппократа». В последние 30 лет использовались многочисленные названия, описывающие этот синдром у лошадей. Как например: рецидивирующая обструкция дыхательных путей (англ.: RAO), хроническая обструктивная болезнь легких у лошадей (ХОБЛ, англ.: COPD), воспалительное заболевание нижних дыхательных путей (англ.: IAD), хронический обструктивный бронхит и бронхиолит (ХОБ), хроническая обструктивная болезнь легких, связанная с летними пастбищами (англ.: SPA-RAO) и запал или эмфизема легких (англ.: heaves) (18).
Существует множество клинических признаков, попадающих под термин «астма лошадей», которые зависят от этиологии и патогенеза, тяжести и осложнений заболевания. Астма лошадей – это прогрессирующее хроническое заболевание, которое обычно ухудшается со временем. При астме происходит хроническая гиперчувствительность бронхиальной системы на различные аллергические и не аллергические факторы, которые приводят к приступам одышки, хрипам и кашлю из-за сужения дыхательных путей (23). Это сужение дыхательных путей вызывается отеком слизистой оболочки, утолщением стенки бронхов, секрецией слизи и спазмом бронхиальных мышц, нейтрофильным притоком, а также изменением гистологической структуры (ремоделированием) дыхательных путей. В зависимости от тяжести клинических признаков часто рекомендуется дифференцирование термина «астма» на легкую, среднюю и тяжелую степени. Легкая степень астмы, аналогично симптомам, ранее упомянутая под термином – воспалительные заболевания нижних дыхательных путей (IAD), а тяжелая степень астмы, аналогично термину, рецидивирующая обструкция дыхательных путей (RAO), соответственно (18).
Этиопатогенез астмы лошади
Механизм зарождения и развития астмы лошадей не до конца изучен. Это не прямолинейный путь развития, а сложная сеть взаимодействия многочисленных внутренних факторов (генетические, иммунологические, нервно-эндокринные, гематологические и респираторные расстройства) с внешними условиями содержания животного, т.е. с этиологическими факторами (кормление, движение и физическая активность животного, микроклимат и гигиена конюшни, температура, влажность и остальные климатические факторы) (31). При этом инфекционные агенты (бактерии, вирусы, грибы), которые в небольшом количестве постоянно присутствуют в дыхательных путях лошади играют небольшую роль в патогенезе астмы лошади. Чаще всего микробы играют роль в самой начальной фазе астмы или как осложнение уже существующего заболевания (вторичная инфекция).
Для лучшего понимания патогенеза астмы лошадей необходимо рассмотреть физиологические процессы, которые происходят в дыхательных путях. Как известно, в защите от микробов и частиц, которые попадают в дыхательную систему лошади, наряду с кашлевым рефлексом важную роль играет мукоцилиарный клиренс или механизм самоочищения дыхательных путей. При дыхании лошади огромное количество воздуха (и все, что находится в воздухе) «фильтруется» в дыхательных путях. Через дыхательную систему лошади в норме за сутки проходит 50 000 – 100 000 литров воздуха, что указывает на большую «физиологическую нагрузку» мукоцилиарной системы, особенно у лошадей, которые живут в неблагоприятных условиях (25). Эффективность мукоцилиарного клиренса лошади зависит от скорости секреции, от свойств слизи на поверхности дыхательных путей и от количества и качества ресничек мерцательного эпителия, присутствующих в слизистой оболочке дыхательных путей.
В составе слизистого эпителия бронха и бронхиол лошади, как хорошо известно, кроме реснитчатых клеток, содержатся бокаловидные клетки, щёточные (каёмчатые), М-клетки, микроворсинчатые клетки, базальные клетки и секреторные клетки Клара, а также антиген-представляющие клетки Лангерганса (дендритные клетки) и нейроэндокриноциты. Реснитчатые клетки, помимо подвижных ресничек, имеют разнообразные рецепторы для глюкокортикоидов, гистамина, адреналина и др. Эти клетки участвуют и в синтезе бронхо- и вазоконстрикторов (эндотелин) и их антагонистов бронхо- и вазодилататоров (закись азота, простагландин Е2) (23). В реснитчатых клетках вырабатываются биологически активные вещества – цитокины и факторы роста, такие как фактор роста фибробластов, тромбоцитарный фактор (усиливает пролиферацию гладких мышц), IL-1 и IL-6 (активируют Т-лимфоциты), IL-8 (определяет хемотаксис эозинофилов крови). Синтез этих факторов роста усиливается под влиянием цитокинов, выделяемых макрофагами после их взаимодействия с антигенами (аллергенами), содержащимися во вдыхаемом воздухе. Важную роль в патогенезе астмы лошадей имеет и нарушение функции клеток Клара. Клетки Клара являются куполообразными клетками с короткими микроворсинками, с выраженной способностью секреции слизи, схожей по составу с легочным сурфактантом, который уменьшает поверхностное натяжение, позволяя бронхиолам расширяться во время вдоха и предотвращая разрушение бронхиол во время выдоха. Клетки Клара производят дополнительно гликозаминогликаны, ферменты и секретоглобулиновый белок, лизоцим, антитела IgA, которые важны в иммунной защите дыхательных путей лошади.
Начальный запуск аллергической астмы, как у людей, так и у лошадей, возникает в результате не только нарушения мукоцилиарного клиренса реснитчатых клеток, но и клеток Клара (31). Причины нарушения мукоцилиарного клиренса могут быть разные. Чаще всего виной этому субклинические вирусные заболевания лошадей (грипп, герпесвирус (EHV-1, EHV-4), аденовирус лошадей -1. Эти вирусные заболевания вызывают у большинства лошадей нарушение функции мукоцилиарного клиренса (25). У лошадей, которые имеют недостаточное движение (главным образом при конюшенном содержании, без выпаса), адренергическая система физиологически подавлена, микоцилиарный клиренс выраженно снижается, таким образом, проблема усиливается. Нарушение мукоцилиарного клиренса и клеток Клара может провоцировать проникновение разных патогенов (микробов) и органических веществ (аллергенов) глубже в слизистую оболочку бронха и бронхиол лошадей, которые запускают механизм развития аллергической реакции. Существуют многочисленные пищевые и непищевые аллергены, кроме пыли, которые приводят к аллергической астме лошадей (21, 24). Аллергия, которая сопровождает астму лошадей, возникает главным образом в ответ на различные бактериальные споры и плесневые грибки (Micropolyspora faeni, Thermoactinomyces vulgaris, Saccharopolyspora rectivirgula, Aspergillus fumigatus), эндотоксины (часть стенки разложенных грамотрицательных бактерий), которые находятся в сене, подстилке или стенах денника (6). Аллергия также часто возникает на аммиак в конюшне, бета-D-глюкан, ультрадисперсные частицы (диаметром менее 100 нм), пылевые частицы растений и на остатки пылевых клещей (Dermatophagoides farinae, Dermatophagoides pteronyssinus) (31). Очень частая причина аллергической реакции дыхательной системы лошади – кормление сеном плохого качества, где находится большое количество скатола (3-метилиндол), который образуется при разложении аминокислот триптофана растений. По этой причине лошади, которые весь день проводят в конюшне и только 1 час на прогулке, при этом питаясь в основном сеном, болеют астмой почти в 50 раз чаще, чем лошади, живущие на свободе, питающиеся свежей травой и находящиеся в постоянном движении (25). Большинство лошадей конюшенного содержания постоянно находятся в запыленных помещениях, особенно если вентиляция в них недостаточна для соблюдения зоогигиенических норм, а также всегда показывают более выраженную парасимпатическую активность вегетативной нервной системы, которая кроме прочего вызывает бронхоспазм и уменьшает активность мукоцилиарного клиренса. У лошадей в конюшенных условиях содержания чаще всего происходит вторичная бактериальная инфекция бронхиальной системы. Аллергия, как известно, возникает на органические вещества, но аллергическая астма лошадей может возникнуть на неорганические вещества, который выбрасываются в атмосферу при сгорании углеводорода (бензин, газ, уголь). По большой вероятности, эти неорганические вещества связываются органическими молекулами и вместе провоцируют запуск аллергической реакции.
При аллергической реакции дыхательной системы лошадей главную роль имеет бронхо-ассоциированная лимфоидная ткань (БАЛТ-система). При астме лошадей протекает классический 1-й и частично 3-й тип аллергической реакции дыхательных путей (21). Механизм развития аллергической реакции 1-го типа полностью соответствует классическим канонам иммунного ответа. Ключевые события, которые приводят к возникновению аллергии следующие. Сначала один из выше перечисленных аллергенов через воздух поступает в дыхательные пути. Дендритная клетка стенки бронха и бронхиол захватывает (фагоцитирует) молекулу аллергена и через сложный путь внутриклеточной обработки (англ.: processing) представляет антигенную детерминанту аллергена (эпитоп) через рецептор главного комплекса гистосовместимости (MHC II) на своей поверхности, который показывает чужеродность иммунной системе проникающего аллергена (рис.1-1). Затем активированная антиген-презентирующая дендритная клетка мигрирует в ближайший лимфатический узел БАЛТ-системы. Здесь дендритная клетка активирует недифференцированную Т-лимфоцитную клетку, которая распознает аллерген и превращается в Т2-хелперные клетки (Th2-клетка) (рис.1-2). B-лимфоциты (B-клетки), также распознают аллергены (рис.1-3), которые активируются и дифференцируются либо в В-клетки иммунной «памяти», либо в плазматические клетки, после чего они активно синтезируют антитела изотипа IgE, специфичного для распознавания этого аллергена (рис.1-4). Активацию B-клетки стимулируют Th2-клетка через продукцию цитокинов, как например IL-4 и IL-10. Эту реакцию угнетают γ-интерферон и IL-2, выделяемые Тh1-клетками. Считается, что одной из причин астмы лошади является нарушение отношения Тh1- и Тh2 клетки (3). Специфичные антитела IgE, которые теперь распознают эпитопы молекулы аллергена, циркулируют по всему организму лошади и связываются со своим рецептором Fc RI на тучных и базофильных клетках. Когда аллерген при повторной встрече вновь попадает в организм через дыхательную систему, он связывается с IgE, который находится на поверхности этих клеток и заставляет клетки высвобождать многочисленные медиаторы аллергической реакции при астме (рис.1-5). Существует и множество не аллергенных стимулов, которые могут вызвать эту активацию тучных и базофильных клеток, включая протеазы, цитокины и лиганды Toll-подобного рецептора. Из гранул тучных и базофильных клеток выбрасываются биологически активные медиаторы: вазоактивные амины (гистамин), протеогликаны (гепарин), липидные медиаторы (лейкотриены, простагландины, тромбоцит-активирующий фактор), ферменты (триптаза, химаза, карбоксипептидаза, катепсин G) и цитокины (TNF-α, IL-3, IL-4, IL-5, IL-13, GM-CSF), которые вызывают характерные симптомы аллергического воспаления дыхательных путей (вазодилатация, слизистая секреция, отек, спазм гладкой мускулатуры бронхов) (23). При этой форме аллергической реакции симптомы проявляются уже через 20-30 мин после повторной встречи с аллергеном (31). Хронический стресс может усугубить это аллергическое состояние, обусловленное подавлением интерлейкина-12, как вегетативной нервной системой, так и осью гипоталамус-гипофиз-надпочечника.
После того как медиаторы острого ответа стихают, часто могут возникать реакции поздней фазы, т.е. гиперчувствительного ответа типа 3, возникающего в результате образования комплекса антигенных антител и последующей активации каскада комплемента с высвобождением анафилатоксиновых пептидов C3a и C5a (16). В этой, более поздней аллергической фазе, которая появляется через 6–24 часов после исходной реакции, различные хемотаксические факторы привлекают в бронхи лошади нейтрофильные гранулоциты (рис.1-6). У человека при этом привлекаются эозинофилы и макрофаги. Это ключевая разница между астмой лошади и человека. Нейтрофильный наплыв в бронхах лошадей, по нашему наблюдению, вызывается частично высоким числом сапрофитных бактерий. Нейтрофилы, при астме лошадей, имеют замедленный спонтанный апоптоз и высвобождают эластазу, метаболиты кислорода, лейкотриен – LTB4, матриксную металлопротеиназу 9, нейтрофильную эластазу, катепсин G. протеиназу-3, IL-1b, IL-8 и IL-17 и фактор некроза опухоли (TNF) (21).
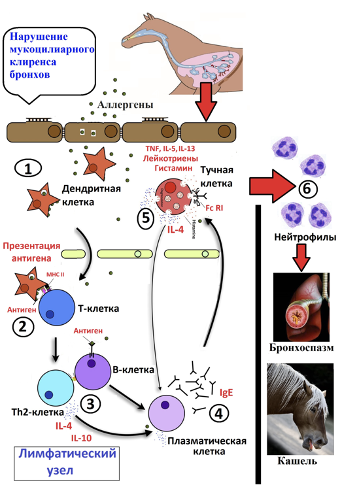
Рис. 1. Упрощенная схема патогенеза астмы лошадей (под фаза 1-6)
Макрофаги обнаруживаются в крупных и мелких бронхах, паренхиме легких, а также в местах деструкции альвеолярной стенки, как при развитии самой тяжёлой фазы астмы –эмфиземы. Макрофаги выделяют TNF -α, IL-8, IL-4, ЛТВ4, что способствует хемотаксису нейтрофилов. В стенке бронхиол повышается накапливание Т-лимфоцитов, которые выделяют перфорин гранзим-B и TNF-α, которые вызывают цитолиз и апоптоз альвеолярных эпителиоцитов. Количество клеток мерцательного эпителия в бронхиолах уменьшается, а клетки, секретирующие слизь, количественно увеличиваются и подвергаются гиперплазии. Возникает выражение утолщение стенок бронхов. Происходит нарушение регуляции эпителиоцитами функционирования молекул адгезии E-селектина. Эпителиальные клетки бронхов при астме лошадей показывают повышенную экспрессию транскрипционных факторов, способных усиливать иммунологический ответ (NF-K, AP-1 и CREB) (5).
Бронхоспазм является ключевой особенностью астмы лошадей. Как известно из физиологии, тонус гладких мышц дыхательных путей лошади контролируется вегетативной нервной системой как центрально, так и через локальный аксонный рефлекс, посредством активации рецепторов циркулирующих катехоламинов и неадренергических нехолинергических механизмов (NANC-систем). Бронхоспазм в астме опосредуется мускариновыми рецепторами ацетилхолина парасимпатической нервной системы блуждающего нерва (1). Кроме того, бронхорелаксация также нарушена из-за снижения плотности β-адренергических рецепторов и эффективности связывания с G-белком, а также измененного ответа NANC-систем. В частности, имеются исследования роли нейропептидного рецептора нейрокинина А на уровне гладких мышц дыхательных путей, усиливающего его бронхоконстриктивные эффекты (29). Другие медиаторы также находятся в фазе бронхоспазма, включая серотонин, эндотелин-1, гистамин и лейкотриен D4. При астме лошадей присоединяющаяся сапрофитная инфекция (бактерии и грибы) дыхательных путей приводит к усилению стеноза (6, 23).
Конечный исход всего этого – значительное нарушение обмена газа в легких (снижение концентрации кислорода и повышение концентрации углекислого газа в артериальной крови). Кислородное «голодание» мышечной ткани вызывает нарушение работоспособности лошади. По нашим исследованиям, в поздней фазе астмы отмечается легочное сосудистое сопротивление, что приводит к повышению нагрузки и гипертрофии правого желудочка (легочное сердце) (14). В тяжелой фазе астмы, через активный «мышечный» процесс вдоха, воздух успевает достичь поверхности альвеола, но во время пассивного выдоха, наблюдается неспособность легких эвакуировать весь воздух из альвеол. Это может привести к тому, что большая часть воздуха из предыдущего акта вдоха останется в легких при запуске следующего вдоха, что приведет к увеличению общего объема воздуха в легких в любой момент времени (увеличится так называемое «мертвое пространство»). Таким образом, происходит растяжение и повышение давления в альвеолах и респираторных бронхиолах, как и тотальная емкость легких. Увеличение объема альвеолярного мертвого пространства легко определяется по снижению концентрации СО2 в выдыхаемом воздухе по сравнению с артериальной кровью (РаСО2). Альвеолярные стенки не могут противостоять давлению воздуха и растягиваются, что обусловливает преждевременное закрытие бронхиол, т.е. стенки бронхиол играют роль клапана («клапанный механизм»), который во время выдоха закрывается и воздух оказывается пойманным, как в ловушке, в альвеолах. Это временно приводит к разрыву меж-альвеолярных перегородок или к деструктивно-морфологическим необратимым изменениям альвеолярных стенок и нарушении перфузии легких. Эта фаза называется эмфизема легких. В конечном исходе уменьшается объем альвеолярной вентиляции с развитием необратимой дыхательной недостаточности животного. У этих лошадей отмечается дополнительные системные проявления: потеря мышечной массы и биоэнергетические расстройства.
Существует и генетическая предрасположенность к возникновению астмы лошадей, примерно в 20% случаев (8, 10). На 13-й хромосоме лошади существует ген IL4Rα, связанный с развитием астмы, кожных аллергий и защиты от паразитов (22). Интересно, что лошади с астмой имеют меньшую зараженность яйцами стронгилидного типа по сравнению со здоровыми лошадьми (8). Причиной этого является то, что некоторые кишечные паразиты выделяют химические вещества, которые подавляют иммунную систему и предотвращают аллергическую реакцию дыхательной системы лошади. Как следует из этой гипотезы, регулярное использование современных антигельминтиков и снижение воздействия паразитов может увеличить риск развития у лошадей астмы и других аллергических заболеваний.
Симптомы и диагностика астмы лошадей
В период с 2008 по 2020 гг. в ветеринарной клинике «Новый Век» было диагностировано и находилось на лечении 890 лошадей с диагнозом «хронический обструктивный бронхит» (или по новой номенклатуре – «астма лошадей»). Возникновение астмы, по нашим наблюдениям, не зависит от породы и пола лошадей. Чаще всего с астмой встречаются лошади старше 9 лет.
Существуют многочисленные методы, которые могут использоваться в постановке диагноза – астма лошадей. В медицине лошадей недавно появилась анкета для сбора анамнестических сведений для оценки рисков развития и существования астмы лошадей (англ.: risk-screening questionnaire, RSQ), которая даёт полезный инструмент для изучения этого эпидемиологического заболевания у лошадей (13, 30). В этом анкетном опросном листе учитывается не только форма дыхания, частота, длина и рецидив кашля и носового выделения у лошадей, а также условия содержания лошадей (конюшенное или свободный выпас) и, особенно, кормление (сено или трава). Вероятность того, что у лошади есть астма, рассчитывается по завершению анкетного вопроса, путем объединения соответствующих оценочных вероятностей (очковая балловая система). Полученные данные анамнеза в постановке предварительного диагноза показались надёжными, как результат, были проверены и подтверждены в соответствии с другими стандартными диагностическими процедурами.
У большинства лошадей сначала проявляются незначительные клинические признаки: хронический (> 3 недель) периодический сухой кашель. Считается, что рецидив кашля длительный период времени – это один из основных симптомов наличия астмы лошадей. Кашель – это очень частый, но не обязательный симптом астмы лошадей. По нашим наблюдениям, примерно 5-10% лошадей с легкой формой астмы не показывают кашель. Также не любой кашель лошадей (особенно острый кашель у молодых лошадей и жеребят) указывает на астму. Другие характерные симптомы астмы лошадей: непереносимость физической нагрузки, усиленное, свистящее дыхание, хрипы с тахипноэ (учащённое поверхностное дыхание свыше 20 раз в минуту) и раздувание ноздрей на вдохе. Признаки и серьезность могут меняться со временем, часто ограничивая активность и желание животного работать. Со временем, при тяжёлой степени астмы, из-за мышечной гипертрофии, от усилия, необходимого для выдоха, вдоль нижнего края ребер может развиваться «запальный желоб». Серозные или слизисто-гнойные двухсторонние выделения из носа встречаются чаще всего при выраженном бактериальном обострении астмы лошади. Повышение температуры встречается также только при выраженном вторичном бактериальном воспалении.
Самая частая диагностическая процедура, которую мы применяли – это комбинация газового анализа артериальной крови и проведение трахеальной эндоскопии. Дополнительные диагностические тесты – это проведение цитологии бронхоальвеолярного лаважа (БАЛ), рентгенологического и ультразвукового обследования, сцинтиграфическое исследование, пневмография, измерение внутриплеврального давления до и после физической нагрузки и проведение функционального анализа легких (спирометрия, капнография, плетизмография, флоуметрическая плетизмография с гистаминовой бронхопровокацией) (4,5,7,11,15).
Газовый анализ артериальной крови проводится забором крови с длинной иглой (14-16 цм) из общей сонной артерии (рис.2) с определением парциального давления кислорода (PaO2) и углекислого газа (PaCO2) в фазе покоя и сразу после 10 минут физической нагрузки.
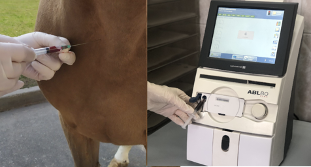
Рис.2. Забор и газовый анализ крови
По нашему мнению, и, по мнению немецких ветеринарных врачей, – это золотой стандарт в диагностике наличия астмы у лошадей. Этот метод помогает определить и степень заболевания. В норме у здоровых лошадей в фазе покоя PaO2 составляет примерно 100 ± 5 мм рт. столба, а PaCO2 40 ± 5 мм рт. столба. Сразу после 10 минут физической нагрузки у этих лошадей PaO2 увеличивается на 5-10 мм рт. столба. В зависимости от уменьшения PaO2 принята классификация астмы лошадей на 5 стадий (9):
I. Стадия (легкая степень) – парциальное давление кислорода (PaO2) от 90-95 мм рт. столба
II. Стадия (средняя степень) – парциальное давление кислорода (PaO2) от 80-90 мм рт. столба
III. Стадия (тяжелая степень) – парциальное давление кислорода (PaO2) от 70-80 мм рт. столба
IV. Стадия (крайне-тяжелая степень) – парциальное давление кислорода (PaO2) от 60-70 мм рт. столба
V. Стадия (эмфизематозная степень заболевания) – парциальное давление кислорода(PaO2) от 60 -50 мм рт. столба.
При астме лошадей парциальное давление кислорода после физической нагрузки ещё больше уменьшается, чем в фазе покоя. При других бактериальных заболеваниях легких и бронхов лошадей парциальное давление кислорода после физической нагрузки увеличивается.
Парциальное давление кислорода в артериальной крови лошади зависит не только от функционального состояния альвеол легких, но и от атмосферного давления и высоты над уровнем моря, где проводится это исследование. При астме лошадей проводится часто и измерение альвеолярно-артериального градиента кислорода (AaDO2), т.е. разница между альвеолярной (рAO2) и артериальной концентрацией кислорода (PaO2), где учитываются эти параметры, по формуле:
AaDO2 = рAO2 (мм рт. столба) - PaO2 (мм рт. столба)
При этом парциальное напряжение О2 в альвеолярном воздухе можно измерить на основе уравнения, основанного на том, что рAО2 и рAСО2 изменяются обратно пропорционально друг другу в зависимости от объема альвеолярной вентиляции (при гипервентиляции РAО2 повышается, а РAСО2 снижается, а при гиповентиляции – наоборот). Уравнение альвеолярного газа применяют в упрощенном виде, а вместо РAСО2 подставляют РаСО2, по формуле:
РAО2 = F1O2 х (Рв - PH2O) - (РAСО2 : ДК)
Рв – атмосферное давление (на уровне моря - 760 мм рт. ст.);
PH2O – давление насыщенного водяного пара (при 37оС - 47 мм рт. ст.);
ДК – дыхательный коэффициент (отношение выделенного СО2 к поглощенному О2, в среднем равен 0,8).
F1O2 – для атмосферного воздуха приблизительно равна 21%.
В норме у здоровых лошадей алвеолярно-артериальная кислородная разница (AaDO2) < 1,35, при тяжелой астме лошадей более 2,22.
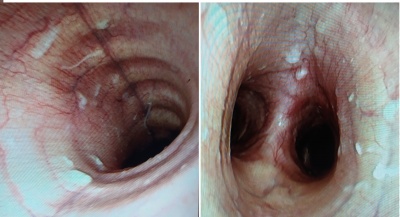
При проведении трахеальной эндоскопии обращают внимание на количество и вязкость слизи, а также на утолщение бифуркации трахеи (рис. 3). Количество и вязкость слизи оценивается по шкале 0-5 (25). У здоровых лошадей либо нет видимой слизи, либо только несколько изолированных пятен (степень 1). Чаще всего при классической форме астмы вязкость слизи увеличена («клеится» на стенку трахеи), количество слизи не переходит 3-й класс и отмечается утолщение бифуркации трахеи. Большое количество более жидкой слизи указывает на выраженное бактериальное обострение астмы или острое бактериальное воспаление бронхов и легких.
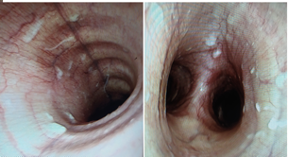
Рис.3. Наличие слизи и утолщение бифуркации трахеи у лошади с астмой
В англоязычной литературе для постановки диагноза астмы лошадей очень часто рекомендуется проведение цитологии бронхоальвеолярного лаважа (БАЛ) (5,15). Бронхоальвеолярный лаваж – это диагностическая процедура, предполагающая введение 250-500 мл 0,9% физиологического раствора в трахею и бронхи лошади с последующим его удалением и цитологическим исследованием полученного субстрата (слизи). Эту диагностическую процедуру мы применяем редко по нескольким причинам: данная процедура достаточно опасна для лошадей, для получения результата необходимо ждать длительное время, а также процентное отношение клеток субстрата часто подвергается изменчивости у астматичных лошадей и не всегда возможно определить степень тяжести заболевания. У лошадей, страдающих астмой, обычно в бронхиальной слизи преобладают нейтрофилы, за которыми следуют лимфоциты, макрофаги и тучные клетки (таблица 1). Другие цитологические находки также указывают на астму лошадей, такие как спирали Куршмана, кристаллы Шарко-Лейдена (продукт кристаллизации эозинофильных гранулоцитов) и пенистые альвеолярные макрофаги (рис. 4).
Таблица 1. Клетки бронхиальной слизи при астме лошадей
|
Клетки бронхиальной слизи |
Лошади с астмой |
Здоровые лошади |
|
Нейтрофильные Гранулоциты (%) |
5-92 |
3-26 |
|
Лимфоциты (%) |
3-80 |
40-70 |
|
Макрофаги (%) |
2-38 |
19-50 |
|
Тучные клетки (%) |
0-3 |
0-6 |
|
Эозинофильные гранулоциты (%) |
0 |
0-6 |
|
Эпителиальные клетки (%) |
0-51 |
0 |
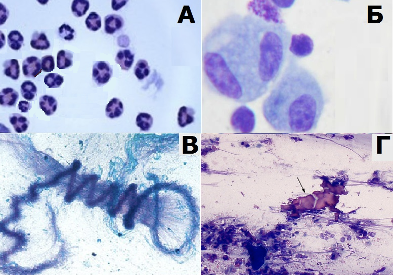
Рис.4. Цитологические находки у лошади с астмой: нейтрофильные гранулоциты (А), пенистые альвеолярные макрофаги (Б), спирали Куршмана (В) и кристаллы Шарко-Лейдена (Г)
Другие процедуры при диагностике астмы лошадей редко применяются по разным причинам. Гематологические и биохимические изменения редко встречается, за исключением лёгкой степени относительного нейтрофильного лейкоцитоза. Повышение концентрации эозинофильних и базофильних гранулоцитов, IgE в крови или трахеобронхиальной слизи не всегда отмечается при астме лошадей (20). Лошади с астмой имеют тенденцию проявлять ослабленные физиологические реакции на физическую нагрузку по сравнению со здоровыми лошадьми, о чем свидетельствует более высокая концентрация молочной кислоты (лактата) в крови при физической нагрузке.
Различные сывороточные белки (биомаркеры) были исследованы у лошадей с астмой (16). Сывороточная концентрация сурфактантного белка D (SP‑D) у лошадей с легкой степенью астмы была значительно выше, чем у контрольных лошадей, как в покое, так и после физических нагрузок. Однако не было обнаружено значительной корреляции между концентрациями SP-D в сыворотке и цитологических изменений бронхиальной слизи у лошадей с астмой. Сывороточные белки острой фазы, такие как сывороточный амилоид А, С-реактивным белком и гаптоглобином, незначительно изменяются у лошадей с астмой. По нашим предварительным результатам концентрация ИЛ-1 и TNF-α у лошадей с астмой встречается только при тяжёлой форме заболевания, чаще всего у животных старше 15 лет, которые имеют и другие сопутствующие заболевания.
Аллергологическое исследование наличия специфичных сывороточных антител у лошади с аллергией (в том числе и у лошадей с астмой) возможно сделать только на следующие аллергены: различные типы клещей (D.farinae D.pteronyssinus Lepidoglyphus destructor, Acarus siro, Tyrophagus), грибов (Asp.fumigatus/Pen.notatum, Micropolyspora faeni/Thermoactinomyces), амброзию, пыльцу берёзы/ольхи/ореха, платана/ивы/тополя, ржи, смеси из шести трав, подорожника, полынь, рапса, слепены, мокрецы, комаров, мошку и овода (27).
Биопсия и гистологическое исследование стенок бронхов лошади применяется редко по причине инвазивности процедуры (возможности кровотечения). При этом замечается перибронхиолярная инфильтрация воспалительных клеток и бронхиолярная гиперплазия гладких мышц, а также метаплазия клеток бронхиолярного эпителия, скопления нейтрофилов и перибронхиолярных лимфоцитов и плазмоцитов (25). Рентгенография является еще одним диагностическим методом, который подтверждает диагноз (рис.5), но чувствительность рентгенографии (как и ультразвукового исследования) слишком низка (26,31).
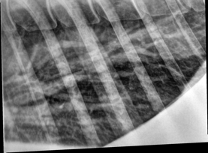
Рис.5. Рентгенологический снимок лёгких лошади с астмой
Измерение внутриплеврального давления (∆Ppl) – достаточно надёжный метод, для которого необходимо специальное оборудование. Внутриплевральное давление у больных астмой лошадей в среднем 33 cm H2O (диапазон 23–58), в то время как у здоровых лошадей в среднем 4 cm H2O (диапазон 1-9) (23).
Функциональные тесты для анализа вентиляции легких лошадей дают надежное данные для выявления обструкции дыхательных путей, но возможно сделать только на специальным дорогостоящем оборудовании и только в нескольких клиниках мира (12). Чаще всего приминается спирометрия для исследования функции внешнего дыхания, в которую входит измерение жизненного объема легких, дыхательного объёма, а также скоростных показателей дыхания. Главным образом выполняются следующие виды спирометрических проб: при спокойном дыхании и функциональные провокационные пробы (с гистамином). Измерением функции легких во время бронхопровокации гистамина могут обнаружить субклиническую обструкцию дыхательных путей при астме лошадей (рис.6). У лошади с астмой даже небольшое количество гистамина (8 мг) вызывает резкое увеличение сопротивления дыхательных путей. Исследование спирометрии резервного объёма вдоха или форсированного и резервного выдоха невозможно выполнить в полном объеме. Техника принудительного выдоха у лошадей требует сильного седативного воздействия, назотрахеальной интубации, искусственной вентиляции легких и применения вакуума. Тем не менее она обнаруживает раннее начало легочной дисфункции при астме лошадей. Недавно появилась возможность у лошадей сделать измерение сопротивления дыхательных путей посредствам импульсной осциллометрии (28). Также недавно появилась возможность измерения альвеолярного давления, остаточного и общего объема воздуха в легких посредствам плетизмографии (19). Пневмотахографическим исследованием можно у астматичных лошадей определить повышенное сопротивление дыхательных путей и пониженную динамическую податливость (англ.: dynamic compliance), через непрерывную графическую регистрацию объема скорости потока вдыхаемого и выдыхаемого воздуха (23). Эти стандартные измерения дыхательной механики очень полезны для определения различий между здоровыми и больными лошадями.
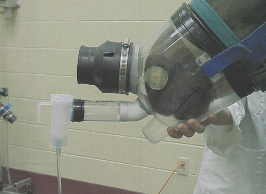
Рис.6. Спирометрическое исследование лошади во время бронхопровокации гистамином
При изучении патологических изменений в легких у лошадей дополнительную информацию можно получить при проведении вентиляционно-перфузионной пульмоносцинтиграфии, поскольку такое исследование характеризует состояние капиллярного русла кровотока и вентиляцию легких, что важно для диагностики функциональных нарушений при заболеваниях респираторной системы, в частности астмы (рис.7).
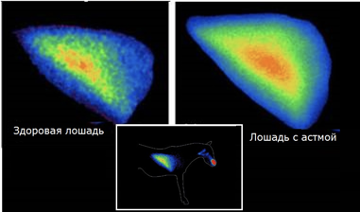
Рис.7. Сцинтиграфическое исследование лошади
Литература
1.Abraham, G., Kottke, C. and Ungemach, F.R.: Equine recurrent airway obstruction does not alter airway muscarinic acetylcholine receptor expression and subtype distribution. J. Vet. Pharmacol. Ther. 30, 401-409, 2007.
2.Bond S., Leguillette R., et al.: Equine asthma: Integrative biologic relevance of a recently proposed nomenclature. J Vet Intern Med. 32(6): 2088–2098. 2018.
3.Bullone M, Lavoie JP.: Review Asthma “of horses and men”—How can equine heaves help us better understand human asthma immunopathology and its functional consequences? Mol Immunol. 66(1):97-105, 2015.
4.Costa, L. R. R., Seahorn, T. L.et al.: Correlation of clinical score, intrapleural pressure, cytologic findings of bronchoalveolar fluid, and histopathologic lesions of pulmonary tissue in horses with summer pasture-associated obstructive pulmonary disease. American Journal of Veterinary Research, 61(2), 167–173. 2000.
5.Couetil LL, Thompson CA.: Airway Diagnostics: Bronchoalveolar Lavage, Tracheal Wash, and Pleural Fluid. Vet Clin North Am Equine Pract. 36(1):87-103, 2020.
6. Dauvillier J, Ter Woort F.: Fungi in respiratory samples of horses with inflammatory airway disease. J Vet Intern Med. 33(2):968-975, 2019.
7.Gerber, V., R. Straub, E. Marti J. et al.: Endoscopic scoring of mucus quantity and quality: observer and horse variance and relationship to inflammation, mucus viscoelasticity and volume. Equine Vet. J. 36:576–582. 2004.
8.Gerber, V., Swinburne, J.E. et al.: Genetics of recurrent airway obstruction (RAO). Deut. Tierarztl. Wochensch. 115, 271-275, 2008.
9.Grabner, A.: Arterielle Blutgasanalyse. in W. Kraft. Klinische Labordiagnostik in der Tiermedizin. 429–30. Schattauer, Stuttgart. 2005.
10.Graubner, C., Drogemuller, M.: RAO- are genes to blame? Tieraerztl. Umschau. 67, 471-473, 2012.
11.Herholz, C.P., Gerber, V.: Use of volumetric capnography to identify pulmonary dysfunction in horses with and without clinically apparent recurrent airway obstruction. Am. J. Vet. Res. 64, 338-345, 2003.
12.Hoffman, A.M., Oura, T.J.et al.: Plethysmographic comparison of breathing pattern in heaves versus experimental bronchoconstriction or hyperpnea in horses. J. Vet. Intern. Med. 21, 184-192, 2007.
13.Hotchkiss JW, Reid SW, Christley R.: Construction and validation of a risk-screening questionnaire for the investigation of recurrent airway obstruction in epidemiological studies of horse populations in Great Britain . Prev Vet Med. 75(1-2):8-21. 2006.
14. Kovac M, Scheidemann W, Tambur Z.: Electrocardiographic interval changes during hyperinfusion in COPD horses. Acta Veterinaria, 2000; 50(5-6): 275-80, 2000.
15.Kutasi, O., Balogh, N., Lajos, Z. et al.: Diagnostic approaches for the assessment of equine chronic pulmonary disorders. J. Equine Vet. Sci. 31, 400-410, 2011.
16.Lavoie-Lamoureux, A., Leclere, M. et al.: Markers of systemic inflammation in horses with heaves. J. Vet. Intern. Med. 26, 1419-1426, 2012.
17.Lavoie JP. Is the time primed for equine asthma? Equine Vet Educ. 27:225‐226, 2015.
18.Lavoie J‐P. Which is the most appropriate in 2017: "Mild to Severe Equine Asthma" or heaves, RAO, equine COPD, IAD, tracheal IAD, bronchial IAD, small airway disease, chronic bronchitis, SPACOPD, SPOPD, summer heaves or summer RAO? World Equine Airway Symposium. Vol 6 Copenhagen, Denmark; 2017.
19.Nolen-Walston, R.D., Kuehn, H., Boston et al.: Reproducibility of airway responsiveness in horses using flowmetric plethysmography and histamine bronchoprovocation. J. Vet. Intern. Med. 23, 631-635, 2009.
20.Marteles D, Odriozola L. et al.: Assessment of serum allergen-specific IgE levels in horses with seasonal allergic dermatitis and recurrent airway obstruction in Spain.Acta Vet Hung. 67(1):11-21, 2019.
21.Moran G.Folch H.: Recurrent airway obstruction in horses - An allergic inflammation: A review Veterinarní medicína. 56(1), 2011.
22.Neuhaus, S., Bruendler, P., Frey, C.F.: Increased parasite resistance and recurrent airway obstruction in horses of a high-prevalence family. J. Vet. Intern. Med. 24, 407-413, 2010.
23.Pirie RS.: Recurrent airway obstruction: a review. Equine Vet J. 46(3):276-88, 2014.
24.Pirie, R.S., Collie, D.D.S., Dixon, P.M. and McGorum, B.C.: Inhaled endotoxin and organic dust particulates have synergistic proinflammatory effects in equine heaves (organic dust-induced asthma). Clin. Exp. Allergy 33, 676-683, 2003.
25.Robinson, N.E., Jefcoat, A.M. and Gerber, V.: Mucus and inflammation in equine heaves. Pferdeheilkunde 18, 551-556, 2002.
26.Siwinska N, Zak A, Slowikowska M.: Prevalence and severity of ultrasonographic pulmonary findings in horses with asthma - a preliminary study. Pol J Vet Sci. 22(4):653-659, 2019.
27.Tahon, L., Baselgia, S., Gerber, V. et al.: In vitro allergy tests compared to intradermal testing in horses with recurrent airway obstruction. Vet. Immunol. Immunopathol. 127, 85-93, 2009.
28.Van Erck, E., Votion, D., Art, T. and Lekeux, P.: Qualitative and quantitative evaluation of equine respiratory mechanics by impulse oscillometry. Equine Vet. J. 38, 52-58, 2006.
29.Venugopal, C.S., Holmes, E.P. et al.: Neurokinin receptors in recurrent airway obstruction: a comparative study of affected and unaffected horses. Can. J. Vet. Res. 73, 25-33, 2009.
30.Wasko AJ, Barkema HW, Nicol J. et al. Evaluation of a risk‐screening questionnaire to detect equine lung inflammation: results of a large field study. Equine Vet J. 43:145‐152, 2011.
31.Wilson EM, Robinson E. Recurrent Airway Obstruction and Inflammatory Airway Disease. in Robinson's Current Therapy in Equine Medicine (Seventh Edition), 2015.

Назад в раздел

















