К вопросу применения иммунодепрессантов в ветеринарной дерматологии
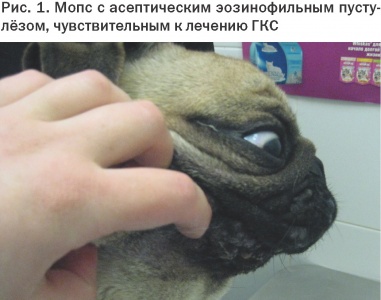
Еще фото
Автор (ы): А.Н. Герке, к.в.н., ветеринарный врач-дерматолог, член Европейского общества ветеринарных дерматологов (ESVD) / А. Gerke, DVM, PhD
Организация(и): ЗАО «Сеть ветеринарных клиник», Санкт-Петербург / «Network of veterinary clinics», St. Petersburg
Журнал: №5 - 2012
Ключевые слова: иммунодепрессанты, аутоиммунитет, цитостатики,
глюкокортикоиды
Сокращения
ГКС – глюкокортикостероиды
ИЛ – интерлейкин
П/О – перорально
В/М – внутримышечно
ПК – подкожно
Введение
Подавление иммунной реактивности может быть необходимым при лечении аллергических и иммунопатологических процессов (атопия, эозинофильный фурункулез, пемфигоидный комплекс, буллезный пемфигоид, системная красная волчанка и др.). Неспецифическое воздействие на иммунную систему осуществляют в следующих случаях:
- отсутствует возможность воздействия на ответ к конкретным антигенам: либо антиген не установлен, либо нет практической возможности специфического подавления реакции (устранение антигена, десенсибилизация и т.д.);
- предполагается, что имеет место общая гиперреактивность иммунной системы, способная обусловить развитие разных процессов независимо от характера антигена [8].
При проведении неспецифической супрессии следует стремиться найти препарат, наиболее эффективный в отношении тех. процессов (клеточных или гуморальных), которые вызвали данное заболевание. Класс иммуносупрессивных препаратов неоднороден и содержит препараты с разными механизмами действия и различным профилем побочных эффектов. Различается и профиль иммуносупрессивного эффекта: некоторые препараты более или менее равномерно подавляют все виды иммунитета, другие имеют особую избирательность по отношению к аутоиммунитету, при сравнительно меньшем влиянии на антибактериальный, противовирусный и противоопухолевый иммунитет. Примерами таких, относительно селективных, иммуносупрессоров являются тимодепрессин, циклоспорин А и такролимус.
По происхождению и строению иммуносупрессивные средства разделяют на глюкокортикойды, антиметаболиты, алкилирующие соединения, антибиотики, алкалоиды и др.
Глюкокортикоиды
Глюкокортикоиды являются факторами естественной реактивности иммунной системы, вызывают следующие фармакологические эффекты:
1. Противовоспалительный эффект: независимо от причины повреждения кортикостероиды неспецифично взаимодействуют со всеми компонентами воспалительного ответа (подавляющее действие на Т-эффекторы гиперчувствительности, на Т-хелперы, продукцию Ig-G-антител, фагоцитоз, подавлением продукции ИЛ-6 и ИЛ-1 в моноцитах и макрофагах). Они уменьшают дилятацию капилляров и экссудацию, подавляют миграцию лейкоцитов и фагоцитарную активность, уменьшают отложение фибрина и препятствуют образованию рубцовой ткани. Противовоспалительные дозы глюкокортикоидов вызывают лимфопению преимущественно за счет перехода большой доли лимфоцитов из кровотока в лимфоидную ткань [9].
2. Воздействие на иммунный ответ: в высоких дозах снижают выработку лимфоцитов и иммуноглобулинов, а также функцию моноцитов и макрофагов. Это приводит к нарушению иммунокомпетентности. Увеличение содержания нейтрофилов, эозинопения – эти эффекты связаны, преимущественно с нарушением миграции клеток.
3. Воздействие на углеводный и белковый метаболизм: стимулируют глюконеогенез, снижают утилизацию глюкозы в периферических тканях, что приводит к гипергликемии. Также отмечается параллельное усиление катаболизма белков с мобилизацией аминокислот из периферических тканей.
4. Водный и электролитный баланс: увеличение реабсорбции натрия и экскреции калия и ионов водорода. Гипернатриемия в редких случаях может стимулировать гипертензию у животных с сердечной недостаточностью.
5. Жировой обмен: перераспределение жира.
6. Повышение выработки соляной кислоты и пепсина в желудке [6, 8].
Исходя из широкого спектра фармакологических и физиологических реакций кортикостероидов, их побочные действия легко предсказуемы:
- метаболические эффекты (ожирение в области живота, мышечная слабость, проксимальная миопатия – преимущественно у собак; гипергликемия, глюкозурия – особенно у кошек; у собак изредка развивается сахарный диабет, требующий инсулинотерапии);
- ломкость капилляров;
- полиурия, полидипсия, атония мочевого пузыря (преимущественно у собак);
- остеопороз, кальциноз кожи спины, холки (у собак при длительной терапии);
- диспептические расстройства;
- повышенная восприимчивость к инфекциям.
Препараты этой группы весьма активны, но побочные эффекты (нарушение функции надпочечников, прогрессирование сахарного диабета, нарушения минерального обмена, плохое заживления ран и др.) обязывают к умеренному их назначению, при необходимости их применения дозу следует снижать как можно быстрее. Важно помнить, что экзогенное введение ГКС приводит к угнетению функции передней доли гипофиза с уменьшением высвобождения АКТГ, и, соответственно, угнетению коры надпочечников. После отмены стероидной терапии восстановление нормальной функции надпочечников может занимать до 6 месяцев. Режим применения ГКС через день вызывает меньшее угнетение функции надпочечников. Краткосрочную терапию можно прекратить быстро без особых трудностей, длительная терапия (более 4 недель) требует постепенной отмены в течение нескольких недель [5, 6].
Приблизительные дозы препаратов группы ГКС приведены в таблице, в скобках приведена дозировка для пульстерапии. Автор предпочитает использовать преднизолон, потому что его побочные и терапевтические эффекты проще отслеживать, чем пролонгированные препараты этой группы. Животные с атопическим дерматитом, как правило, хорошо отвечают на лечение ГКС. В противовоспалительных дозах эти препараты подавляют множество генов, ответственных за производство цитокинов, хемокинов и адгезивных молекул, при том, что антител например IgE, производится на прежнем уровне [6]. Поэтому местное применение ГКС показано при локализованном проявлении атопического дерматита. Однако необходимо избегать длительного местного применение ГКС (в виде лосьонов, спреев, кремов, мазей) ввиду развития кожной атрофии, образования комедонов. При сильно выраженных симптомах атопии можно использовать преднизолон системно в дозе 0,25-0,5 мг/кг или дексаметазон в дозе 0,1 мг/кг.
В нашей практике при аутоиммунных болезнях преднизолон в иммуносупрессивных дозах (2-6 мг/кг) назначается ежедневно короткими курсами до стабилизации состояния пациента, затем доза снижается до противовоспалительной и/или увеличиваются интервалы между введением препарата до 2-3 суток. При невозможности снизить дозу и кратность введения ГКС переводим пациентов на комбинированную терапию с использованием цитостатиков.
Цитостатики
Долгое время в дерматологии основными показаниями для цитостатиков считались опухоли. Сейчас иммуносупрессивная активность цитостатиков используется для терапии иммунокомплексных и аутоиммунных кожных заболеваний (пузырчатка, склеродермия, системная красная волчанка и др.). Учитывая особую опасность, применение этих препаратов ограничивается особо тяжелыми случаями, когда имеется резистентность к ГКС. Большая часть побочных действий цитостатиков связана с их антипролиферативным действием, которое распространяется на все виды быстро делящихся клеток (костный мозг, эпителий желудочно-кишечного тракта, клетки репродуктивной системы). Поэтому наиболее часто возникают следующие осложнения: анорексия, рвота, реже диарея, язвенный стоматит, анемия. Противопоказаниями к назначению цитостатиков являются: гиперчувствительность, печеночная и почечная недостаточность, беременность, тяжелые инфекции. В процессе лечения необходимо проводить мониторинг лабораторных показателей крови. Из всего многообразия препаратов этой группы в терапии дерматологических пациентов нами используется лишь три (азатиоприн, циклофосфамид, хлорамбуцил).
Антиметаболиты
Антиметаболиты – антифолиевые – метотрексат и антипуриновые – азатиоприн – оказывают цитотоксическое действие на размножающиеся клетки иммунной системы (преимущественно В-лимфоциты и Т-супрессоры). Азатиоприн подавляет синтез ДНК и РНК. В результате нарушается деление зрелых лимфоцитов. Поскольку митоз и пролиферация этих клеток – обязательные компоненты иммунного ответа, именно их нарушением, по-видимому, обусловлено иммуносупрессивное действие азатиоприна. Возможен и другой механизм – блокирование синтеза РНК (вероятно, мРНК), затрудняющее переработку антигена еще до стимуляции лимфоцитов. Однако на вторичный иммунный ответ азатиоприн почти не влияет. Его обычно назначают в дозе 1,5-5 мг/кг/сутки в комбинации с преднизолоном или циклоспорином, что позволяет снизить дозу последних. Азатиоприн выпускается по доступной цене в таблетках по 0,05, что позволяет его удобно дозировать. Чаще всего собакам назначается азатиоприн курсом 4-6 недель вместе с ГКС, причем доза последних постепенно снижается. Далее для поддержания ремиссии препарат вводят в дозе 2 мг/кг через день, проводя ежемесячно контроль «печеночных» показателей и клинического анализа крови. Азатиоприн быстро разрушается в печени, поэтому коррекции дозы в зависимости от нарушения функции почек не требуется, хотя возможно накопление метаболитов азатиоприна. В некоторых случаях, у собак с высокой чувствительностью к препарату развиваются лейкопения и, реже, тромбоцитопения. В таких случаях дозу снижают. В высоких дозах и при длительном применении азатиоприн вызывает желтуху вследствие холестатического гепатита, реже анемию, что требует отмены препарата [1, 4, 5]. Препарат противопоказан кошкам ввиду необратимой миелосупрессии даже в минимальной дозе [7].
Алкилирующие соединения
Алкилирующие соединения – циклофосфамид и хлорамбуцил – активируются, попадая в активные опухолевые и иммунокомпетентные клетки, разрушая ДНК, подавляя развитие этих клеток, обладают избирательным действием на клетки лимфоидного ряда (Т и В-лим-фоциты), проявляя супрессорную активность как в отношении пролиферирующих, так и «покоящихся» иммунокомпетентных клеток. Эти препараты является цитотоксичными для В-лимфоцитов и угнетают их стимулированную пролиферацию. Циклофосфан косвенно (через Т-хелперные лимфоциты) вызывает супрессию зрелых форм цитотоксических Т-киллеров. Высокие терапевтические дозы циклофосфана вызывают снижение числа и ослабление функции макрофагов и моноцитов. Наиболее частыми побочными действиями алкилирующих соединений являются: панцитопения (на 7-14 день), повреждение слизистой оболочки желудочно-кишечного тракта за счет ингибирования регенеративных процессов (гастроэнтероколит), геморрагический цистит, алопеции у собак с постоянно отрастающей шерстью (пудели, бобтейл, керри-блю-терьер). Препараты этой группы успешно применяются для лечения собак и кошек с пузырчаткой и кошек с эозинофильными гранулемами, неподдающимися ГКС терапии. Дозы циклофосфана составляют 1,5-2,5 мг/кг (50 мг/м2 поверхности тела) 1 раз в день 4 дня подряд, еженедельно. Пульс-терапия циклофосфамидом (7 мг/кг в/в еженедельно) позволяет снизить токсичность препарата, не снижая его эффективности. Хлорамбуцил (лейкеран) назначают в дозах 0,1-0,2 мг/кг (2-4 мг/м2 поверхности тела) ежедневно или через день. Препарат удобно дозировать (таблетки 2 мг), миелосупрессия достаточно редка и обратима, даже у кошек проходит после отмены препарата. Симптомы поражения желудочно-кишечного тракта (анорексия, рвота, диарея) возникают реже при назначении через день. Курс обычно составляет 1-2 месяца, затем доза может быть снижена вплоть до отмены препарата. Быстрая отмена алкилирующих соединений при аутоиммунных болезнях кожи может привести к «эффекту отдачи» [3, 4, 6]. При лечении животных препаратами этой группы рекомендуется проводить контроль клинического анализа крови, включая подсчет тромбоцитов, каждые 2 недели.
Циклоспорин А
Из антибиотиков наиболее широко используется пептид грибкового происхождения циклоспорин А, который преимущественно угнетает Т-хелперы и эффекторы, сохраняя Т-супрессоры, что способствует угнетению иммунопатологических процессов, позволяет обеспечить необходимую степень подавления иммунитета без тяжёлых, угрожающих жизни побочных эффектов и глубокого снижения противоинфекционного иммунитета. Он нарушает синтез ИЛ-2 и других провоспалительных цитокинов, блокируя транскрипцию их мРНК, и, таким образом, тормозит пролиферацию Т-лимфоцитов и останавливает развитие клеточно-опосредованных иммунных реакций [5]. При атопическом дерматите и аутоиммунном адените сальных желез он применяется в дозе 2.5 мг/кг/сутки. В тяжелых случаях доза может быть увеличена до 5 мг/кг/сутки. Суточную дозу следует делить на 2 приёма. При достижении положительного клинического результата, дозу необходимо постепенно снижать до полной отмены. Недостатком этого препарата являются высокая стоимость. Основными побочными действиями этого препарата является нефротоксичность, анорексия, рвота. Если не удается контролировать ситуацию с помощью одного циклоспорина, то для достижения начальной ремиссии или для купирования приступа воспаления можно присоединить системные ГКС (преднизолон в суточной дозе 0.2-0.6 мг/кг или другой глюкокортикостероид в эквивалентной дозе). Поскольку циклоспорин А подавляет синтез Т-лимфоцитами ИЛ-2, полагают, что сочетание его с глюкокортикоидами приведет к двойному блоку в цепочке: макрофаг – ИЛ-6/ИЛ-1 – Т-лимфоцит – ИЛ-2. Циклоспорин А эффективнее в комбинации с глюкокортикоидами, однако есть сообщения о летальном исходе от системного микоза в результате такого лечения [2]. В связи с частым осложнением атопии дерматитом, вызванным грибами рода Malassezia, некоторые авторы рекомендуют сочетать циклоспорин А с кетоко-назолом с целью снижения дозы циклоспорина и предотвращения распространения грибковых инфекций [2].
Следующим этапом развития теории и практики иммуносупрессивной терапии – внедрение протоколов комбинированной трёхкомпонентной иммуносупрессии, принятых в гуманной медицине [1]. Стандартная трёхкомпонентная иммуносупрессия на сегодняшний день состоит из комбинации циклоспорина А, глюкокортикоида и цитостатика (метотрексата или азатиоприна).
Заключение
В заключении можно сказать, что стероиды и цитостатики – препараты, способные вызвать резкое улучшение течения определенных тяжелых болезней и столь же резкое ухудшение здоровья вследствие развития побочных эффектов, поэтому решение об использовании этих средств должно быть обосновано. После улучшения состояния пациента дозы необходимо уменьшить до минимально необходимой для поддержания нужного эффекта, затем вплоть до отмены (по возможности) [6]. Применение иммунодепрессантов способствует снижению резистентности организма к опухолевому росту и инфекции, т.е. предрасполагает к развитию различных бактериальных, грибковых, паразитарных и вирусных инфекций, причем часто с участием условно-патогенных возбудителей. Учитывая потенциальную опасность этих инфекций для жизни, следует применять эффективную систему профилактических и лечебных мероприятий, особенно в случаях длительного применения комбинированного иммуносупрессивного лечения. Терапия должна проводиться под постоянным гематологическим контролем, при неблагоприятных сдвигах дозы препаратов снижают, либо лечение прекращают. При отсутствии эффекта лечения возможно комбинированное применение нескольких средств, замена схемы терапии.
Литература
1. Добрица В.П., Ботерашвили Н.М., Добрица Е.В. Современные иммуномодуляторы для клинического применения. СПб., Политехника, 2001.-251 с.
2. Пападогианакис Э. Новое об атопическом дерматите // VetPharma, 2012. № 1-2. С. 22-24.
3. Патерсон С. Кожные болезни кошек: пер. с англ. М.: Аквариум-ЛТД, 2002.- 168 с.
4. Патерсон С. Кожные болезни собак: пер. с англ. М.: Аквариум-Принт, 2006.- 176 с.
5. Райд Дж. Л. Клиническая фармакология и фармакотерапия: пер. с англ. М.: Медицинская литература, 2009. – 416 с.
6. Рациональная фармакотерапия заболеваний кожи и инфекций, передаваемых половым путем. Под ред. Ку-бановой А.А., Кисиной В.И. М.: Литтерра, 2005.- 882 с.
7. Современный курс ветеринарной медицины Кирка: пер. с англ. М.: Аквариум-Принт, 2005.- 1376 с.
8. Софронов Б.Н., Левин М.Я., Орехова Л.Ю. Введение в иммунологию. СПб.: Стайл, 1995.- 116 с.
9. Bach J.-F. Regulatory T-cells in autoimmune diseases: the role of non-Th2 cells. Basic mechanisms and therapeutic perspectives.- Autoimmunity Reviews, 2002.- v. 1, № 1-2, 1 р.

Назад в раздел

















