Использование метода полимеразной цепной реакции в реальном времени для выявления инфекционных агентов и сопутствующих инфекций при диарее собак
Еще фото
Автор (ы): Алина Бауманн да Роча Гицци, отдел ветеринарной медицины Федерального университета Парана, Бразилия, Симоне Тостес Оливейра, отдел ветеринарной медицины Федерального университета Парана, Бразилия, Кристиан М. Лейтеннегер, IDEXX лаборатория, США, Марко Эстрада, IDEXX лаборатория, США, Дениз Адамчик Кожемякин, лаборатория патологии животных «Clinilab», Бразилия, Рафаэль Стедиль, отделение медицины животных Федерального университета Рио-Гранде-ду-Сул, Бразилия, Мэри Маркондис, клиника хирургии и репродукции животных Колледжа ветеринарной медицины при Государственном университете Сан-Паулу, Бразилия, Александр Уэлкер Биондо, отдел ветеринарной медицины Федерального университета Парана, Бразилия, отделение ветеринарной патологической биологии Университета штата Иллинойс, США / Aline Baumann da Rocha Gizzi, department of Veterinary Medicine, Federal University of Parana, Brazil, Simone Tostes Oliveira, department of Veterinary Medicine, Federal University of Parana, Brazil, Christian M Leutenegger, IDEXX Laboratories Inc., USA, Marko Estrada, IDEXX Laboratories Inc., USA, Denise Adamczyk Kozemjakin, сlinilab Laboratory of Animal Pathology, Brazil, Rafael Stedile, department of Animal Medicine, Federal University of Rio Grande do Sul, Brazil, Mary Marcondes, department of Clinics, Surgery and Animal Reproduction, College of Veterinary Medicine, Sao Paulo State University, Brazil, Alexander Welker Biondo, department of Veterinary Medicine, Federal University of Parana, Brazil, department of Veterinary Pathobiology, University of Illinois, USA
Журнал: №6 - 2014
Перевод с английского А.Н. Герке
УДК 619:616-022:616.34-008.314.4:634.7
Gizzi et al. BMC Veterinary Research 2014, 10:23 http://www.biomedcentral.com/1746-6148/10/23
Ключевые слова: собака, смешанная инфекция, диарея, возбудители, ПЦР в режиме реального времени
Key words: canine, co-infection, diarrhea, panel , real- time PCR
Сокращения
CDV – вирус чумы собак
CCOV – коронавирус собак
CPV-2 – тип 2 парвовируса собак
CPA – Clostridium perfringens альфа-токсин
Аннотация
Справочная информация: Инфекционная диарея может быть вызвана бактериями, вирусами, простейшими, а также их ассоциацией. Выявление смешанной инфекции у собак с диареей важно для определения прогноза и выработки стратегии лечения и профилактики. Хотя многие патогенные организмы по отдельности были выявлены методом полимеразной цепной реакции (ПЦР) в режиме реального времени, полный перечень возбудителей, вызывающих диарею у собак, принадлежащих частным владельцам, до сих пор не установлен. Целью данного исследования являлось установление встречаемости отдельных возбудителей и сопутствующих инфекций методом ПЦР в режиме реального времени у собак с диареей и без, а также распространенности инфекций в разных странах. В исследовании были использованы собаки, принадлежащие частным владельцам, обратившимся в ветеринарную клинику. Образцы фекалий были исследованы с использованием молекулярных методов на вирус чумы плотоядных, коронавирус собак, парвовирус собак второго типа (CPV-2), альфа-токсин Clostridium perfringens (CPA), Cryptosporidium spp., Giardia spp. и бактерии рода Salmonella spp.
Результаты: В общей сложности, в исследование было включено 104 собаки с диареей и 43 клинически здоровые собаки, которые были обследованы последовательно в крупнейшем частном ветеринарном госпитале. В целом, у 71 из 104 (68,3%) собак с диареей были выявлены инфекционные агенты: у 39 из 71 собак (54,9%) – один возбудитель, у 32 из 71 собак (45,1%) – ассоциированная инфекция, в том числе у 21 из 32 собак (65,6%) – два, у 5 из 32 (15,6%) – три, и у 6 из 32 (18,8%) – четыре возбудителя одновременно. 13 из 43 (30,2%) собак контрольной группы оказались положительны, но лишь по одной инфекции. Наиболее распространенными возбудителями, вызывающими диарею у собак, были CPA (40 из 104 собак, 38,5%), CPV-2 (36 из 104 собак, 34,6%) и Giardia spp. (14 из 104 собак, 13,5%). Парвовирус собак CPV-2 был наиболее распространенным возбудителем в случаях ассоциированной инфекции, он был выявлен совместно с CPA, Cryptosporidium spp. или лямблиями Giardia spp. Не установлено статистически достоверных отличий (Р = 0,8374) в продолжительности диареи или смертности (Р = 0,5722) в зависимости от наличия одного возбудителя или сопутствующих инфекций.
Выводы: У собак с диареей установлена более высокая распространенность возбудителей инфекций, чем в контрольной группе. В то время как у здоровых собак были выявлены только моноинфекции, около половины собак с диареей имели сопутствующие инфекции. Таким образом, у собак с диареей необходимо подозревать несколько возбудителей. Влияние сочетанной инфекции на исход болезни остается неясным, поскольку уровень смертности и продолжительность диареи, как оказалось, не зависят от этих факторов.
Summary
Background: Infectious diarrhea can be caused by bacteria, viruses, or protozoan organisms, or a combination of these. The identification of co-infections in dogs is important to determine the prognosis and to plan strategies for their treatment and prophylaxis. Although many pathogens have been individually detected with real-time polymerase chain reaction (PCR), a comprehensive panel of agents that cause diarrhea in privately owned dogs has not yet been established. The objective of this study was to use a real-time PCR diarrhea panel to survey the frequencies of pathogens and co-infections in owned dogs attended in a veterinary hospital with and without diarrhea, as well the frequency in different countries. Feces samples were tested for canine distemper virus, canine coronavirus, canine parvovirus type 2 (CPV-2), Clostridium perfringens alpha toxin (CPA), Cryptosporidium spp., Giardia spp., and Salmonella spp. using molecular techniques.
Results: In total, 104 diarrheic and 43 control dogs that were presented consecutively at a major private veterinary hospital were included in the study. Overall, 71/104 (68,3%) dogs with diarrhea were positive for at least one pathogen: a single infection in 39/71 dogs (54,9%) and co-infections in 32/71 dogs (45,1%), including 21/32 dogs (65,6%) with dual, 5/32 (15,6%) with triple, and 6/32 (18,8%) with quadruple infections. In the control group, 13/43 (30,2%) dogs were positive, all with single infections only. The most prevalent pathogens in the diarrheic dogs were CPA (40/104 dogs, 38,5%), CPV-2 (36/104 dogs, 34,6%), and Giardia spp. (14/104 dogs, 13,5%). CPV-2 was the most prevalent pathogen in the dual co-infections, associated with CPA, Cryptosporidium spp., or Giardia spp. No statistical difference (P = 0,8374) was observed in the duration of diarrhea or the number of deaths (P = 0,5722) in the presence or absence of single or co-infections.
Conclusions: Diarrheic dogs showed a higher prevalence of pathogen infections than the controls. Whereas the healthy dogs had only single infections, about half the diarrheic dogs had co-infections. Therefore, multiple pathogens should be investigated in dogs presenting with diarrhea. The effects of multiple pathogens on the disease outcomes remain unclear because the rate of death and the duration of diarrhea did not seem to be affected by these factors.
Справочная информация
Инфекция, как причина диареи собак, все еще остается проблемой для ветеринарного врача в связи с изменчивостью возбудителей и возможностью одновременного наличия сопутствующих инфекций, вызванных вирусами, бактериями и простейшими [27, 30]. Патологические процессы взаимосвязаны, в то время как некоторые возбудители остаются на поверхности слизистой оболочки и выделяют мощные энтеротоксины, что нарушает поток жидкости, другие проникают и размножаются в неповрежденных клетках эпителия, вызывая воспаление и гибель клеток организма хозяина [11]. Тем не менее, многие собаки являются носителями потенциальных возбудителей без каких-либо клинических признаков, поэтому причинно-следственные связи до конца не изучены. Молекулярные методы были использованы для идентификации и диагностики инфекционных заболеваний, в дополнение к традиционным культуральным и серологическим методам [19, 20]. Среди этих подходов использование ПЦР в режиме реального времени значительно повышало чувствительность, при этом она была выше, чем при использовании стандартных ПЦР для идентификации возбудителей в образцах фекалий собак [16]. Поэтому, несмотря на то что ряд патогенных микроорганизмов был обнаружен по отдельности методом ПЦР в реальном времени, в том числе Salmonella spp. [16] и патогенные штаммы кишечной палочки Escherichia coli [28], список потенциальных возбудителей, вызывающих диарею у собак частных владельцев, до сих пор не установлен. Таким образом, целью данного исследования было изучение патогенных сопутствующих инфекций в популяции собак с диареей и контрольной группе собак, принадлежащих частным владельцам, с использованием ПЦР в реальном времени и анализа возбудителей, вызывающих диарею.
Результаты
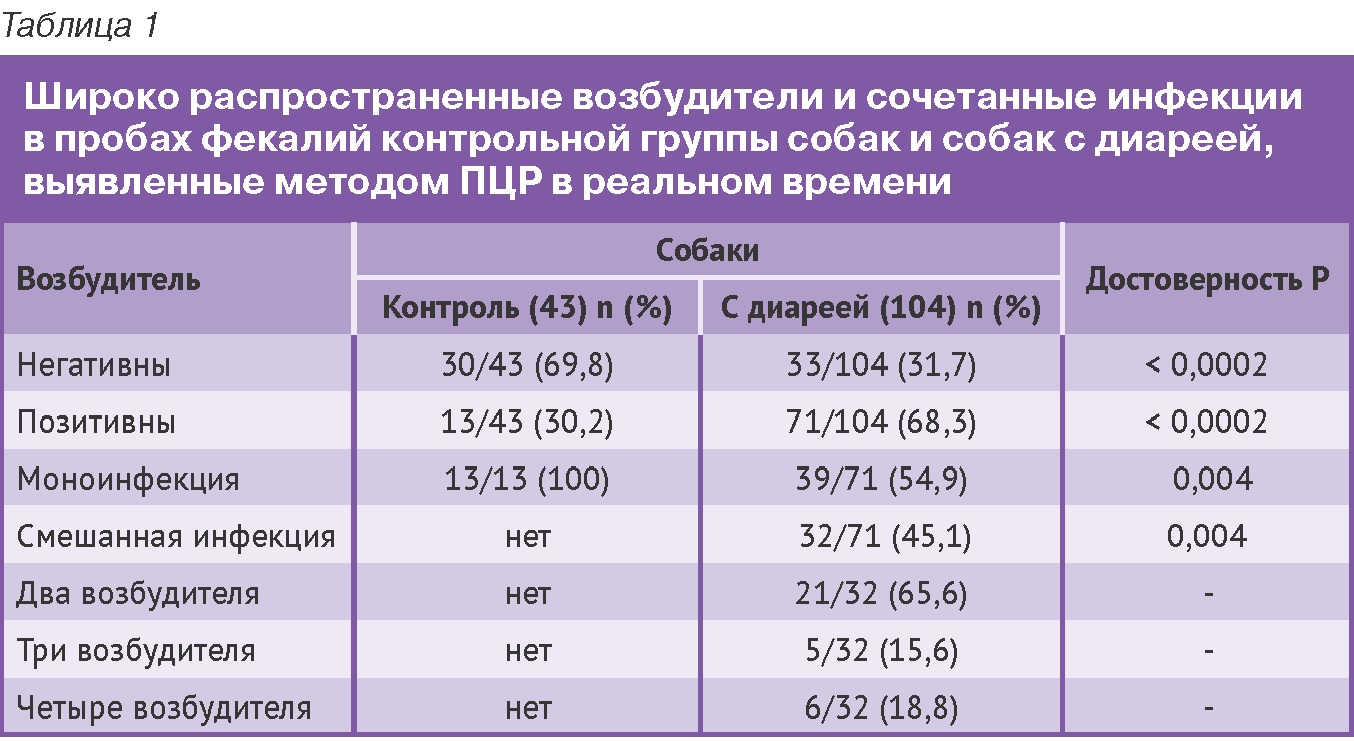
Методом ПЦР в реальном времени были идентифицированы потенциальные энтеропатогены в 71 из 104 (68,3%) образцов фекалий при диарее, в большинстве случаев присутствовало несколько возбудителей. Один возбудитель был причиной диареи в 39 из 71 (54,9%), а смешанная инфекция была выявлена в 32 из 71 (45,1%) позитивной пробы. При ассоциированной инфекции (Табл. 1) было обнаружено два, три и четыре возбудителя. Наиболее часто в случаях ассоциированной инфекции был выявлен парвовирус типа 2 (CPV-2). Так, пробы фекалий от собак с диареей были CPV-2 позитивны в 21 из 36 случаев (58,3%) в сочетании с другими возбудителями, одновременно с ним были выявлены альфа-токсин Clostridium perfringens (CPA), Cryptosporidium spp. и Giardia spp. Несмотря на то что у 13 из 43 (30,2%) собак контрольной группы в пробах фекалий были обнаружены микроорганизмы, способные вызвать диарею, во всех случаях не было обнаружено смешанной инфекции.
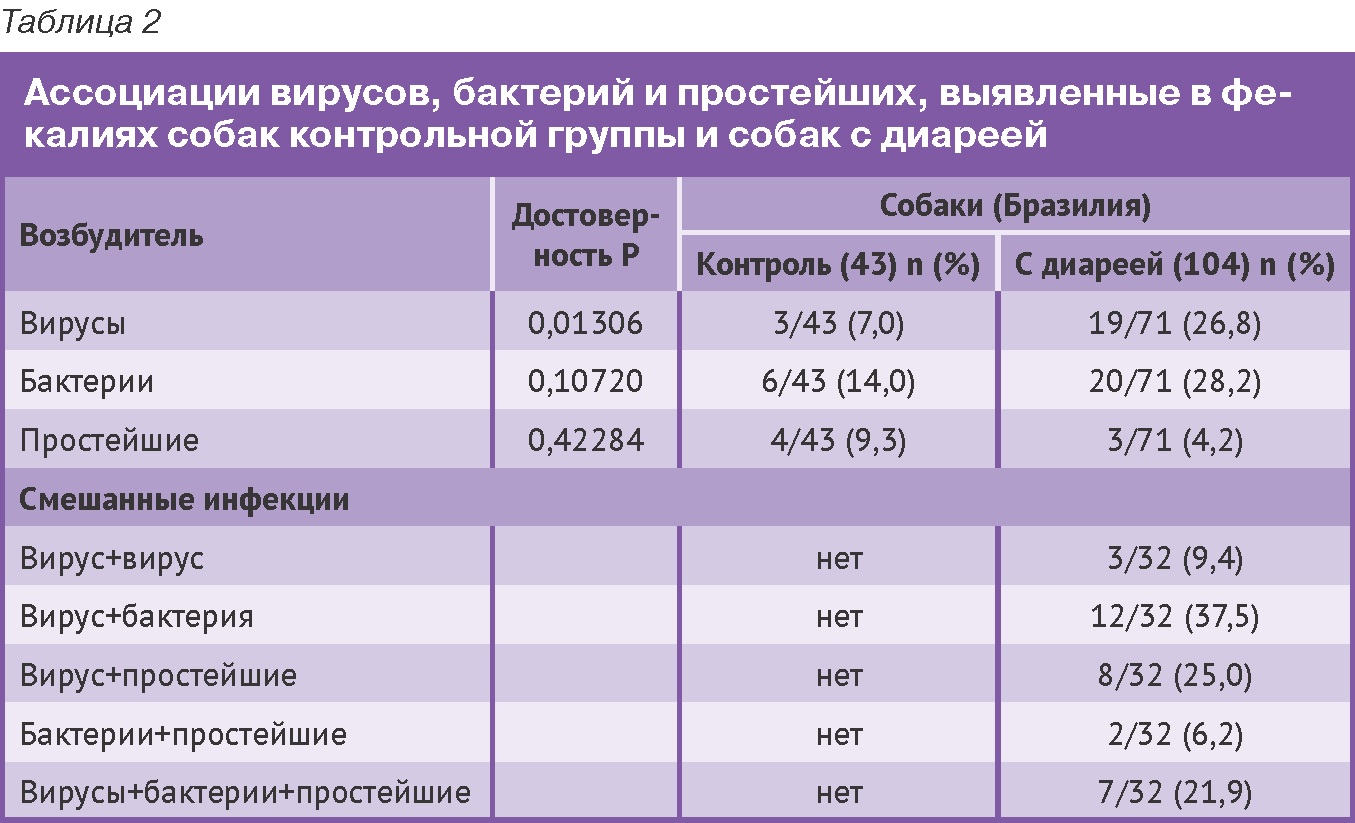
У 71 из 104 (68,3%) собак с диареей были выявлены моноинфекции, в том числе вирусные (26,8%), бактериальные (28,2%) или вызванные простейшими (4,2%), в то время как у собак контрольной группы в пробах фекалий были обнаружены вирусы (7,0%), бактерии (14,0%) и простейшие (9,3%). Ассоциация вирусной и бактериальной инфекций является преобладающим типом смешанной инфекции в группе собак с диареей (37,5%), причем наиболее частыми инфекциями (75%) в этой группе животных были парвовирус (CPV-2) и коронавирус собак (CCoV). Ассоциация вирусов и простейших была обнаружена у 25% собак этой группы, бактерий и простейших – у 6,2%, одновременное сочетание вирусной, бактериальной и протозойной инфекции – у 21,9% собак (Табл. 2).
Была установлена достоверная связь между результатами ПЦР в реальном времени на «возбудителей диареи» у собак с диареей (P < 0,001) и контрольной группы собак с нормальными фекалиями.
Среди отдельных возбудителей, выявленных методом ПЦР в реальном времени (Табл. 3), в пробах фекалий собак с диареей наиболее распространенным микроорганизмом является Clostridium perfringens (CPA), выделяющая альфа-токсин. Эта инфекция была выявлена у 40 из 104 (38,5%) собак с диареей и у 6 из 43 (14,0%) собак контрольной группы, причем эти отличия статистически высоко достоверны (P = 0,006). Тем не менее, для определения роли данного возбудителя при диарее собак необходима количественная оценка CPA в пробе фекалий. Как только был предварительно установлен предел более 300,000 копий/г фекалий [18], различия между контрольной группой (4 из 43, 9,3%) и группой собак с диареей (37 из 104, 35,6%) стали статистически значимыми (P = 0,0025). Парвовирус CPV-2 оказался вторым по частоте встречаемости, обнаруженным у 36 из 104 (34,6%) собак с диареей и не выявленным (0 из 43, отрицательно) у собак контрольной группы. Эти различия между группами также были статистически достоверны (P < 0,001).
Несмотря на то что у 9 из 104 (8,7%) собак с диареей был обнаружен вирус чумы собак (CDV), различие между группами были статистически не достоверны (Р = 0,059). Подобным образом у 12 из 104 (11,5%) собак с диареей и у 3 из 43 (7,0%) собак контрольной группы был обнаружен коронавирус (CCoV), причем не установлено достоверных отличий между группами (P = 0,554). Только у 1 из 104 (1,0%) и у 8 из 104 (7,7%) собак с диареей были обнаружены Salmonella spp. и Cryptosporidium spp. соответственно. В контрольной группе только у 2 из 43 (4,7%) были обнаружены Cryptosporidium spp., и эти группы достоверно не отличались (P = 0,724). Giardia spp. были обнаружены у 14 из 104 (13,5%) собак с диареей и у 2 из 43 (4,7%) собак контрольной группы, но эти различия недостоверны (P = 0,151).
Возрастные особенности
Среди собак с диареей 43 из 104 были в возрасте до года, 36 из 104 – от 1 до 8 лет и 25 из 104 – старше 8 лет. ПЦР позитивно было 39 из 43 (90,7%) проб фекалий от животных в возрасте до года, 20 из 36 (55,5%) проб от собак 1-8 лет и 12 из 25 (48,0%) – от собак старше 8 лет. Установлена статистически значимая связь между возрастом собак и парвовирусом CPV-2 (P < 0,0001), Giardia spp. (P = 0,01) и CCoV (P = 0,02), которые наиболее распространены у собак до года. Несмотря на то что парвовироз рассматривается в основном как болезнь щенков, CPV-2 также встречается у 4 из 36 (11,1%) животных в возрасте 1-8 лет и у 3 из 25 (12,0%) собак старше 8 лет. Только 13 из 36 (36,1%) животных, положительных по CPV- 2, не были вакцинированы, из которых 1 из 4 (25%) и 1 из 3 (33,3%) были взрослыми собаками в возрасте 1-8 лет и старше 8 лет соответственно. Подробности о сроках вакцинации и торговых марках вакцин не рассматривались в данном исследовании. Была установлена статистически значимая взаимосвязь между возрастом собак и возбудителями (P < 0,0001). Таким образом, наиболее часто у собак в возрасте до года (25/43, 58,1%) были выявлены смешанные инфекции, вызванные двумя и более возбудителями. Смешанные инфекции реже встречались в остальных возрастных группах, в том числе у 5 из 36 (13,8%) собак в возрасте 1-8 лет и у 3 из 25 (12%) собак старше 8 лет. Ассоциация вирусов и простейших значительно чаще является причиной диареи у собак до года (P = 0,0026), чем в других возрастных группах. Тем не менее, статически значимой зависимости между возбудителями и возрастом собак не установлено.
Зависимость продолжительности диареи от количества возбудителей
Не установлено статистически достоверной связи (P = 0,8374) между продолжительностью болезни и количеством возбудителей, вызвавших диарею.
Смертность при диарее
Наличие смешанной инфекции не увеличивает вероятность летального исхода по сравнению с моноинфекцией (P = 0,5722).
Продолжительность диареи
Данное исследование показало, что при продолжительности диареи более 10 дней стоит подозревать какое-либо инфекционное заболевание (P = 0,6606).
Связь диареи с применением антибиотиков
До получения результатов исследования проб фекалий (приблизительно 5 дней) 40 из 104 (38,5%) собак получали эмпирическое лечение с использованием комбинации 2-4 антибиотиков. Однако 40 из 71 (56,34%) собаки с диареей, у которых были получены положительные результаты ПЦР, лечили антибиотиками, которые, согласно литературным данным, не были уместными при инфекциях, выявленных в конечном счете.
Паразитологические исследования
В общем, в 20 из 104 (19,2%) и в 3 из 43 (7,0%) образцов фекалий от собак с диареей и контрольной группы соответственно результаты паразитологического исследования были положительны. Наиболее распространенными кишечными паразитами при диарее собак были прстейшие (Giardia spp. и/или Isospora spp.), которые обнаружились у 12 из 104 (11,5%) собак, и гельминты (Ancylostoma sp. и/или Toxocara sp.), которые выявлены у 10 из 104 (9,6%) собак. Все паразиты, обнаруженные в трех положительных пробах контрольной группы, были определены как Ancylostoma sp. После того как пробы фекалий собак с диареей и контрольной группы были исследованы, в 22 из 23 (95,7%) «положительных» образцов фекалий и в 61 из 124 (49,2%) «отрицательных» образцов фекалий при рутинном паразитологическом исследовании был получен «положительный» результат при исследовании на возбудителей диареи методом ПЦР в реальном времени. Если 13 из 147 (8,8%) проб были «положительны» при исследовании на гельминтозы (Ancylostoma sp. и/или Toxocara sp.), то 12 из 13 (92,3% из них) были также «положительны» при исследовании ПЦР в реальном времени. У собак, зараженных гельминтами, в 1,7 раза чаще выявляли и других возбудителей диареи при исследовании методом ПЦР в реальном времени, что указывает на статистически значимую связь (P = 0,006) между инфекциями, выявленными ПЦР в реальном времени, и гельминтозами. При исследовании на Giardia spp. методом ПЦР в реальном времени в 16 из 147 (10,9%) образцов был получен положительный результат, в то время как только в пяти из них Giardia spp. были обнаружены при паразитологическом исследовании. Учитывая, что ПЦР в реальном времени является «золотым» стандартом для выявления возбудителей, паразитологическое исследование показало чувствительность 31,2% (95% в доверительном интервале 12,1-58,5%). Isospora spp. были найдены в 7 из 147 (8,4%) образцов при паразитологическом исследовании, и все эти образцы также были положительными в ПЦР в реальном времени, поэтому возможно, что Isospora spp. может способствовать возникновению ассоциированных инфекций.
Географические особенности
Проблема диареи собак распространена повсеместно, инфекции были подтверждены в 68,3% проб фекалий от собак в Бразилии, в 54,5% проб в США, в 58,4% проб в Австралии, в 52,0% в Канаде, в 51,7% в Великобритания и 49,6% в Японии (Табл. 4). Смешанные инфекции при диарее собак встречались чаще в Бразилии (45,1%), чем в других странах, принявших участие в исследовании (Табл. 4), наиболее редко – в США (P <0,0001), Австралии (P = 0,01) и Канаде (P = 0,04).
Обсуждение
Методом ПЦР в реальном времени была установлена высокая распространенность носительства возбудителей, вызывающих диарею у собак, так, по крайней мере, один возбудитель был выявлен в 68,3% проб в Бразилии, несколько реже в США (54,5%), Австралии (58,4%), Канаде (52,0%), Великобритании (51,7%) и Японии (49,6%), как показано в таблице 4. Смешанные инфекции у собак с диареей в Бразилии были выявлены также чаще (45,1%), чем в других странах. Несмотря на более высокую распространенность энтеропатогенов и сопутствующих инфекций в Бразилии, данная проблема существует и в других странах, таким образом, инфекционная диарея является повсеместным явлением. Несмотря на то, что собаки, у которых было выявлено несколько возбудителей одновременно, присутствовали во всех возрастных группах. Это исследование подчеркивает важность выявления сопутствующих инфекций, особенно у собак в возрасте 0-1 года, поскольку установлено, что вероятность ассоциированных инфекций у щенков была в 4 раза выше, чем в других возрастных группах. Многие кишечные вирусы, бактерии и паразиты могут быть причиной диареи, вероятно, как по отдельности [22], так и в комбинации, при этом, ассоциации возбудителей могут вызвать более сильную диарею, чем моноинфекции [12]. Болезнетворные микроорганизмы при ассоциированной инфекции могут взаимодействовать синергически, например, воздействуя на иммунную систему хозяина, когда присутствие одного возбудителя приводит к повышению численности и/или вирулентности другого, что в результате способствует более тяжелому течению болезни [1, 13]. Таким образом, межвидовые взаимодействия возбудителей, оказывая влияние на организм хозяина, могут воздействовать на течение болезни и снижать вероятность благоприятного исхода [17, 23].
Однако этим исследованием было установлено, что при смешанной инфекции не увеличивалась продолжительность диареи, а также не было никакого существенного различия в числе летальных исходов в зависимости от числа возбудителей. Кроме того, в этом исследовании не было выявлено никакой достоверной взаимосвязи между взаимодействием энтеропатогенов при сопутствующих инфекциях, таким образом, причинно-следственная связь между наличием возбудителя и возникновением диареи до сих пор неясна. Наличие условно-патогенных или комменсальных микроорганизмов можно определить как дисбаланс кишечной флоры или дисбактериоз, при этом при выявлении возбудителей не всегда необходимо лечение. Тем не менее, поскольку все возбудители, изученные в данном исследовании, вызывали диарею в экспериментальных исследованиях, наличие информации о носительстве позволяет разработать стратегию профилактики и терапии. Данное исследование показало, что при продолжительности диареи более 10 дней стоит рассматривать инфекционные причины при дифференциальной диагностике. Эмпирические методы лечения и использование нескольких антибиотиков общепринято в рутинной ветеринарной практике, и знание перечня возбудителей предотвращает неправильное или чрезмерное применение антимикробных препаратов, что может привести к распространению резистентных микроорганизмов. Более того, некоторые из этих микроорганизмов являются потенциальными зоонозными возбудителями, в том числе анкилостомы, Giardia spp., Cryptosporidium spp. и Salmonella spp. Своевременное выявление этих микроорганизмов может снизить риск их попадания в организм человека и других животных.
Хотя это исследование было сфокусировано на собаках, принадлежащих частным владельцам, предположительно собаки, содержащиеся в приютах для животных, также могут быть носителями сопутствующих инфекций, в том числе зоонозов [29]. Были отмечены различия в распространенности как отдельных возбудителей, так и сочетанной инфекции, таким образом, у собак с диареей, содержащихся в приютах, чаще регистрировали ассоциированные инфекции (96,0%) [29], чем наблюдалось в данном исследовании (45,1%). Эта неоднородная популяция собак, возможно, имела иммунные нарушения вследствие воздействия факторов окружающей среды, скученного содержания, а также пищевых и/или психологических причин, а иногда и в связи с недостаточной медицинской помощью. Поэтому очевидно, что уровень сочетанной инфекции в этой группе собак значительно выше, чем у собак, содержащихся в домашних условиях.
В случаях сочетанной инфекции в этом исследовании наиболее часто были выявлены ассоциации вирусных и бактериальных агентов, в отличие от данных исследования, проведенного в США, где преобладали ассоциации вирусов и простейших. Наиболее часто в случаях сочетанной инфекцией были выявлены CPV-2 и CPA, они были обнаружены в 9 из 12 (75,0%) образцов от собак в Бразилии, при этом в США сочетанная инфекция CCoV и Giardia spp. была выявлена у 35,4% собак. При сопутствующих инфекциях может возникнуть необходимость проведения более интенсивных терапевтических мероприятий как по устранению конкретных возбудителей, так и коррекции электролитных, кислотно-щелочных расстройств, потенциального сепсиса и других метаболических последствий, а также в пищевой поддержке [24].
Ген альфа-токсина, присутствующий во всех штаммах Clostridium perfringens, может быть найден у клинически здоровых собак как часть нормальной микрофлоры кишечника [21]. Так, в настоящем исследовании он был обнаружен у 14% собак контрольной группы. Результаты ряда работ показывают, что традиционная ПЦР на выявление только CPA почти всегда будет положительной, что не имеет диагностической ценности [21]. Однако недавнее исследование показало, что количественное определение CPA может быть использовано в качестве диагностического маркера для выявления возбудителя у пациентов с диареей [18]. Используя ту же методику как и в предыдущем исследовании [18], мы выявили существенное различие между контрольной группой (4/43, 9,3%) и группой собак с диареей (37/104, 35,6%, Р = 0,0025), приняв за положительный результат более 300,000 копий CPA. Большее количество CPA у собак с диареей, чем у контрольных собак, предполагает, что высокие концентрации токсинов, продуцируемых этой бактерией, оказывают патогенное действие на желудочно-кишечный тракт. В настоящем исследовании, у собак с диареей в случаях сочетанной инфекции с CPA было в 3 раза больше копий, чем у тех, что были инфицированы только CPA. Мы предполагаем, что в этих случаях избыточный рост Clostridium perfringens приводит к увеличению количества токсина, что способствует возникновению диареи у собак.
Все собаки контрольной группы были отрицательными по парвовирусу CPV-2, при этом была установлена достоверная связь диареи и парвовируса (Р = 0,000004), CPV-2 был выявлен у 36 из 104 (34,6%) больных собак. Та же распространенность (18/51, 34,6%) наблюдалась в исследовании, проведенном в Бразилии, но только со щенками до 6 месяцев [2], в предыдущих исследованиях этот показатель составил от 16% [25] до 58% [14]. Хотя парвовироз считается, прежде всего, болезнью щенков, настоящий труд показал важность исследования взрослых собак на CPV-2, так как вирус был выявлен у 11,1% собак в возрасте 1-8 лет и 12,0% собак старше 8 лет. Кроме того, CPV-2 наиболее часто присутствует при ассоциированной инфекции у взрослых собак. Так, 58,3% проб от собак с диареей были положительными на CPV-2 совместно с другими возбудителями, и только у 3,8% щенков было выявлено несколько возбудителей одновременно с CPV-2 [2]. Эти данные могут отличаться в зависимости от географического региона, особенностей популяции, видов возбудителей и используемых методов диагностики [14]. Хотя данные о вакцинации живой модифицированной вакциной не были в центре внимания данного исследования, значение количества копий при выявлении CPV -2 было использовано для различия вакцинных штаммов от инфекций природного типа. Несмотря на использование вакцинации, CPV-2 по-прежнему был распространен среди собак, участвовавших в этом исследовании, лишь 13 из 36 (36,1%) из положительных по CPV-2 животных не были ранее вакцинированы. Тем не менее, остается неясным, может ли вакцина CPV-2 обеспечивать защиту от новых вариантов CPV, но недавнее исследование показало, что случаи неэффективности вакцины, скорее всего, не связаны с мутациями [3]. Таким образом, дальнейшие работы должны выяснить, насколько имеющиеся в настоящее время вакцины фактически контролируют местные штаммы парвовируса, и какие факторы могут влиять на эффективность вакцинации. В настоящем исследовании CPV-2 был самым распространенным возбудителем при ассоциированной инфекции с участием двух возбудителей, что может быть связано со значительным заражением окружающей среды или иммуносупрессией у собак [4].
Несмотря на то что CCoV был выявлен у собак с диареей чаще (11,54%), чем у собак контрольной группы (6,98%), отсутствие статистически значимого различия в этих показателях может указывать на второстепенную роль CCoV как возбудителя кишечной инфекции у собак. В отличие от CPV-2, приводящего к гастроэнтериту, CCoV был также обнаружен у здоровых собак, как сообщалось ранее [25]. Коронавирусная инфекция собак характеризуется низкой смертностью и высокой заболеваемостью с типично легким течением энтерита [5, 6]. Однако в случаях сочетанной инфекции CCoV с другими кишечными возбудителями наблюдалось более тяжелое течение диареи и даже более высокая смертность, например, при совместном выявлении CCoV и CPV-2 [7], аденовируса-1 [8], CDV [9]. Последний, как правило, чаще выявлялся у собак с диареей, чем у контрольных собак, хотя значение P было достаточно близко к пределу статистической значимости (P = 0,059).
В то время как встречаемость ряда кишечных инфекций, таких как Salmonella spp., Cryptosporidium spp. и Giardia spp. в различных странах была аналогичной (Табл. 4), CDV и CPV-2 примерно в 4 раза более распространены в Бразилии. Возможно, высокая частота вирусных заболеваний может быть связана с различиями в патогенности штаммов CPV-2, вакцинацией и экологическими факторами. В развитии вирусной инфекции важную роль может играть также ответ иммунитета хозяина, однако необходимы дальнейшие исследования, чтобы полностью понять причину такого широкого распространения парвовирусной инфекции в Бразилии. Общепризнанно, что кишечные паразиты способствуют возникновению диареи, в данной работе 95,7% положительных и 49,2% негативных проб при паразитологическом исследовании оказались положительными при использовании метода ПЦР в реальном времени, что доказывает, что копроскопия не может быть использована как единственный метод диагностики.
Выводы
Насколько нам известно, это первое исследование в Бразилии, выполненное с использованием ПЦР в реальном времени для анализа панели возбудителей диареи. Наши результаты показывают, что у собак с диареей присутствует относительно высокая распространенность патогенных инфекций. В то время как у клинически здоровых собак имели место лишь отдельные возбудители, около половины собак с диареей были положительны по нескольким возбудителям, что подчеркивает важность одновременного исследования нескольких возбудителей в пробах фекалий. Наиболее распространенными возбудителями при диарее собак в Бразилии были C. perfringens, выделяющая альфа-токсин, CPV-2 и Giardia spp. Среди сопутствующих инфекций, представленных двумя возбудителями, преобладали ассоциации парвовируса с C. perfringens, Cryptosporidium spp. и Giardia spp.
В этом исследовании не установлено связи между количеством возбудителей и длительностью диареи или увеличением риска смерти. Однако, учитывая, что все инфекционные агенты, рассмотренные выше, были описаны как возможная причина диареи в экспериментальных исследованиях, информация о носительстве этих возбудителей может позволить нам планировать лечение и выработать стратегию профилактики. Тем не менее, последствия воздействия нескольких патогенов на исход болезни остаются неясными, поскольку ни смертность, ни длительность диареи, как оказалось, не зависят от этого фактора.
Методика
Исследование популяции собак
В общей сложности 147 собак (104 с диареей и 43 клинически здоровых) были последовательно доставлены их владельцами в крупнейший частный ветеринарный госпиталь города Куритиба в Южной Бразилии для исследований методом ПЦР на потенциальных возбудителей диареи, проведения паразитологического обследования и сбора клинических данных.
Свежие образцы фекалий были собраны от всех 147 бразильских собак, помещены в пластиковые контейнеры, которые хранили до проведения исследования в холодильнике при +4°С. Пробы фекалий оценивали согласно шкале, описанной ранее [31]: 1 – жидкие или водянистые неоформленные фекалии; 2 – очень мягкие, несформированные фекалии; 3 – очень мягкие, умеренно сформированные фекалии; 4 – оформленные, твердые и цилиндрические фекалии. В группу собак с диареей были отнесены пробы с баллами от 1 до 3, в то время как у собак контрольной группы не было отмечено желудочно-кишечных расстройств (рвота, диарея или отсутствие аппетита), и их фекалии были оценены на 4 балла.
Кроме того, учитывали результаты исследования 12370 проб фекалий, проводимого в коммерческих целях методом ПЦР в реальном времени. Данные результаты были получены из Соединенных Штатов Америки (7829), Австралии (526), Канады (2855), Великобритании (674) и Японии (486). Пробы фекалий из разных стран (Бразилии, США, Австралии, Великобритании и Японии) были доставлены в США и исследованы методом ПЦР в реальном времени, часть проб из Канады были исследованы в том же режиме методом ПЦР, у того же поставщика услуг в стране происхождения (Канада). Количество нуклеиновых кислот, стабильность и контроль качества оценивались с помощью системы внутреннего контроля.
Данные эксперименты на животных были одобрены Этическим Комитетом и Обществом защиты животных Федерального университета Кутираба, Штата Парана Южной Бразилии (протокол номер 036/2011).
Клинические результаты
Была проведена оценка продолжительности болезни и смертности собак с диареей в зависимости от числа выявленных возбудителей. Также была рассмотрена связь между клиническими признаками, возбудителями и продолжительностью диареи (≤10 дней, от 10 дней до 2 месяцев, и > 2-х месяцев) и проведена оценка используемых антибиотиков для эмпирической терапии, осуществляемой после отбора проб до получения результатов.
ПЦР в реальном времени
Нуклеиновые кислоты были экстрагированы с использованием стандартных протоколов (Corbett XTractor-Gene, Qiagen, Valencia, CA, USA). Ген 18S рРНК был использован для определения количества геномной ДНК и кДНК после обратной транскрипции и для подтверждения чистоты ДНК.
Для проведения ПЦР были использованы расходные материалы IDEXX (IDEXX Laboratories, Inc., Westbrook, ME, USA) и коммерческое программное обеспечение (PrimerExpress версии 3.0, Applied Biosystems, Foster City, CA, США). Кроме того, два праймера, фланкирующие амплифицированный фрагмент при ПЦР в режиме реального времени, были подвергнуты анализу с целью проверки последовательности. Пробы фекалий были исследованы методом ПЦР в реальном времени для выявления потенциальных энтеропатогенов, в том числе CDV (фос-фопротеин G, GenBank Accession номер AY649446.1), CCoV (М-гена, тип I, AF502583; тип EII D13096), CPV-2 (VP2, U22139), CPA (альфа токсин, L43545), Cryptosporidium spp. (ssrRNA A093489), Giardia spp. (ssrRNA, DQ836339) и Salmonella spp. (ген А, EU348366) в референсной лаборатории в течение 5 дней после сбора проб. CPA был определен количественно путем использования предварительно установленного предела > 300,000 копий/г фекалий [18]. Для разделения вакцинных и природных типов парвовирусной инфекции CPV-2 был использован предел (1,2 млн). ПЦР в реальном времени проводили со стандартными праймерами с использованием реактивов Mastermix (LC480 ProbesMaster, Roche Applied Science, Indianapolis, IN, США) на коммерчески доступном анализаторе ПЦР в реальном времени (Roche LightCycler 480).
Аналитическая и клиническая проверки
Исследования методом ПЦР в режиме реального времени были утверждены аналитически и клинически. Аналитическая проверка каждого анализа осуществлялась с использованием специфического синтетического положительного контроля по следующим шести критериям: эффективность амплификации, линейность, внутренняя и внешняя воспроизводимость, линейный коэффициент корреляции (r2), отношение флуоресцентного сигнала к шуму. Аналитическая чувствительность каждого анализа составила 10 молекул, результативность амплификации варьировала между 95 и 100%. Пробы были обработаны с использованием стандартных методов для каждого теста, а также была определена корреляция. Специфичность всех исследований методом ПЦР в реальном времени была подтверждена путем проведения повторного исследования проб материала с использованием дополнительных пар праймеров с внешним положительным контролем. Диагностическая чувствительность и специфичность на основе сравнения с референсными методами составили 90% для каждого теста, проводимого методом ПЦР в реальном времени. Учитывая, что «золотым» стандартом диагностики считаются следующие методы: иммунофлуоресцирующий анализ антител для CDV, иммуноферментный анализ для CPV-2 и Giardia и ПЦР в реальном времени, по данным Калифорнийского университета в Дэвисе, для CCoV, Cryptosporidium, и Salmonella.
Для контроля исследования каждой пробы было использовано 7 ступеней контроля качества:
1) ПЦР положительный контроль (количественный);
2) ПЦР отрицательный контроль;
3) отрицательный контроль экстракции (пять контролей на 96-луночный планшет);
4) ДНК контроль, ориентированный на 18S рРНК, используемый для количественного определения ДНК в представленной пробе;
5) РНК контроль, ориентированный на 18S рРНК, для количественного определения комплементарной ДНК в представленном образце после обратной транскрипции;
6) контроль контаминации окружающей среды;
7) пики внутреннего положительного контроля для мониторинга ингибирования ПЦР.
Эти контроли были использованы для оценки функциональности ПЦР (1), доказательства отсутствия загрязнения в реагентах (2) и оборудовании (5), отсутствия перекрестного загрязнения в процессе экстракции (3), оценки качества и чистоты ДНК и РНК для оценки качества проб (4 и 5), протокола обратной транскрипции (5), отсутствия случайных положительных сигналов ПЦР в лаборатории (6) и отсутствия ПЦР-ингибирующих веществ, перенесенных с матрикса образца (7).
Паразитологические исследования
Был использован ранее описанный флотационный метод с помощью сульфата цинка [10] и насыщенного раствора хлорида натрия [26]. Паразитологические исследования для выявления яиц паразитов, личинок, цист и ооцист в соответствии с их морфологическими характеристиками были проведены путем световой микроскопии [15, 26].
Статистический анализ
Результаты были подвергнуты статистическому анализу с помощью теста х2 или критерия вероятности Фишера. Различия считались значимыми при Р < 0,05. Статистический анализ проводили с использованием веб-сайта статистического расчета (VassarStats, Колледж Вассар, Паф-кипси, США).
Конфликт интересов
Авторы заявляют, что они не имеют конкурирующих интересов.
Вклад авторов
Алина Бауманн да Роча Гицци, Симоне Тостес Оливейра, Александр Уэлкер Биондо, Кристиан М. Лейтеннегер задумали исследование, участвовали в его разработке и координации; Алина Бауманн да Роча Гицци, Дениз Адамчик Кожемякин, Кристиан М. Лейтеннегер, Марко Эстрада участвовали в сборе данных и выполняли лабораторные анализы; Рафаэль Стедиль провел статистический анализ. Все авторы участвовали в разработке рукописи, прочли и одобрили окончательный вариант рукописи.
Благодарности
Авторы благодарят Марселус Сансон, Дэвида Поволни, Дафина М. Альбино, Мариану С. Оливейра и Марсель Прейндл за техническую помощь.
Литература
1. Bhavnani D, Goldstick JE, Cevallos W, Trueba G, Eisenberg JN: Synergistic effects between rotavirus and coinfecting pathogens on di-arrheal disease: evidence from a community-based study in northwestern Ecuador. Am J Epidemiol, 2012, 5:387-395.
2. Castro TX, Uchoa CMA, Albuquerque MC, Labarthe NV, Garcia RCNC: Canine parvovirus (CPV) and intestinal parasites: laboratorial diagnosis and clinical signs from puppies with gastroenteritis. Intern J Appl Res Vet Med, 2007, 5:72-76.
3. Castro TX, Costa EM, Leite JP, Labarthe NV, Cubel Garcia RC: Monitoring of canine parvovirus (CPV) strains detected in vaccinated puppies in Brazil. Res Vet Sci, 2011, 90:336-340.
4. Decaro N, Buonavoglia C: Canine parvovirus – a review of epidemiological and diagnostic aspects, with emphasis on type 2c. Vet Microbiol, 2012, 155:1-12.
5. Decaro N, Buonavoglia C: An update on canine coronaviruses: viral evolution and pathobiology. Vet Microbiol, 2008, 132:221-234.
6. Decaro N, Desario C, Billi M, Mari V, Elia G, Cavalli A, Martella V, Buonavoglia C: Western European epidemiological survey for parvovirus and coronavirus infections in dogs. Vet J, 2011, 187:195-199.
7. Decaro N, Martella V, Desario C, Bellacicco AL, Camero AL, Camero M, Manna L, d'Aloja D, Buonavoglia C: First detection of canine parvovirus type 2c in pups with haemorrhagic enteritis in Spain. J Vet Med B Infect Dis Vet Public Health, 2006, 53:468-472.
8. Decaro N, Campolo M, Elia G, Buonavoglia D, Colaianni ML, Lorusso A, Mari V, Buonavoglia C: Infectious canine hepatitis: an "old" disease reemerging in Italy. Res Vet Sci, 2007, 83:269-273.
9. Decaro N, Camero M, Greco G, Ziz-zo N, Tinelli A, Campolo M, Pratelli A, Buonavoglia C: Canine distemper and related diseases: report of a severe outbreak in a kennel. New Microbiol, 2004, 27:177-181.
10. Dryden MW, Payne PA, Ridley R, Smith RVT: Comparison of common fecal flotation techniques for the recovery of parasite eggs and oocysts. Vet Ther, 2005, 6:14-28.
11. Greene CE, Marks SL: Gastrointestinal and intra-abdominal infections. In Infectious Diseases of the dog and cat. 4th edition. Edited by Greene CE. St. Louis: Saunders Elsevier, 2012:950-981.
12. Griffiths EC, Pedersen AB, Fenton A, Petchey OL: The nature and consequences of coinfection in humans. J Infect 2011, 3:200-206.
13. Grimprel E, Rodrigo C, Desselberg-er U: Rotavirus disease: impact of coinfections. Pediatr Infect Dis J, 2008, 27:S3-S10.
14. Godsall SA, Clegg SR, Stavisky JH, Radford AD, Pinchbeck G: Epidemiology of canine parvovirus and coronavirus in dogs presented with severe diarrhoea to PDSA PetAid hospitals. Vet Rec, 2010,167:196-201.
15. Hendrix CM, Robinson E: Common laboratory procedures for diagnosing parasitism. In Diagnostic Para-sitology For Veterinary Technicians. 3rd edition. Edited by Hendrix CM, Robinson E. St Loui: Mosby Elsevier, 2006:227-245.
16. Kurowski PB, Traub-Dargatz JL, Morley PS, Gentry-Weeks CR: Detection of Salmonella spp in fecal specimens by use of real-time polymerase chain reaction assay. Am J Vet Res, 2002, 63:1265-1268.
17. Lello J, Norman RA, Boag B, Hudson PJ, Fenton A: Pathogen interactions population cycles, and phase shifts. Am Nat, 2008, 2:176-182.
18. Leutenegger CM, Marks SL, Robertson J: Toxin quantiication of clostridium perfringens is a predictor for diarrhea in dogs and cats. In Proceedings of the American College of Veterinary Internal Medicine (ACVIM): May 30 June 2012. Edited by McFarlane D, Sellon R. New York: Curran Associates, Inc, 2012:38.
19. Liu YT: A technological update of molecular diagnostics for infectious diseases. Infect Disord Drug Targets, 2008, 8:183-188.
20. Mackay IM: Real-time PCR in the microbiology laboratory. Clin Microbiol Infect, 2004, 10:190-212.
21. Marks SL, Kather EJ, Kass PH, Melli AC: Genotypic and phenotypic characterization of clostridium perfringens and clostridium dificile in diarrheic and healthy dogs. J Vet Intern Med, 2002, 16:533-540.
22. O Ryan M, Prado V, Pickering LK: A millennium update on pediatric diarrheal illness in the developing world. Semin Pediatr Infect Dis 2005, 16:125-136.
23. Pedersen AB, Fenton A: Emphasizing the ecology in parasite community ecology. Trends Ecol Evol, 2007, 3:133-139.
24. Richter KP: Clinical evaluation of dogs and cats with speciic clinical singns. In Small Animal Gastroenterology. Edited by Stainer JM. Hannover: Schluetersche, 2008:115-120.
25. Schulz BS, Strauch C, Mueller RS, Eichhorn W, Hartmann K: Comparison of the prevalence of enteric viruses in healthy dogs and those with acute haemorrhagic diarrhoea by electron microscopy. J Small Anim Pract, 2008, 49:84-88.
26. Sloss MW, Zajac AM, Kemp LR: Exame de Fezes Para Diagnostico de Parasitas. In Parasitologia Clinica Veterindria. 6th edition. Edited by Zajac AM. Sao Paulo: Manole Ltda, 1999:03-44.
27. Simpson KW: Gastric disease. In Textbook of Veterinary Internal Medicine. Volume 2. 6th edition. Edited by Ettinger SJ, Feldman EC. Philadelphia: WB Saunders Co, 2004:1310-1331.
28. Stenske KA, Bemis DA, Gillespie BE, Oliver SP, Draughon FA, Matteson KJ, Bartges JW: Prevalence of urovirulence genes cnf, hlyD, sfa/foc, and papGIII in fecal Escherichia coli from healthy dogs and their owners. Am J Vet Res, 2009, 70:1401-1406.
29. Tupler T, Levy JK, Sabshin AJ, Tucker SJ, Greiner EC, Leutenegger CM: Enteropathogens identiied in dogs entering a Florida animal Shelter with normal feces or diarrhea. J Am Vet Med Assoc, 2012,241:338-343.
30. Villiers E, Blackwood L: Laboratory evaluation of gastrointestinal disease. In BSAVA Manual of Canine and Feline Clinical Pathology. 2nd edition. Edited by German AJ, Hall EJ. Gloucester: BSAVA, 2005:207-222.
31. Westermarck E: Clinical evaluation of patients with chronic diarrhea. In Small Animal Gastroenterology. 1st edition. Edited by Stainer JM. Hannover: Schluetersche, 2008:127-133.

Назад в раздел

















