Дермодекоз собак: новая субстанция на основе авермектинов для создания новых лекарственных препаратов
Еще фото
Автор (ы): Т.С. Стерлина, Н.А. Колесникова, Т.С. Новик, А.В. Осеев, В.А. Дриняев
Журнал: №5 - 2012
Демодекоз собак – паразитарное заболевание, возбудителем которого является клещ Demodex canis. По мнению большинства исследователей, клинические проявления болезни возникают при избыточном размножении клещей, когда иммунная система собаки по какой-либо причине не может это размножение контролировать [1, 2].
Основными противопаразитарными средствами для сельскохозяйственных животных в последние 30 лет являются препараты на основе авермектинов и их производных. Попытки их применения для лечения демодекоза собак наблюдаются, по крайней мере, с середины 80-х гг. В первую очередь это относится к ивомеку, действующим веществом которого является ивермектин. Однако установлена высокая токсичность ивермектина для собак, в особенности среди пород колли и шелти. У животных наблюдали клинические признаки, ассоциированные с нейротоксическим действием препарата, такие как атаксия, мидриаз, аномальное поведение, тремор, слабость, угнетение, слепота, повышенная саливация, рвота, судороги, нарушения дыхания, кома и гибель [3]. Токсичными для собак этих пород в той или иной степени оказались и другие производные авермектинов и авермектиноподобных соединений – дорамектин, милбемицин, моксидектин; сообщения о подобных случаях приведены в недавних обзорах [1, 2].
В настоящее время известно, что повышенная чувствительность колли к ивермектину связана с высокой проницаемостью у них гематоэнцефалического барьера для ивермектина в результате мутации гена MDR-1 [4, 5]. При генетическом тестировании выявилось, что эта мутация встречается не только у колли и их помесей: специалисты ветеринарной лаборатории клинической фармакологии (Колледж ветеринарной медицины Вашингтонского государственного университета), где учредили процедуру проверки и запатентовали диагностический тест, считают, что чем больше собак будет проверяться, тем большее число пород попадет, вероятно, в список «пострадавших»; даже у домашних беспородных собак эта мутация встречается в 5% случаев [6]. Более того, неврологические побочные эффекты при ежедневном введении ивермектина были обнаружены у 28 собак «нечувствительных» пород; генетическая проверка обнаружила мутацию гена MDR-1 только у одной из них, у остальных генетические аномалии не были выявлены [7]. Следовательно, ивермектин и его аналоги могут быть опасными не только для собак пастушьих пород, не только при мутации гена MDR-1, и не зря сторонники применения ивермектина советуют для своевременного установления непереносимости препарата осторожное и постепенное повышение дозы для собак всех пород [1, 2].
Отсюда понятна острая необходимость в разработке препаратов с использованием менее токсичной субстанции. Традиционным способом снижения токсичности субстанций является их химическая модификация. Правда, этот способ применим только для так называемых однокомпонентных субстанций. Именно так были получены ивермектин как производное абамектина и селамектин как производное дорамектина. На основе селамектина разработан препарат стронгхолд, предназначенный для борьбы с экто- и эндопаразитами у собак всех пород и породных помесей, но для лечения демодекоза он не рекомендован.
Многокомпонентные субстанции, такие как аверсектин С [8], можно модифицировать другим способом, просто меняя их компонентный состав. Дело в том, что индивидуальные авермектины не идентичны по своим биологическим характеристикам. Для них характерна разная противопаразитарная активность, разная токсичность для теплокровных, к тому же они действуют через разные рецепторы [9, 10]. Поэтому при изменении компонентного состава комплекса можно получать субстанции с разными антипаразитарными и токсическими свойствами в зависимости от преобладания в комплексе тех или иных компонентов.
В настоящей работе представлены результаты оценки переносимости на животных пяти вариантов разработанных в НБЦ «Фармбиомед» авермектиновых комплексов разного компонентного состава и проверки токсичности образца, выбранного в качестве субстанции будущего препарата для лечения демодекоза собак, на адекватной лабораторной модели.
Материалы и методы
Исследования проводили в соответствии с правилами лабораторной практики (приказ МЗ РФ № 267 от 19.06.03) и «Руководству по экспериментальному (доклиническому) изучению новых фармакологических веществ» (2005). Содержание животных осуществлялось в соответствии с правилами, принятыми Европейской Конвенцией по защите позвоночных животных, используемых для экспериментальных и иных научных целей [11].
Эксперименты выполнены на белых беспородных мышах-самцах и новорожденных крысятах от беспородных крыс-самок. Животные были получены из питомника «Филиал Андреевка ГУ НЦ биомедицинских технологий РАМН», разведены специально и ранее не участвовали в исследованиях; от производителя получено ветеринарное свидетельство последнего контроля здоровья животных. Животных содержали в виварии ВИГИС.
В группы животных распределяли произвольно методом «случайных чисел», используя в качестве критерия массу тела.
В НБЦ «Фармбиомед» в лабораторных условиях было создано несколько оригинальных композиций авермектиновых комплексов (далее – АК) разного компонентного состава. На первом этапе работы оценивали переносимость каждой композиции в опытах на мышах. Мыши были выбраны с учетом их высокой чувствительности к авермектинам в результате повышенной проницаемости гемато-энцефалического барьера для последних (ситуация аналогична наблюдаемой для собак).
Использовали мышей самцов массой 22-25 г; в каждую группу входило по 10 животных; опыты были проведены в трех повторностях. Каждый из пяти вариантов АК вводили одним из трех способов: подкожно в виде инъекционного раствора, накожно (в обоих случаях на водно-спиртово-полимерной основе) и ректально в форме свечей (основа состояла из ланолина безводного 0,08 г; масла какао до 1,5 г). При накожном введении за сутки до аппликации у мышей в области спины выстригали шерстный покров (2x2 см), куда затем наносили тестируемый образец.
При подборе доз руководствовались имеющейся в литературе информацией о токсических свойствах ивермектина (LD50 для мышей) [12] и предполагаемой терапевтической дозой. Последняя составляет 0,2 мг/кг массы тела при подкожном введении и 0,5 мг/кг массы тела – при накожном. Для опыта была выбрана максимальная доза, т.е. 0,5 мг/кг массы тела, равная к тому же 1/50 LD50. Мы полагали, что при использовании более высоких доз, вызывающих большую смертность, будет труднее оценить различия между тестируемыми веществами.
Переносимость оценивали по общему состоянию животных, проявлению симптомов интоксикации, включая характерные для авермектинов нейротоксические признаки (скученность, угнетение, нарушение координации движений, судороги и т.п.), видимым физиологическим функциям и гибели животных; при инъекционном введении, кроме того, оценивали местную реакцию в месте введения. За животными наблюдали в течение 14 суток.
На втором этапе исследовали токсичность композиции АК, которую выбрали по результатам первого этапа (композиция получила название аверсектин С1). Использовали новорожденных крысят, т.к. у них гематоэнцефалический барьер формируется в процессе постнатального развития, и новорожденные крысята более чувствительны к действию авермектинов по сравнению со взрослыми животными [12], т.е., это наиболее чувствительная к авермектинам лабораторная модель.
Аверсектин d вводили подкожно, однократно, в первые или десятые сутки после рождения. При выборе дозы опирались на величину LD50 ивермектина для новорожденных крысят [12]. Выбранная доза, 1,5 мг/кг массы тела, составила 1/2 LD50, т.к. мы хотели оценить переносимость аверсектина С1 в наиболее жестких условиях. На каждую дозу использовали помет из 10-12 крысят обоего пола; опыты были проведены в трех повторностях. На 10-дневных крысятах для большей достоверности поставлено 2 серии опытов. Всего в этих опытах использовали 205 крысят. Критерием оценки токсического действия аверсектина С1 служила гибель животных: определяли процент смертности крысят в течение одной-трех недель после инъекции.
Во всех экспериментах в качестве препарата сравнения использовали ивермектин.
По окончании экспериментов животных умерщвляли дислокацией шейных позвонков.
Статистическую обработку полученных данных проводили с помощью программы Office Excel по Стьюденту-Фишеру с использованием t-критерия.
Результаты
1. Оценка переносимости разных композиций авермектиновых комплексах на мышцах
Все композиции АК отличались относительно низким содержанием авермектина В1, но по уровню остальных компонентов они различались довольно существенно, представляя собой сложные системы, в которых каждый индивидуальный авермектин мог оказать влияние на свойства других компонентов (Табл. 1).
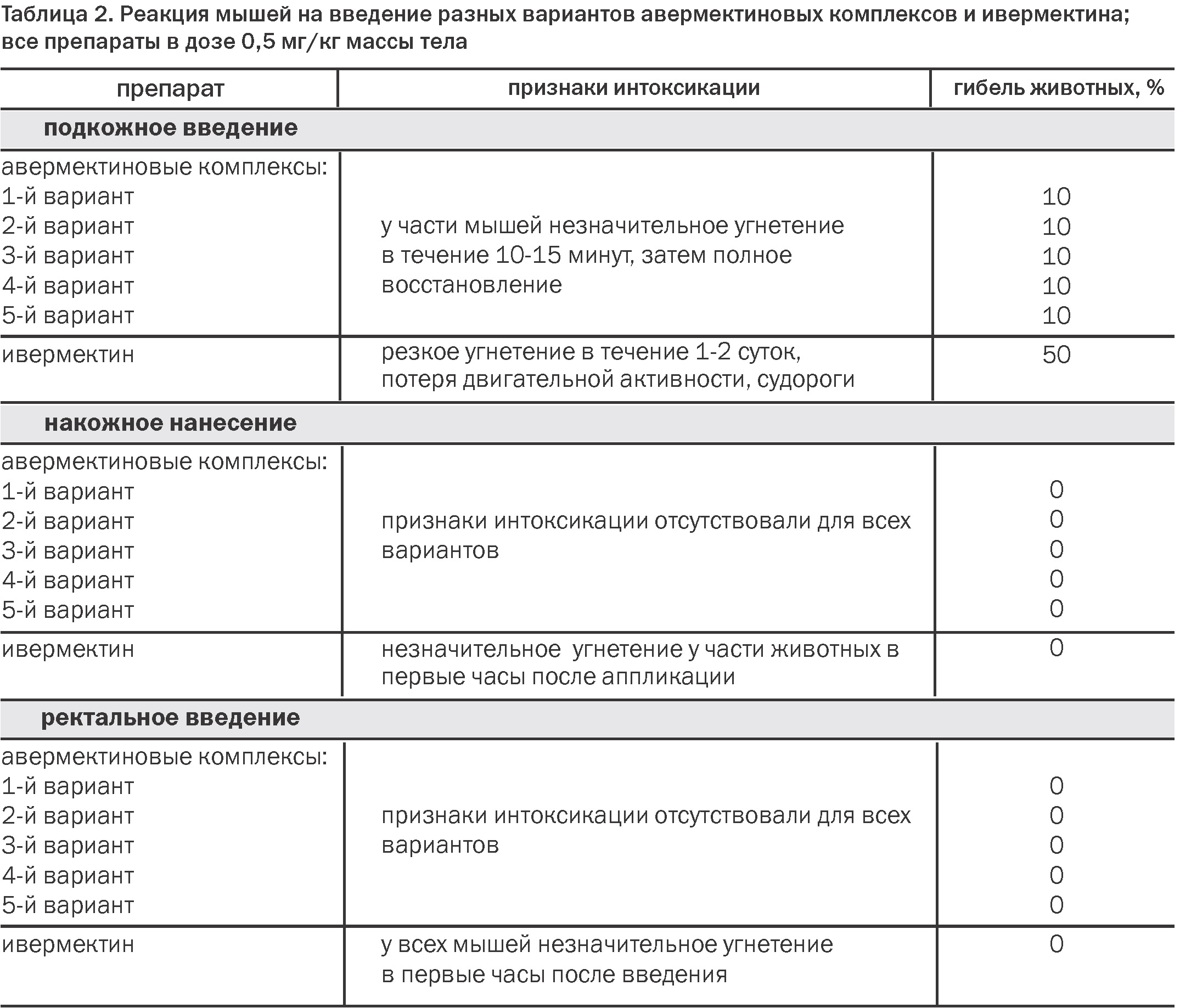
Результаты по сравнительной оценке переносимости АК и ивермектина на мышах обобщены в Таблице 2. Прежде всего, заметно, что токсичность вводимых соединений зависит от способа введения: она максимальна при подкожном введении и значительно меньше при двух других, причем, самое безопасное введение – накожное; это полностью согласуется с литературными данными [12, 13]. Но даже при подкожном введении АК признаки интоксикации появились только у части мышей, были незначительны и кратковременны; смертность не превышала 10%. При введении ивермектина признаки интоксикации были более выраженными, сохранялись намного дольше, погибало уже 50% животных. При двух других способах обработки гибели животных не наблюдалось – ни при введении АК, ни ивермектина, однако при введении АК признаки токсичности отсутствовали полностью у всех мышей, а при введении ивермектина было отмечено незначительное угнетение – или у всех мышей (ректальное введение) либо хотя бы у части животных (накожное нанесение).
Подводя итоги, можно заключить, что токсичность всех вариантов АК оказалась одинаковой, и при всех путях введения она ниже токсичности ивермектина. Особенно хорошо заметны различия при подкожном введении, и это тем более важно, что на основе АК предполагалось разработать именно инъекционный препарат.
Поскольку было установлено, что АК по токсичности не различаются, то выбор будущей субстанции определялся технологическими требованиями. Выбранный в качестве субстанции вариант получил название аверсектин d.
2. Оценка токсического действия аверсектина С1 на новорожденных крысятах.
Результаты, полученные при подкожном введении аверсектина d новорожденным крысятам, сведены в таблицу 3. У 10-дневных крысят смертность учитывали на 21-е сутки.
Для наглядности по данным этой таблицы сделана диаграмма выживаемости новорожденных крысят (Рис. 1). Выживаемость рассчитывали по формуле: % выживаемости = 100% - % гибели.
В опытах на однодневных крысятах (Рис. 1А) в группе, получившей ивермектин, через неделю после введения выжило 39,52% детенышей (фиолетовые стобцы), в группе, получившей аверсектин С1 – 74% (зеленые столбцы). Через три недели после введения все крысята, которым ввели ивермектин, погибли; из крысят, получивших аверсектин С1, 34,28%, т.е. почти треть, выжили.
У 10-дневных крысят (Рис. 1Б) гематоэнцефалический барьер сформирован уже в большей степени, чем у однодневных. Поэтому смертность в этих опытах ниже, чем в предыдущей серии. В группах, получавших аверсектин С1 (зеленые столбцы), не погиб ни один детеныш, т.е. выживаемость была 100%-ой. Однако токсичность ивермектина у этих крысят остается заметной: в группах, получавших ивермектин (фиолетовые столбцы), выжило только около половины крысят, в первой серии – 49,54%, во второй – 44,13%, т.е., в двух сериях аналогичных опытов получены практически одинаковые результаты.
Таким образом, результаты, полученные в опытах на новорожденных крысятах, свидетельствуют, что в этих условиях токсическое действие аверсектина С1 или полностью отсутствует на фоне довольно заметной токсичности ивермектина (опыты на 10-дневных крысятах) или, по крайней мере, существенно ниже токсичности ивер-мектина (односуточные крысята).
Это дает основание для использования аверсектина С1 в качестве действующего вещества препарата, предназначенного для лечения собак.
В качестве иллюстрации практического применения приведенных выше данных приводим в краткой форме информацию по препарату Аверсект® K&C. Разработанный на основе аверсектина С1 препарат прошел все необходимые для регистрации испытания, зарегистрирован как Аверсект® K&C (свидетельство о регистрации №ПВР-3-6.0/02674 от 11.02.11) и присутствует в справочнике «Видаль-ветеринар» 2011 г. издания. Он выпускается в форме 0,2% и 0,5% раствора для инъекций; 0,2% раствор предназначен для кошек и небольших собак (0,1 мл на 1 кг массы животного), 0,5% раствор – для собак средних и крупных размеров (0,4 мл на 10 кг). При пересчете на ДВ получается стандартная для авермектинов терапевтическая доза: 0,2 мг/кг или 200 мкг/кг м.т. животного. Ниже мы приводим некоторые выдержки из регистрационного досье.
По параметрам острой токсичности Аверсект K&C можно отнести к 4 классу опасности по ГОСТ 12.007-76.
В рекомендуемых дозах препарат не проявляет гепато- и нефротоксического действия, не вызывает аллергических реакций и не проявляет отдаленных эффектов.
В процессе клинического применения препарата разработаны эффективные схемы лечения различных клинических форм демодекоза собак, с использованием аверсекта K&C, аверсектиновой мази и мази фармайодной антисептической. Статья опубликована [14].
Литература
1. Mueller RS. Treatment protocols for demodicosis: an evidencebased review// Veterinary Dermatology - 2004.- V. 15.- P. 75-89.
2. Mueller, R. S., Bensignor, E., Ferrer, L., et al. Treatment of demodicosis in dogs: 2011 clinical practice guidelines// Veterinary Dermatology - 2012.- V. 23.- № 2.- P. 86-98.
3. Lovell R.A. Ivermectin and piperazine toxicoses in dogs and cats//Toxicology of selected Pesticides, drugs and Chemicals. - 1990. - V. 20. - № 2. - P. 453-467.
4. Mealey K.L., Bentjen S.A., Gay J.M. et al. Ivermectin sensitivity in collies is associated with a deletion mutation of the mdr1 gene. Pharmacogenetics 2001; 11: 727-733. Цит. по [2].
5. Roulet A., Puel O., Gesta S. et al. MDR1-deficient genotype in Collie dogs hypersensitive to the P-glycoprotein substrate ivermectin. European Journal of Pharmacology 2003; 460: 85-91. Цит. по [2].
6. Veterinary Clinical Pharmacology Laboratory at the College of Veterinary Medicine URL: http://www.vetmed. wsu.edu/depts-VCPL/
7. Bissonnette S, Paradis M, Daneau I et al. The ABCB1-1D mutation is not responsible for subchronic neurotoxicity seen in dogs of non-collie breeds following macrocyclic lactone treatment for generalized demodicosis. Veterinary Dermatology 2009; 20: 60-66. Цит. по [2].
8. Дриняев В.А., Кругляк Е.Б., Мосин В.А. и др. Аверсектин С: физико-химические и биологические свойства. Приклад биохим микробиол 1999;35:2:199-205.
9. Drinyaev V.A., Mosin V.A., Kruglyak E.B. et al. Effect of aver-mectins on Ca2+-depended Cl- currents in plasmalemma of Chara coralline cells. J. Membrane Biol 2001; 182:71-79.
10. Kokoz Yu.M., Tsyganova V.G, Korystova A.F. et al. Selective cytostatic and neurotoxic effects of avermectins and activation of the GABA receptors. Bioscience Rep 1999; 18:6: 535-546.
11. European Convention for the Protection of Vertebrate Animals Used for Experimental and other Scientific Purposes (ETS 123). Strasbourg, 1986.
12. Lankas, G.R., Gordon, L.R. Toxicology. In: Campbell, W.C., ed., Ivermectin and Abamectin, 1989, New York: Springer-Verlag, pp. 89-112.
13. Новик Т.С., Бару Р.В., Рябова В.А. и др. Острая токсичность аверсектина c при различных путях и формах введения. Эксперим. клин. фармакол. 2001, № 2, с.64-68.
14. Колесникова Н.А., Осеев А.В., Тыкин М.С. и др. Эффективные схемы лечения демодекоза. VetPharma 2012, № 3, с.48-50.

Назад в раздел

















