Инфузионные растворы - какими бывают и чем отличаются?
 21.04.2023
21.04.2023
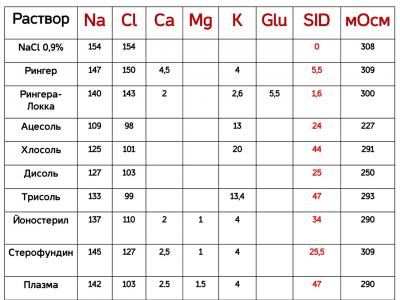
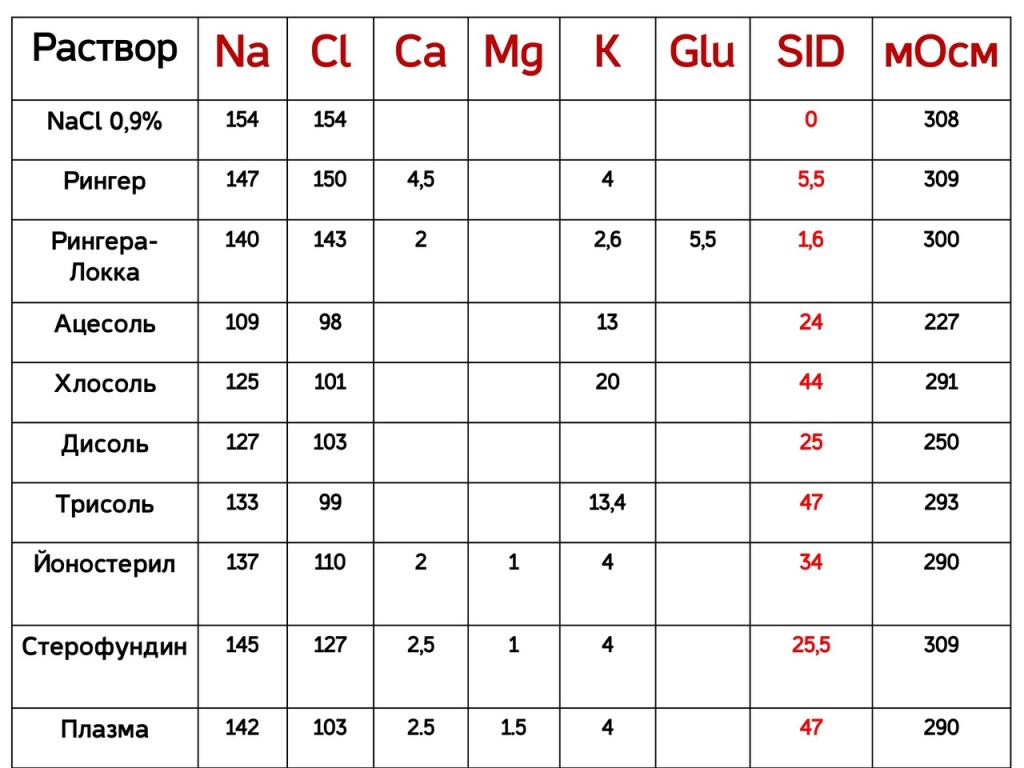 Прогнозирование эффектов кристаллоидных растворов легко провести с помощью физико-химической модели кислотно-щелочного равновесия Стюарта. Согласно его теории характеристиками сбалансированного кристаллоидного раствора являются:
Прогнозирование эффектов кристаллоидных растворов легко провести с помощью физико-химической модели кислотно-щелочного равновесия Стюарта. Согласно его теории характеристиками сбалансированного кристаллоидного раствора являются:• SIDinf = 24 мEqL-1;
• соответствие содержания электролитов их плазменной концентрации;
• наличие в составе органических ионов, предотвращающих повышение концентрации Cl в инфузионном растворе и являющихся донаторами резервной щелочности.
Исходя из этого выделяют среди кристаллоидных растворов:
1. несбалансированные (0,9% раствор NaCl)
2. частично сбалансированные (растворы Рингера лактат и Хартмана)
3. полностью сбалансированные растворы (Йоностерил, Стерофундин).
Применение несбалансированных растворов опасно развитием гиперхлоремического ацидоза. Использование частично сбалансированных кристаллоидных растворов может формировать или усугублять лактатацидоз в условиях тканевой гипоксии и/или дисфункции печени. Инфузия сбалансированных растворов позволяет быстро корректировать метаболический ацидоз.
Для объяснения физиологического эффекта инфузии несбалансированных растворов используют модель поведения кислот и щелочей канадского физиолога Питера Стюарта. Для описания КЩС Стюарт использовал серию уравнений, учитывающих закон действующих масс (Гульдберга и Вааге), закон сохранения масс и закон электронейтральности применимо к водным растворам.
При оценке кислотно-щелочного состояния, согласно Стюарту, выделают так называемое «рабочее» пространство КЩС: интерстиций, плазма и эритроциты (IPE – Interstitium, Plasma and Erythrocytes). Любое итоговое равновесие системы является функцией трёх независимых переменных, находящихся в IPE. Эти переменные включают в себя pCO2 (парциальное давление углекислого газа в растворе), SID (разница сильных ионов в растворе - strong ion difference) и A[TOT] (общая концентрация слабых кислот в растворе – альбумин, фосфаты).
SID является разницей между зарядом полностью диссоциируемых катионов (натрий, калий, кальций, магний) и анионов (хлориды, лактат, кетоновые кислоты и другие органические кислоты с pKa<4.0) и выражается в мэкв/л.
SID = (Na+ + K+ + Ca++ + Mg++) – Cl- + (другие сильные анионы)
Если допустить, что в растворе присутствуют только основные заряженные частицы, то, согласно закону электронейтральности, SID должен быть равным нулю. В биологических жидкостях SID не равен нулю, а представляет собой положительный заряд. Это объясняется присутствием в биологических растворах слабых электролитов, например, белков и фосфатов. Следовательно, заряд сильных катионов превышает заряд сильных анионов, и разница в норме составляет порядка 40 мэкв/л. Увеличение SID ведёт к алкалозу (в основном за счёт увеличения количества HCO3-), уменьшение SID ведёт к ацидозу (за счёт снижения количества HCO3-).
Напротив, увеличение A[TOT] ведёт к ацидозу, уменьшение – к алкалозу.
Идеальный инфузионный раствор должен не оказывать негативного эффекта на прогноз заболевания, обладать удовлетворительной фармакокинетикой, не накапливаться в тканях, не оказывать эффекта на электролитный состав плазмы, КЩС, не обладать отрицательными эффектами на гемостаз и иммунную систему, должен быть дешёвым, легко храниться и иметь длительный срок годности.
1) Кравец О.В., Клигуненко Е.Н. Базовые основы и принципы управляемой инфузионной терапии у больных с неотложной хирургической патологией органов брюшной полости // МНС. 2017. №5 (84). URL: https://cyberleninka.ru/article/n/bazovye-osnovy-i-pr.. (дата обращения: 12.07.2022).
2) Cherniy, V. (2018). Сбалансированные растворы в инфузионной терапии. Резервная щелочность. Идеальный инфузионный раствор. Клінічна та профілактична медицина. 2. 83-92. 10.31612/2616-4868.2-5.2018.10.
https://www.biovitar.ru/infuzionnye-rastvory-kakimi-b..
Источник: Анестезиологическое ветеринарное общество ВИТАР


















