Первичная и вторичная глаукома у собак. Современный подход к диагностике и медикаментозному лечению
Еще фото
Автор (ы): С.А.Бояринов - ветеринарный врач-офтальмолог при ИВЦ МВА, начальник лечебно-профилактического отдела СББЖ г.Пушкино, аспирант кафедры ФГБУ ФГБОУ ВО МГАВМиБ - МВА им.К.И.Скрябина, член RSVO, ESVO, RGS
Организация(и): Федеральное государственное бюджетное образовательное учреждение высшего образования «Московская государственная академия ветеринарной медицины и биотехнологии ― МВА имени К.И. Скрябина» (ФГБОУ ВО МГАВМиБ ― МВА им. К.И. Скрябина) (109472, Москва, ул. Ак. К.И. Скрябина, д. 23).
Журнал: №6 - 2016
Глаукома на данный момент представляет собой тяжелую офтальмопатию, характеризующуюся повышенным внутриглазным давлением (ВГД) и поражением сетчатки и зрительного нерва. В ветеринарной офтальмологии глаукома является тяжело поддающимся лечению заболеванием, нередко приводящим к потере глаза, в силу различных обстоятельств. Но современный набор диагностического оборудования, а также широкий выбор противоглаукомных лекарственных средств позволяет эффективно контролировать данную патологию в течение длительного периода наблюдения. Основной задачей данной статьи является популяризация знаний, накопленных за длительный период работы в области ветеринарной офтальмологии по проблеме глаукомы у собак.
Ключевые слова: внутриглазное давление, внутриглазная жидкость, гидродинамика, глаукома, офтальмотонус, сетчатка, собака.
Сокращения: ВГД ― внутриглазное давление, ВГЖ — внутриглазная жидкость, ДЗН – диск зрительного нерва, ОКТ — оптическая когерентная томография, ПОУГ ― первичная открытоугольная глаукома, ПЗУГ ― первичная закрытоугольная глаукома, ПК – передняя камера, ПУГ ― постувеальная глаукома, УПК — угол передней камеры, ЭРГ – электроретинография.
Введение
В настоящее время как в медицине, так и в ветеринарии глаукому принято интерпретировать как группу хронических глазных заболеваний с различной этиологией, сопровождающихся периодическим или постоянным повышением внутриглазного давления (ВГД) с прогрессирующим поражением зрительного нерва и сетчатки и, как следствие, снижением зрительных функций. Буквально несколько десятилетий назад глаукому характеризовали только как заболевание, сопровождающееся повышением ВГД. Как известно, ведущим патогенетическим фактором при развитии глаукоматозного процесса является повышенное ВГД, связанное с нарушением оттока внутриглазной жидкости (ВГЖ) [10, 11, 12].
Диагностика глаукомы у собак нередко ограничивается исследованием офтальмотонуса. Однако одним из важнейших клинических признаков, сопровождающих глаукому, являются патологические изменения глазного дна, которые возможно исследовать при офтальмоскопии и фундоскопии, ультразвуковом исследовании, электроретинографии (ЭРГ) и др. [7, 10].
Несмотря на фундаментальные исследования, посвященные вопросам глаукомы у животных, малоизученной остается возможность медикаментозной терапии данной патологии, что обуславливает крайне низкую эффективность от рекомендаций врача-офтальмолога. Совместимость ЛС, режим дозирования, гипотензивный эффект, а также побочные реакции должны учитываться при назначении противоглаукомной терапии [8].
ГИДРОДИНАМИКА ГЛАЗА
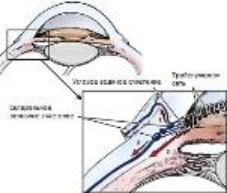
Циркуляция ВГЖ обеспечивает нормальный уровень ВГД у собак, а также доставку питательных веществ и удаление продуктов метаболизма из интраокулярных структур (хрусталик, стекловидное тело, роговица и др.). Помимо этого, водянистая влага обеспечивает прозрачность оптического аппарата и поддержание сферической формы глазного яблока. Нарушение циркуляции ВГД приводит к значительным патологическим изменениям, нарушению гидродинамического баланса, повышению офтальмотонуса и развитию глаукомы. Нормальное движение водянистой влаги осуществляется из задней камеры глаза в переднюю камеру (ПК) через отверстие зрачка и, затем, по дренажному аппарату угла передней камеры (УПК) в венозную систему глаза. Постоянная циркуляция ВГЖ происходит за счет разницы давлений в полостях глаза [6].
По разным литературным данным, нормальное ВГД у собак варьирует от 10 до 25 мм рт.ст. и зависит от таких факторов, как положение тела и психическое состояние животного. В работах Gelatt et al. (1981) отмечена суточная вариабельность ВГД: у собак в утренние часы офтальмотонус ниже, чем в вечерние, на 2–4 мм рт.ст. Также разница между левым и правым глазом одного и того же животного при тонометрии не должна превышать 5 мм рт.ст. [17].
Внутриглазная жидкость
ВГЖ образуется беспигментным эпителием отростков цилиарного тела из плазмы крови с помощью нескольких процессов: активной секреции, а также пассивных ультрафильтрации и диффузии. Секреция продуцирует 80–90% всего объема камерной влаги, а на пассивные процессы (ультрафильтрация и диффузия) приходится 10–20%.
ВГЖ на 99% состоит из воды, оставшуюся частью составляет хлор, карбонат, сульфат, фосфат, магний, натрий, калий, кальций, альбумины, глобулины, глюкоза, аскорбиновая и молочная кислоты, а также аминокислоты, ферменты, кислород и гиалуроновая кислота.
Камеры глаза
Первичная секреция водянистой влаги происходит в заднюю камеру глаза, которая расположена сзади радужной оболочки и ограничена хрусталиком, цилиарным и стекловидным телом. Из задней камеры ВГЖ через отверстие зрачка поступает в ПК. ПК глаза расположена между внутренней поверхностью роговицы и передней поверхностью радужной оболочки.
Основная функция камер глаза – это поддержание нормального взаимоотношения внутриглазных тканей, а также участие в проведении света до сетчатки и, кроме того, в преломлении световых лучей совместно с роговицей. Преломление световых лучей обеспечивается одинаковыми оптическими свойствами роговицы и внутриглазной жидкости.
Дренажная система глаза
Важной структурой ПК глаза является ее периферическая часть, где корень радужной оболочки переходит в цилиарное тело, а роговица – в склеру. Эта зона перехода образует УПК, через который осуществляется отток ВГЖ из ПК.
Дренажная система иридокорнеального угла представлена нитями гребенчатых связок, через которые водянистая влага из ПК поступает в цилиарную щель, содержащую трабекулярную сеть. После фильтрации между волокнами губчатой структуры сети ВГЖ попадает в узкое щелевидное пространство, угловое водяное сплетение. Оттуда камерная влага оттекает в эписклеральные и конъюнктивальные вены, а также в склеральные венозные сплетения, которые соединяются с системой вортикозных вен. Это основной путь оттока водянистой влаги, и он составляет у собак 85% от всего объема ВГЖ. Остальная часть (15%) выходит из глаза через увеосклеральный путь оттока, при этом влага поступает из УПК между цилиарным телом и хориоидеей, проходя вдоль мышечных волокон, и далее попадает в супрахориоидальное пространство, откуда оттекает непосредственно через склеру [13].
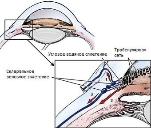
Движение жидкости через трабекулы выполняет еще одну важную функцию: промывание, очистку трабекулярного аппарата. В трабекулярную сеть поступают продукты распада клеток и пигментные частицы, кровь, которые удаляются с током ВГЖ. Установлено, что мелкие частицы, размером до 2–3 мкм, задерживаются в трабекулярной сети частично, а более крупные — полностью. Известно, что нормальные эритроциты, диаметр которых 7–8 мкм, проходят через трабекулярный фильтр свободно. Это связано с эластичностью эритроцитов и их способностью проходить через поры диаметром 2–2,5 мкм. Вместе с тем измененные и потерявшие эластичность эритроциты задерживаются трабекулярным фильтром [6, 28].
Очищение трабекулярного фильтра от крупных частиц происходит путем фагоцитоза. Фагоцитарная активность характерна для клеток трабекулярного эндотелия.
ЭТИОПАТОГЕНЕЗ ГЛАУКОМЫ
Глаукома у собак – это группа глазных заболеваний, сопровождающихся постоянным или периодическим повышением ВГД с последующим поражением диска зрительного нерва (ДЗН) и сетчатки и, как следствие, снижением зрительных функций. Рост офтальмотонуса связан непосредственно с нарушением циркуляции ВГЖ [6].
В соответствии с причиной, вызывающей гидродинамические нарушения, выделяют как первичную, так и вторичную глаукому.
Этиопатогенез первичной глаукомы
Первичная глаукома развивается самостоятельно в результате нарушения работы дренажного аппарата глаза и не является следствием другого окулярного заболевания. Как правило, первичная глаукома развивается билатерально, имеет строгую породную предрасположенность и является наследуемой патологией. Первичная глаукома у собак разделяется на две основные формы: первичная открытоугольная глаукома (ПОУГ) и первичная закрытоугольная глаукома (ПЗУГ), которые связаны с состоянием УПК – открытым или закрытым соответственно [11, 30].
ПОУГ у собак является редким заболеванием и встречается у таких пород собак, как бигль, норвежский элкхаунд. Данная форма первичной глаукомы является наследственной и развивается в основном у собак среднего возраста (4–7 лет). При гониоскопии УПК глаза остается открытым, а патологические процессы, приводящие к развитию глаукомы, происходят на микроструктурном уровне. Эти микроструктурные изменения связаны с мутацией гена ADAMTS10, который угнетает производство коллагена и нарушает функцию микрофибрилл в дренажном аппарате УПК. Как правило, эти патологические изменения развиваются в течение нескольких лет и, в конечном счете, приводят к разрушению структуры УПК, нарушению гидродинамики, повышению ВГД и развитию глаукомы [25, 30].
ПЗУГ у собак встречается в 8 раз чаще, чем ПОУГ, и характеризуется закрытым или узким УПК глаза. Отмечено, что у самок данная патология встречается в два раза чаще, чем у самцов. ПЗУГ, так же, как и ПОУГ, является породным заболеванием и наиболее часто встречается у американских и английских кокер спаниелей, бассетхаундов, чау-чау, самоедских лаек, сибирских хаски, немецких догов, прямошёрстных ретриверов и др. У этих пород собак отмечают нарушение структуры УПК при гониоскопии – закрытий или узкий. Важным фактором, обуславливающим развитие ПЗУГ, является задержка развития и дифференцирования УПК и дренажной системы в процессе эмбриогенеза. Вследствие этого в радужно-роговичном углу сохраняется мезенхимальная ткань, а также значительная гребенчатая связка (pectinate ligament). Данная патология получила названия дисплазии гребенчатой связки (pectinate ligament dysplasia), гониодисгенез или мезодермальный дисгенез. В результате закрытия иридо-корнеального угла происходит нарушение оттока ВГЖ через дренажную систему трабекулярной сети и повышение ВГД [26, 30].
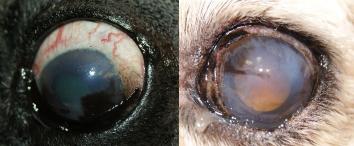
Этиопатогенез вторичной глаукомы
Вторичная глаукома развивается в результате сопутствующих патологий органа зрения (увеит, катаракта, гемофтальм и др.), которые, в свою очередь, вызывают нарушения гидродинамики глаза. Вторичная глаукома имеет несколько различных форм [15].
Одним из наиболее распространенных заболеваний, приводящих к развитию вторичной глаукомы, является воспаление сосудистой оболочки глаза. Развитие ПУГ происходит у собак, как правило, при длительном хроническом течении воспалительного процесса сосудистой оболочки – увеите. Повышение ВГД происходит в результате грубых поствоспалительных изменений: формирования задних и гониосинехий, структурных изменений дренажного аппарата, изменения состава вырабатываемой ВГЖ, разрушения гематоофтальмического барьера. Также возможно развитие зрачкового блока вследствие образования поствоспалительной спайки радужной оболочки с хрусталиком. В этом случае затрудняется циркуляция ВГЖ из задней камеры в ПК, происходит скопление водянистой влаги за радужной оболочкой, вызывая бомбаж последней. Все эти изменения приводят к нарушению баланса между выработкой и оттоком водянистой влаги и развитию вторичной ПУГ. Данная патология является наиболее тяжелой из всех видов вторичных глауком [9, 22].
Посттравматическая глаукома развивается на фоне тяжелых травм глазного яблока. Так, проникающие ранения могут привести к деструкции структур дренажного аппарата и рецессии УПК глаза. Немаловажную роль в таких случаях играют возможные повреждения хрусталика и радужной оболочки, которые являются значительным фактором риска развития глаукомы. Контузия глазного яблока в результате травмы нередко вызывает интраокулярные кровотечения и сопутствующие иридоциклиты. В таких случаях, из-за наличия в ПК глаза значительного количества фибрина и форменных элементов крови, происходит обструкция радужно-роговичного угла и повышение офтальмотонуса. Рецидивирующая гифема или прямое повреждение дренажной системы могут служить причиной повышения ВГД.
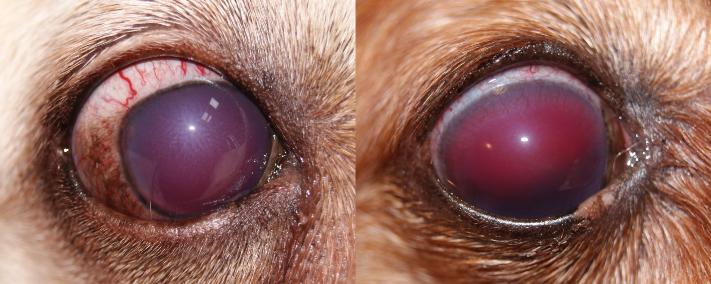
Вторичная глаукома, связанная с патологическим состоянием хрусталика, обозначается термином «факогенная глаукома» и имеет несколько различных форм.
Так, частичное или полное смещение хрусталика может спровоцировать повышение офтальмотонуса, поражение нейроретины и привести к развитию факотопической глаукомы. Дислокация хрусталика происходит в результате разрыва или ослабления цинновых связок, удерживающих его. Различают сублюксацию (подвывих) и люксацию (вывих) хрусталика. Подвывих характеризуется ослаблением или частичным разрывом цинновых связок. Для люксации характерны полное нарушение целостности связок и смещение хрусталика либо в ПК (частично или полностью), либо в стекловидное тело. Считается, что основная причина повышения ВГД при факотопической глаукоме – функциональный зрачковый блок в результате ущемления хрусталика в отверстии зрачка или смещении его в ПК и закрытии УПК глаза. Также может развиться витреальный блок – смещение стекловидного тела вперед из-за нарушения положения хрусталика, что, в свою очередь, ведет к скоплению и застою ВГЖ в заднем сегменте глаза и блокаде отверстия зрачка стекловидным телом [5, 16].
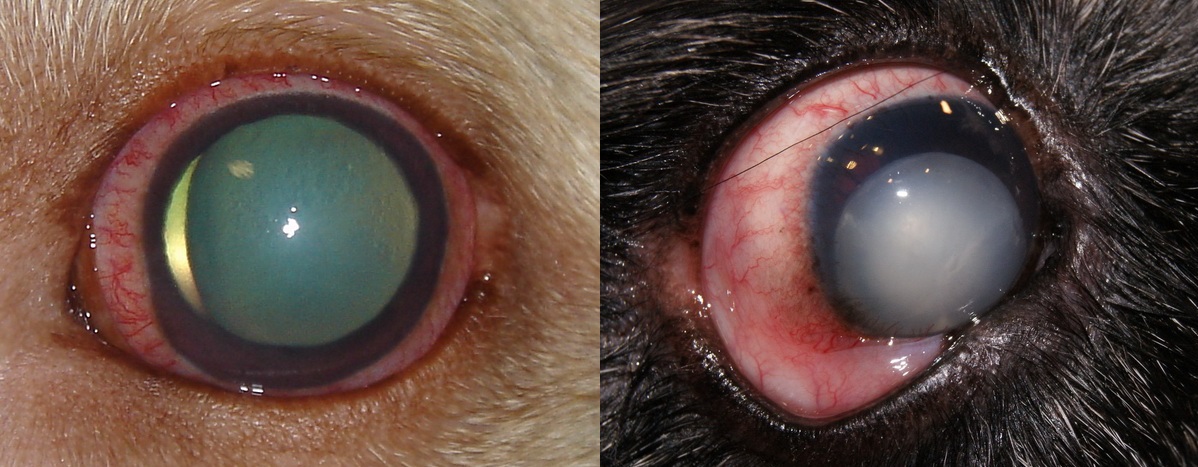
Повышение ВГД при факоморфической глаукоме развивается в результате увеличения размеров самого хрусталика и плотного прилегания задней поверхности радужной оболочки к последнему. Развивается зрачковый блок – ВГЖ, продуцируемая цилиарным телом, из задней камеры глаза в ПК не поступает. Это приводит к повышению давления в задней камере и выпячиванию радужной оболочки вперед. Происходит частичное или полное ущемление угла ПК глаза корнем радужной оболочки, отток водянистой влаги через дренажную систему радужно-роговичного угла затрудняется.
Разрыв капсулы хрусталика, а также лизис перезрелой катаракты может привести к развитию хрусталик-индуцированного увеита, закупорке УПК воспалительным экссудатом и хрусталиковым белком, формированием задних синехий. Такие патологические изменения в гидродинамической системе глаза могут привести к повышению ВГД и развитию вторичной факолитической глаукомы. В основе данной патологии лежит закрытие радужно-роговичного угла хрусталиковым белком и макрофагами, содержащими хрусталиковое вещество, а также воспалительным экссудатом. Это происходит из-за развития перезрелой катаракты и просачивания через капсулу хрусталика во ВГЖ протеинов, содержащихся в веществе хрусталика. В результате этого трабекулярные щели забиваются, что и служит причиной ухудшения оттока влаги через дренажную систему глаза и повышения ВГД [5, 16].
Основной причиной афакической глаукомы считается выпадение в ПК стекловидного тела, блокирующего зрачок и УПК. После экстракции катаракты у собак иногда возникает временное повышение ВГД или развивается вторичная афакическая глаукома. Реактивная гипертензия глаза, вызванная операционной травмой, сохраняется от нескольких часов до 2–3 дней. Более стойкое повышение офтальмотонуса и глаукома могут возникнуть в отдаленном периоде.
Ранняя афакическая глаукома обычно бывает следствием операционных и послеоперационных осложнений:
- • ущемление в ране или роговичное предлежание стекловидного тела;
- • блокада зрачка и колобомы радужки воздухом, экссудатом или стекловидным телом;
- • формирование гониосинехии
В более позднем периоде к афакической глаукоме могут привести:
- • рубцовые изменения в дренажной области склеры;
- • дистрофия в трабекулярной системе, отложение в ней пигмента;
- • сращение и заращение зрачка и колобомы радужки.
Однако возможно развитие и витреотопической формы афакической глаукомы, которая может проявляться в двух вариантах: 1) передний витреальный блок – выпадение стекловидного тела в ПК и возникновение грыжи блокирует зрачок и частично угол ПК; 2)задний витреальный блок – смещение вперед всего стекловидного тела с радужкой и задней капсулой хрусталика из-за нарушения оттока ВГЖ и скопления ее в ретровитреальном пространстве или в задних отделах стекловидного тела [1].
Пигментная форма вторичной глаукомы встречается достаточно редко и связана с синдромом пигментной дисперсии у собак породы золотистый ретривер. На раннем этапе данная патология характеризуется гиперпигментацией радужной оболочки, отложением пигмента на передней капсуле хрусталика и формированием тонкостенных кист в ПК глаза. В результате наличия свободного пигмента во ВГЖ происходит обструкция трабекулярной сети, нарушение гидродинамики глаза и повышение ВГД. По подобному механизму развивается меланоцитарная глаукома у керн-терьеров [30].
Образование меланом, аденом, аденокарцином цилиарного тела и радужной оболочки является частой причиной повышения офтальмотонуса из-за нарушения циркуляции камерной влаги и развития неопластической глаукомы. Формирование передних и гониосинехий, блокада УПК глаза продуктами распада опухоли, а также прорастание неоплазии в иридокорнеальную область являются основными патогенетическими факторами развития данной формы вторичной глаукомы [30].
ПАТОГЕНЕЗ ГЛАУКОМНОЙ ОПТИЧЕСКОЙ НЕЙРОПАТИИ (ГОН)
Поражение сетчатки и зрительного нерва является основным механизмом, приводящим к необратимой слепоте у собак при глаукоме [10].
Наиболее точно глаукому описывает J. Flammer (2001): «Глаукома – это прогрессирующая оптическая нейропатия, характеризующаяся экскавацией ДЗН и соответствующим ей снижением светочувствительности сетчатки». Из этого определения следует, что глаукома представляет собой, прежде всего, заболевание зрительного нерва и нейроретины, а повышенный офтальмотонус служит ведущим фактором риска развития данной патологии.
Под глаукомной оптической нейропатией понимают поражение самого глубокого ретинального слоя – ганглиозных клеток сетчатки, аксоны которых формируют зрительный нерв.
При повышении ВГД происходит механическое сдавливание аксонов зрительного нерва, входящих в состав нервных волокон, в отверстиях решетчатой пластинки склеры (lamina cribrosa scrlerae). Нарушается кровоснабжение и микроциркуляция ДЗН и сетчатки, развивается ишемия и гипоксия нервной ткани, образуется избыток свободных радикалов, происходит усиление перекисного окисления липидов. Нарушается работа K-Na-насоса и возникает деполяризация мембран клеток. В ответ на это происходит выброс глутамата, перевозбуждение глутаматных (NMDA) рецепторов и поступление избыточного количества ионов Са2+ в клетку, вызывая эксайтотоксическую гибель ганглиозных клеток сетчатки [24, 19].
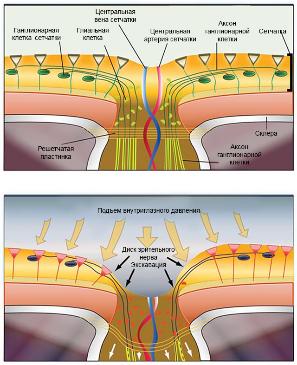
Немаловажным механизмом, усугубляющим развитие глаукомного поражения нейронов сетчатки, является реперфузия. Колебание ВГД оказывает наиболее разрушающее влияние на ткани глаза. Уменьшение кровоснабжения зрительного нерва и сетчатки приводит к острой нехватке кислорода в клетках, но восстановление питания приводит к избыточному поступлению O2 и накоплению свободных радикалов [10].
Как известно, наружные слои сетчатки получают питание от хориокапилляров, в то время как внутренние – от ретинальных сосудов. Поэтому развитие ретинальной ишемии и гипоксии оказывает разрушающее влияние на нейроретину [18].
В литературе значительное внимание уделяется роли нейротрофических факторов в патогенезе глаукомного поражения. Так, в результате повышения офтальмотонуса происходит блокада ретроградного аксонального транспорта и нарушается поступление нейротрофинов, в том числе BDNF (brain-derived neurotrophic factor), стимулирующего и поддерживающего жизнеспособность нейронов [12].
Таким образом, совокупность нескольких факторов (биомеханический, сосудистый и метаболический) запускает каскад реакций нейронального повреждения, приводящих к гибели сетчатки и атрофии ДЗН.
КЛИНИЧЕСКИЕ ПРИЗНАКИ ГЛАУКОМЫ
Глаукома у собак является результатом нарушения оттока и циркуляции ВГЖ. Так как офтальмотонус может повышаться до самых различных пределов и протекать от нескольких часов до нескольких месяцев, то и симптомы будут зависеть от длительности течения заболевания и уровня ВГД.
Все клинические симптомы глаукомы будут являться результатом повышения ВГД и воздействия его на глазное яблоко.

Рост офтальмотонуса выше 25 мм рт.ст. у собак является важным симптомом при диагностике глаукомы и основным предрасполагающим фактором. Также разница между левым и правым глазом одного и того же животного более 5 мм рт.ст. будет указывать на патологический процесс. В то же время, повышение ВГД в отсутствие других клинических признаков (изменения сетчатки ДЗН, снижение зрения) не подтверждает диагноз «глаукома» [15].
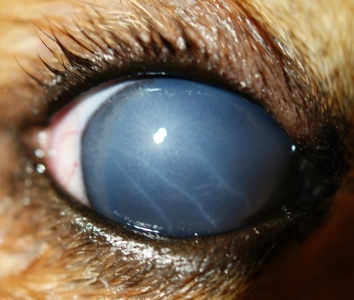
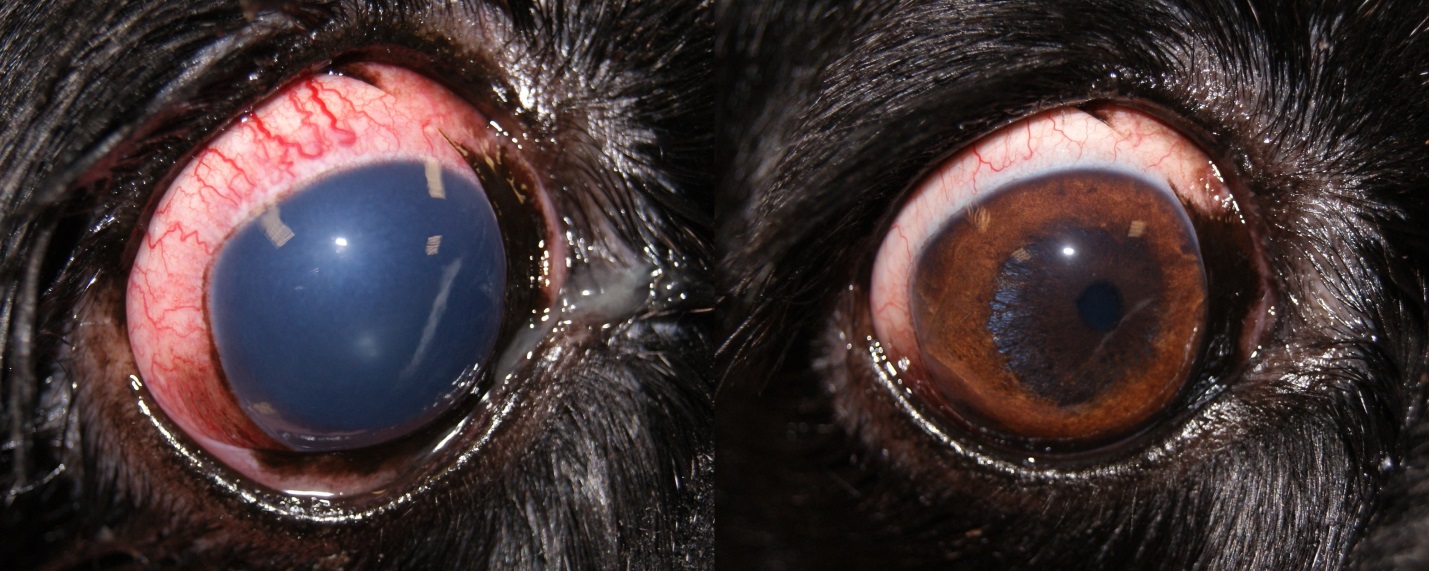
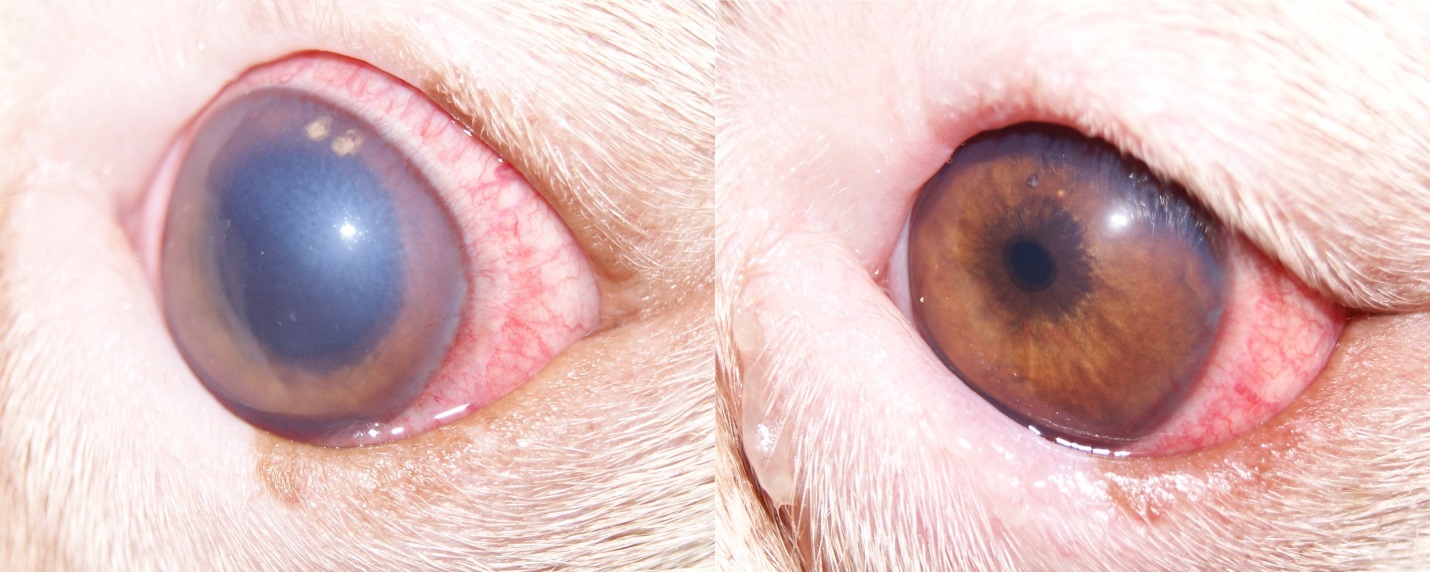
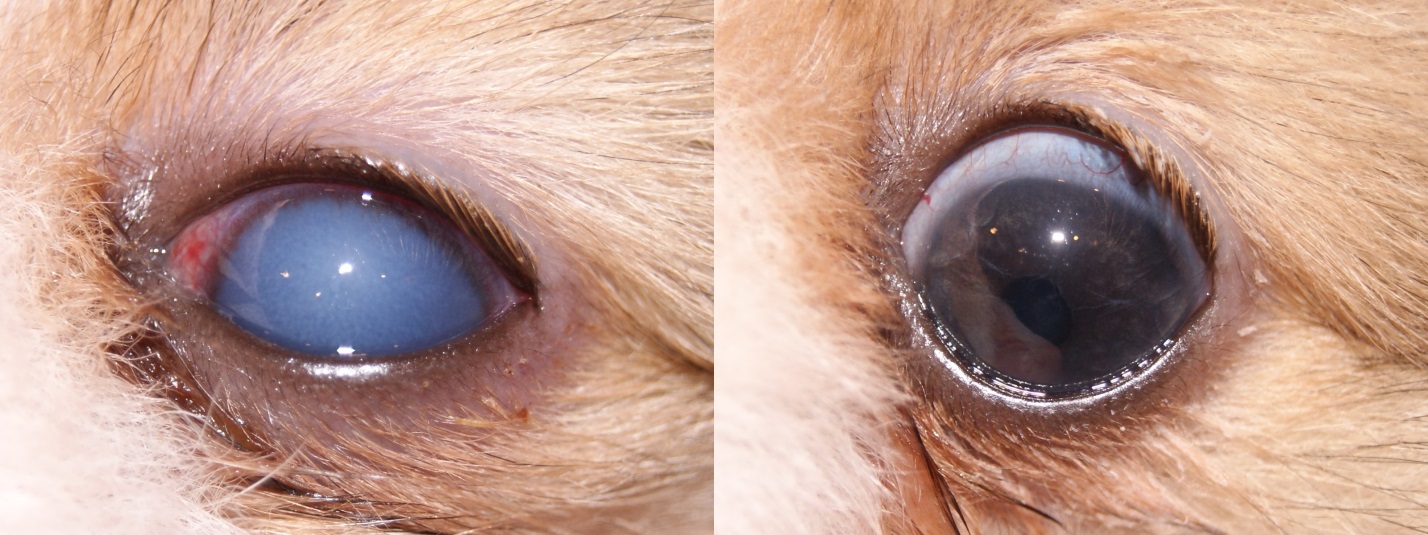
При повышении уровня офтальмотонуса до 50–60 мм рт.ст. у собак мы отмечали общее угнетенное состояние, снижение активности и аппетита, выраженный болевой синдром, блефароспазм, слезотечение. В запущенных случаях развивается увеличение глазного яблока в размерах в результате растяжения склеры и роговицы – буфтальм.
Застойные эписклеральные сосуды являются важным симптомом повышения ВГД и будут результатом нарушения оттока ВГЖ по вортикозным венамВ некоторых случаях можно отметить выраженную гиперемию и отек конъюнктивы, а также наличие смешанной инъекции сосудов.

Подъем уровня офтальмотонуса вызывает нарушение функции эндотелия роговицы и приводит к развитию корнеального эндотелиального отека. Также при разрыве десцеметовой оболочки могут наблюдаться единичные или множественные линейные дефекты на роговице (полосы Хааба).
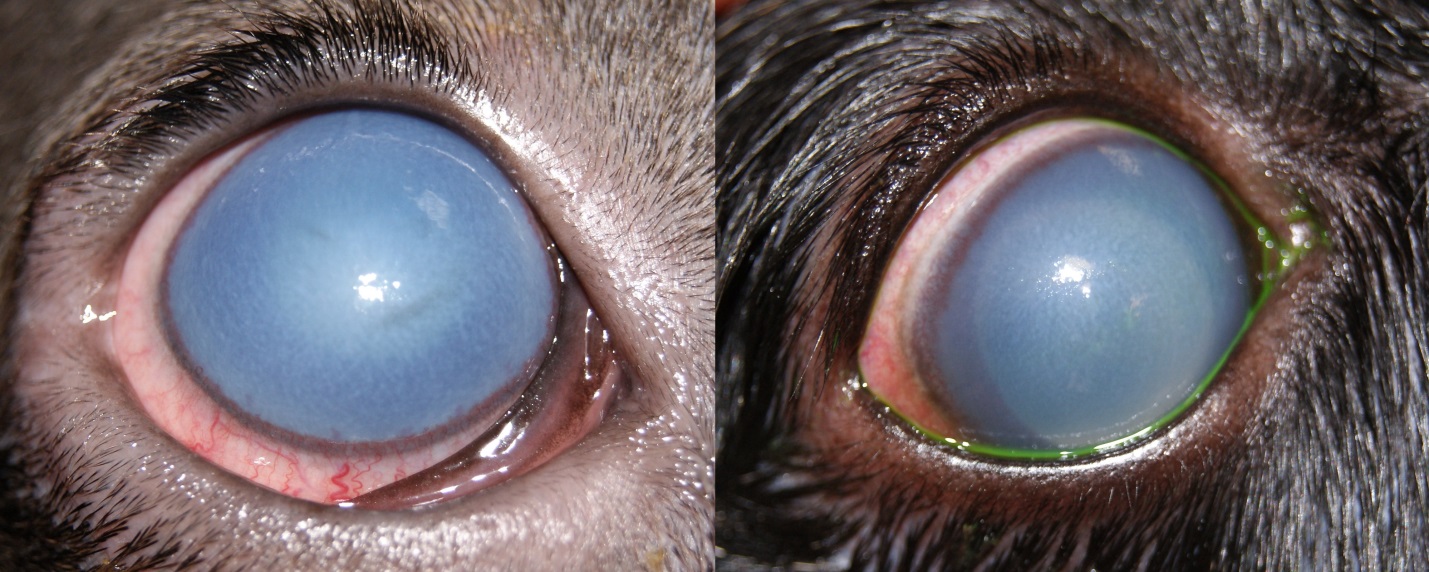
При хроническом течении глаукомы изменения роговицы могут включать в себя васкуляризацию, отложение пигмента (пигментозный кератит).
Уменьшение глубины ПК глаза является результатом застоя ВГЖ и отсутствия ее оттока, а также смещения хрусталика и радужной оболочки вперед.
На начальных стадиях глаукомы реакция зрачка на свет снижена. В запущенных стадиях, а также при остром приступе наблюдается значительный мидриаз. Такое состояние обусловлено несколькими причинами: поражением сетчатки и ДЗН, а также параличом мускулатуры зрачка.
Повышение ВГД может спровоцировать ослабление или разрыв цинновых связок, удерживающих хрусталик. В таком случае происходит частичное смещение (сублюксация) или вывих (люксация) хрусталика.
Снижение остроты зрения, вплоть до полной слепоты, будет являться необратимым результатом глаукомного процесса. Нами было отмечено, что длительное воздействие повышенного ВГД на структуры глазного яблока приводит к атрофическим изменениям в сетчатке и зрительном нерве. При исследовании глазного дна мы отмечали расширенную экскавацию ДЗН и, соответственно, уменьшение нейроретинального пояска. Данные изменения возникают в результате механического продавливания решетчатой пластинки склеры кзади на фоне подъема офтальмотонуса. Также отмечали гиперрефлексию тапетума (локальную в начальных стадиях заболевания, генерализованную в поздних стадиях) и истончение сосудов сетчатки. Это связано с механическим сдавливанием сосудистого пучка, проходящего через канал зрительного нерва, нарушением трофических функций сосудов сетчатки и развитием ишемии и гипоксии сетчатки [7].
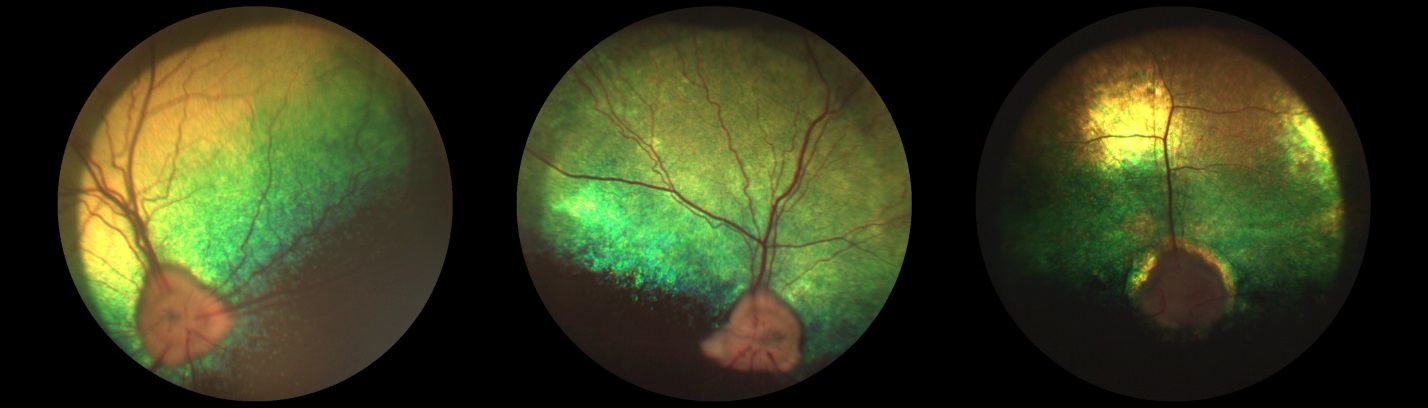
По нашему мнению, именно офтальмоскопические и функциональные изменения сетчатки являются основными при постановке диагноза «глаукома» у собак.
Для вторичной глаукомы также характерны симптомы, связанные с тем офтальмологическим заболеванием, которым она вызвана. Так, при ПУГ отмечается наличие гониосинехий, задних синехий, структурных изменений дренажного аппарата. Посттравматическая глаукома характеризуется наличием повреждений структур глазного яблока (хрусталик, радужка, роговица), интраокулярного кровотечения (гефема). Катаракта или люксация хрусталика могут быть клиническими признаками факогенной глаукомы, а отсутствие хрусталика – афакической [1, 2, 5]. Пигментная форма вторичной глаукомы характеризуется гиперпигментацией радужной оболочки, отложением пигмента на передней капсуле хрусталика и формированием тонкостенных кист в ПК глаза. При неопластической глаукоме отмечается наличие внутриглазных новообразований.
ДИАГНОСТИКА ГЛАУКОМЫ
В настоящее время диагностика глаукомы у собак недостаточно подробно описана в отечественной литературе по ветеринарии. Однако в иностранных источниках значительное внимание уделяется таким базовым методам исследования, как тонометрия, гониоскопия и офтальмоскопия. В медицинской практике широко используется биомикроскопия с помощью щелевой лампы, ЭРГ, ультразвуковое исследование глазного яблока. В последнее время значительное внимание уделяется цифровым методам исследования: фундус-фотографирование, оптическая когерентная томография.
Важную роль играет динамическое наблюдение за собаками с глаукомой, а также регулярный контроль ВГД.
Анамнестические данные
В диагностике глаукомы важная роль отводится сбору анамнеза. Данные о начале и продолжительности заболевания являются значимыми. Особое внимание рекомендуется уделять ранее перенесенным заболеваниям органа зрения, травмам и/или операционным вмешательствам в области глаза.
Первичный наружный офтальмологический осмотр
Необходимо уделять внимание первичному офтальмологическому осмотру и детальному обследованию переднего отрезка глаза, размеру и положению глазного яблока, состоянию конъюнктивальной и роговой оболочек, сосудам конъюнктивы и склеры. Также проводят тщательную оценку ПК глаза, радужной оболочки и хрусталика.
Биомикроскопия
По нашему мнению, при объективном исследовании глазного яблока можно выявить ряд характерных для данного заболевания признаков: застойная инъекция эписклеральных сосудов, отек роговицы и снижение ее чувствительности, мелкая ПК глаза, мидриаз, отсутствие реакции зрачка на свет. При биомикроскопии хрусталика оценивают его положение, размер, форму и прозрачность.
Тонометрия
Значительное место в вопросах, посвященных диагностике глаукомы, отводится тонометрии (измерение ВГД). Так как повышенный офтальмотонус – наиболее важный фактор риска развития глаукомы у собак, то определение величины ВГД имеет большое значение в диагностике данной патологии. В основном используются инструментальные методы измерения ВГД, такие как: аппланационная тонометрия по Маклакову, импрессионная тонометрия по Шиотцу и контактная электронная тонометрия Tonovet или Tonopen. По различным данным, нормальное ВГД у собак варьирует от 10 до 25 мм рт.ст. и зависит от таких факторов, как положение тела и эмоциональное состояние животного [30].
Гониоскопия
Следующим важным диагностическим исследованием является гониоскопия. Данное исследование позволяет оценить состояние УПК глаза с помощью специальной линзы – гониоскопа. В ветеринарной офтальмологии в основном используют линзы Гольдмана, Краснова, Ван-Бойнингена, Баркана, Koeppe. При гониоскопии оценивается УПК глаза – открытый, узкий и закрытый. В наших работах мы уделяли внимание ряду патологических изменений иридокорнеального угла: наличие гониосинехий, экссудата и пигмента, дистрофия трабекул, дисплазии гребенчатой связки [6].
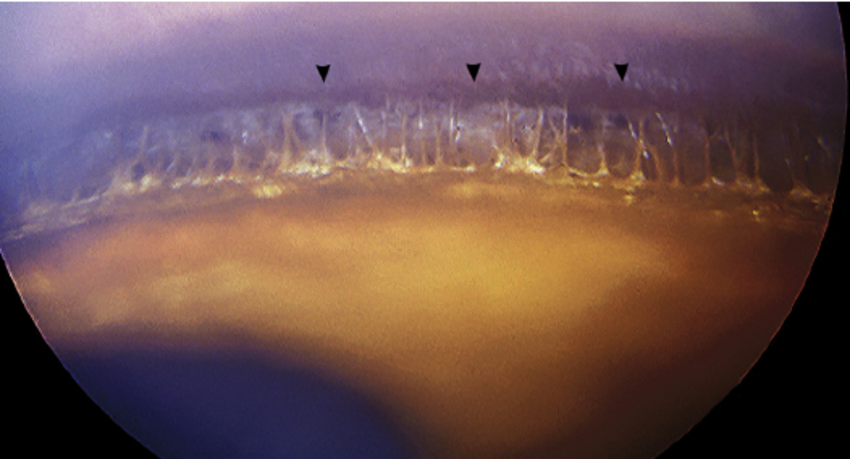
Офтальмоскопия
Для диагностики заднего сегмента глазного яблока широко используется метод прямой и непрямой офтальмоскопии. С помощью данного диагностического исследования возможно выявить изменения ДЗН и сетчатки. В многочисленных работах подчеркивается, что именно наличие глаукоматозной экскавации ДЗН является основным клиническим признаком глаукомы. В наших исследованиях мы рекомендуем значительное внимание уделять состоянию нейроретинального пояска и сосудов сетчатки.
Фундоскопия
По нашему мнению, именно исследование глазного дна играет ведущую роль в диагностике глаукомы, поэтому большое значение отдается детальной оценке структур сетчатки. Нами широко применялась фундоскопия, с возможностью фотографирования глазного дна. Результатом такого исследования будет мониторинг состояния ДЗН и сетчатки. С помощью данного метода можно на разных стадиях развития глаукомы оценить атрофию зрительного нерва и пигментного эпителия, повышение тапетальной рефлективности, истончение сосудов сетчатки, локализацию и величину ишемических очагов [7].

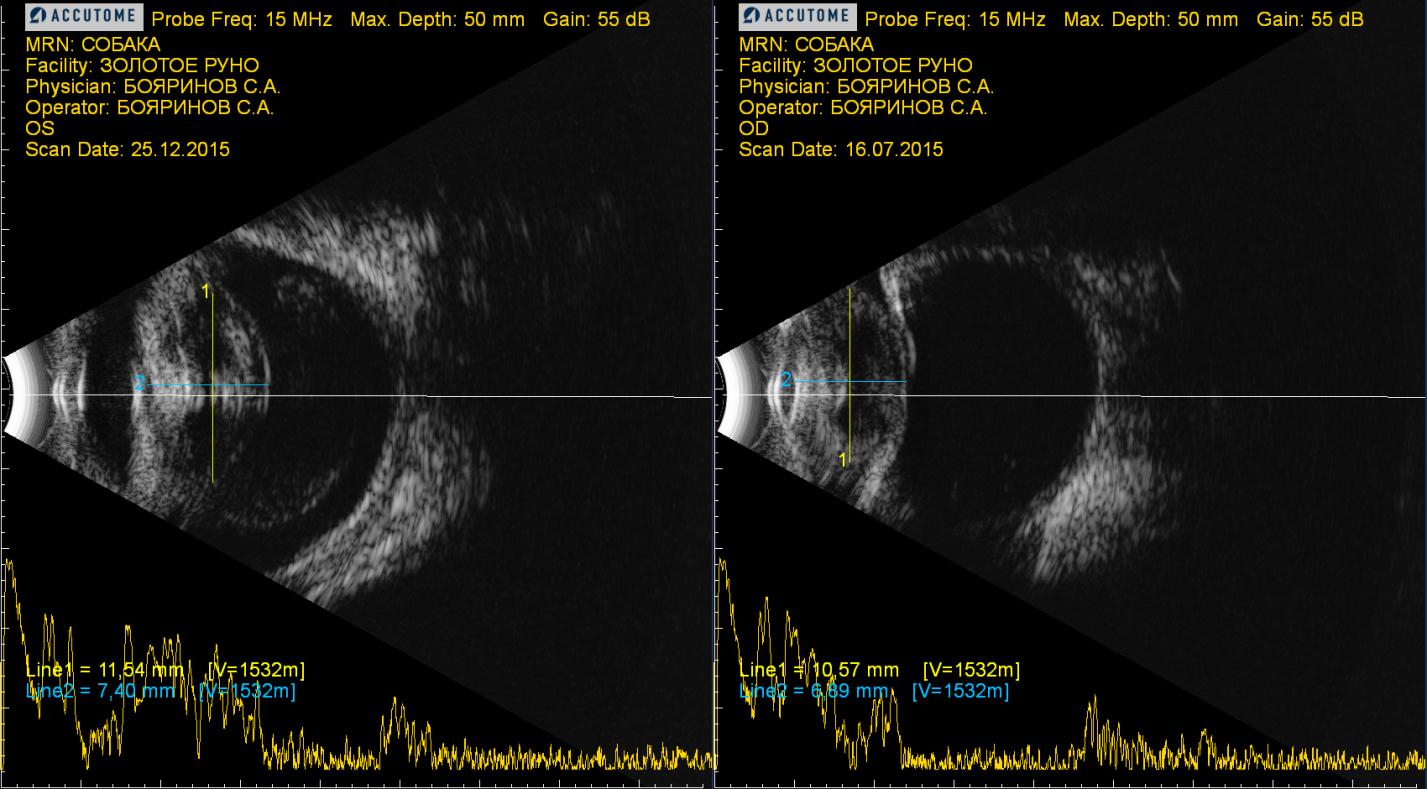
Ультразвуковое исследование глазного яблока
Многие авторы уделяют внимание ультразвуковому исследованию глазного яблока при глаукоме. Для этого используются датчики с частотой 10–15 MHz в A- и B-режимах. Исследуют размеры глазного яблока, положение и размеры хрусталика, состояние стекловидного тела и сетчатки [3].
Ультразвуковая биомикроскопия
В последнее время широко применяется метод ультразвуковой биомикроскопии (УБМ) для диагностики глаукомы. Данный вид исследования дает возможность детально визуализировать передний сегмент глаза на микроструктурном уровне. Ультразвуковая биомикроскопия проводится датчиками с разрешением 50–80 MHz и позволяет получить информацию о состоянии ПК глаза, оценить ее глубину, оценить структуру УПК, исследовать пути оттока ВГЖ [19].
Оптическая когерентная томография
В иностранной литературе по ветеринарной офтальмологии описано применение метода оптической когерентной томографии (ОКТ) у животных. Эта бесконтактная неинвазивная технология позволяет исследовать морфологию заднего отрезка глаза in vivo. Высокая разрешающая способность ОКТ дает возможность получить цифровые изображения сетчатки, ДЗН в режимах 2D и 3D и выявить изменения слоя нервных волокон и наличие глаукоматозной экскавации ДЗН [18, 20].

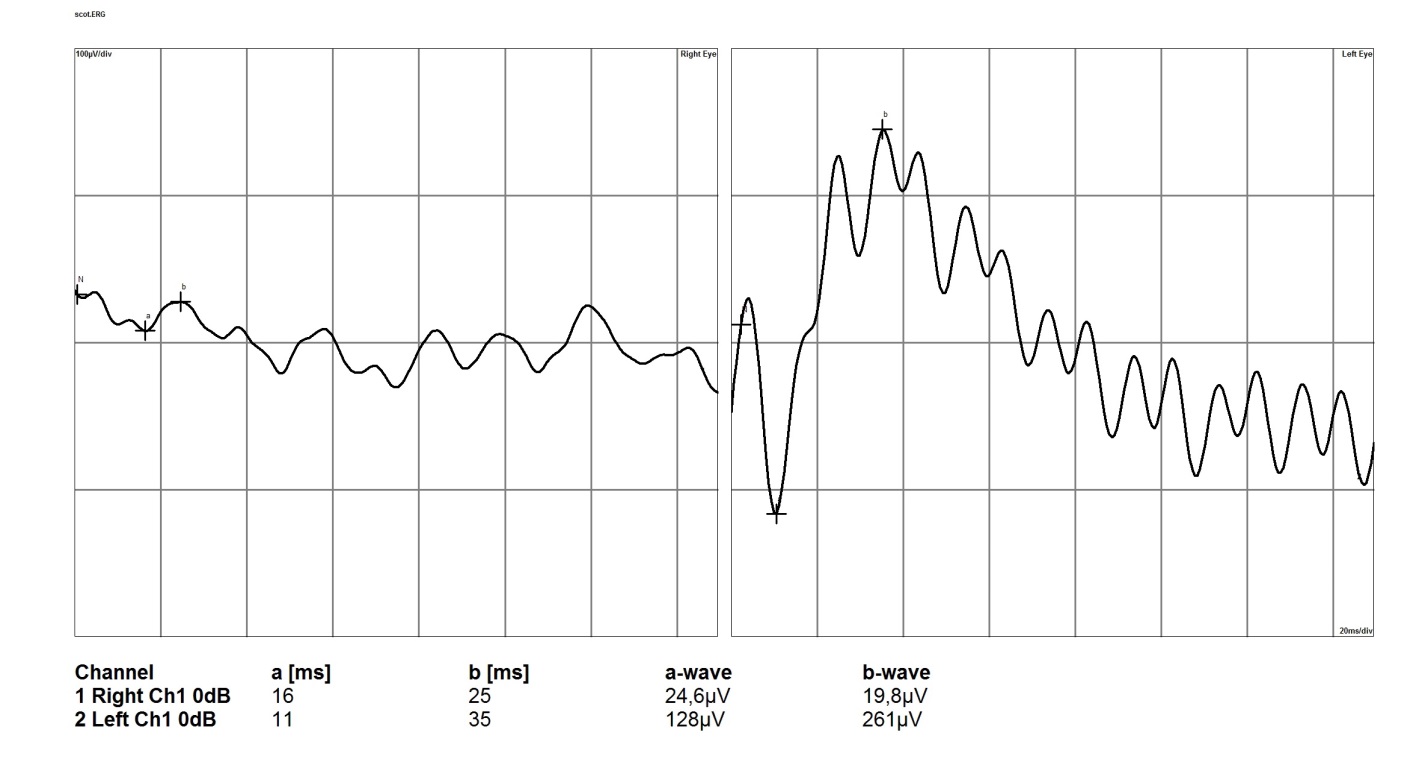
Электроретинография
Для оценки состояния зрительных функций, а именно для определения функциональной активности сетчатки используется метод ЭРГ. Сущность данного метода заключается в регистрации биопотенциалов клеток сетчатки в ответ на световой раздражитель. Различают несколько видов ЭРГ для диагностики глаукомы: общая, ритмическая, паттерн-ЭРГ и осцилляторные биопотенциалы. Эти методы позволяют выявить ранние нарушения функции сетчатки еще до появления визуальных изменений. Так, при начальных поражениях ганглионарных клеток сетчатки общая ЭРГ будет нормальной или супернормальной, в то время как паттерн-ЭРГ будет снижена. В продвинутых стадиях глаукоматозного процесса наблюдается угнетение всех биопотенциалов сетчатки, вплоть до отсутствия ответа на световой раздражитель [14].
МЕДИКАМЕНТОЗНОЕ ЛЕЧЕНИЕ ГЛАУКОМЫ
Медикаментозная терапия глаукомы у собак является базовым мероприятием в снижении ВГД. Даже в случае запущенной патологии необходимо руководствоваться знаниями о возможностях местного гипотензивного лечения. В отдельных случаях назначение ЛС, снижающих ВГД, будет необходимым звеном при подготовке пациента к хирургическому или лазерному лечению [5].
В основе местной гипотензивной терапии при глаукоме лежат следующие принципы:
- • лечение основного заболевания (если глаукома вторичная);
- • снижение ВГД;
- • улучшение кровоснабжения сосудистого тракта и защита клеток сетчатки от воздействия повреждающих факторов – нейропротекция.
При выборе местной гипотензивной терапии ветеринарный врач должен быть уверен в точности диагноза. Одно из условий успешной терапии ― постоянный мониторинг ВГД. Желательно использовать минимальное число лекарственных средств при максимальной эффективности и учитывать эффект тахифилаксии (привыкания) и побочные реакции [8, 11, 27].
Алгоритм лечения глаукомы
- • Монотерапия гипотензивным лекарственным средством.
- • При неэффективности назначенной монотерапии и/или запущенности патологии заменяют выбранный препарат на лекарственное средство другой фармакологической группы или назначают комбинированную терапию.
- • Не следует применять препараты одной фармакологической группы.
- • Необходимо регулярно измерять ВГД, чтобы оценить эффективность местной гипотензивной терапии.
Современные лекарственные средства, предназначенные для снижения офтальмотонуса при глаукоме, по механизму действия подразделяют на две основные группы:
- 1. лекарственные средства, улучшающие отток ВГЖ;
- 2. лекарственные средства, угнетающие продукцию ВГЖ.
Препараты, улучшающие отток ВГЖ
Простагландины (синтетические аналоги простагландинов F2α)
- • Латанопрост 0,0005%;
- • Травопрост 0,004%
Препараты данной фармакологической группы эффективно снижают офтальмотонус за счет стимуляции простагландиновых рецепторов и развития миоза, тем самым улучшая увеосклеральный путь оттока ВГЖ.
С осторожностью применять при увеальной офтальмогипертензии и ПУГ, а также при любых воспалительных заболеваниях сосудистой оболочки глаза.
М-холиномиметики
Пилокарпин 1%, 2%, 4%. Гипотензивный эффект связан со стимуляцией М-холинорецепторов вегетативной нервной системы. Происходит сокращение сфинктера зрачка и цилиарной мышцы, развивается медикаментозный миоз. За счет этого раскрывается УПК и улучшается отток водянистой влаги.
С осторожностью применять при увеальной офтальмогипертензии и ПУГ, а также при воспалительных заболеваниях сосудистой оболочки глаза.
Препараты, угнетающие продукцию ВГЖ
Неселективные β1,2-адреноблокаторы
Тимолол 0,25%, 0,5%. Снижение ВГД наступает в результате блокирования β-адренорецепторов цилиарного тела и, соответственно, снижения секреции ВГЖ.
С осторожностью применять при патологиях сердечно-сосудистой системы, особенно у животных массой менее 10 кг.

Селективные β1-адреноблокаторы
Бетаксолол 0,25%, 0,5%. Снижение ВГД наступает в результате блокирования β1-адренорецепторов цилиарного тела и, соответственно, снижения секреции ВГЖ.
Бетаксолол является блокатором кальциевых каналов, ограничивая поступление ионов кальция в клетку, защищая ее от гибели, тем самым улучшая микроциркуляцию сетчатки и ДЗН, что обуславливает его прямой нейропротекторный эффект.
С осторожностью применять при патологиях сердечно-сосудистой системы, особенно у животных массой менее 10 кг.
α- и β-адреноблокаторы
Бутиламиногидроксипропоксифеноксиметилметилоксадиазол 1%, 2%. Лекарственные средства данной фармакологической группы снижают офтальмотонус за счет блокирующего влияния на β1,2-α1-адренорецепторы, тем самым угнетая продукцию ВГЖ.
Селективные α2-адреномиментики
- • Клонидин 0,125%, 0,25%, 0,5%.
- • Бримонидин 0,15%, 0,2%.
Гипотензивный эффект обусловлен стимуляцией α2-адренорецепторов и активацией рецептора G-белка, которые ингибируют активность аденилатциклазы. Это снижает концентрацию цАМФ и, следовательно, секрецию ВГЖ цилиарным телом.
Бримонидин также улучшает увеосклеральный путь оттока [31]. Бримонидин обладает прямыми доказанными нейропротекторными свойствами путем ингибирования каскада апоптозных изменений. С осторожностью применять при патологиях сердечно-сосудистой системы, а также у животных массой менее 10 кг (выраженный системный гипотензивный эффект).
Ингибиторы карбоангидразы (ИКА)
- • Бринзоламид 1%.
- • Дорзоламид 2%.
В результате ингибирования активности карбоангидразы II в отростках цилиарного тела нарушается образование ионов бикарбоната, с последующим снижением концентрации натрия и транспорта жидкости. Происходит угнетение продукции ВГЖ и снижение офтальмотонуса. Имеются данные, что ингибиторы карбоангидразы улучшают глазничное кровоснабжение, что позволяет рассматривать их как препараты с нейропротекторным действием. При длительном и частом применении ИКА могут нарушать состоятельность эпителия роговицы.
НЕЙРОПРОТЕКЦИЯ ПРИ ГЛАУКОМЕ
Стабилизация ВГД является основной целью терапии глаукомы. Однако стоит учитывать тот факт, что даже при нормализации офтальмотонуса зрительные функции у собак значительно снижаются. Прежде всего, это связано с комплексным воздействием на сетчатку и ДЗН повреждающих факторов и развитием глаукомной оптической нейропатии. В связи с этим, защита ганглиозных клеток сетчатки является важным аспектом в комплексном лечении глаукомы у собак [10].
Под нейропротекцией понимают защиту нейронов сетчатки и волокон зрительного нерва от воздействия повышенного ВГД и ишемии. Коррекция метаболических нарушений, улучшение микроциркуляции и трофики тканей, а, в конечном счете, предотвращение необратимой гибели ганглиозных клеток сетчатки является основной целью нейропротекции при глаукоме [12].
В нейропротекции принято различать прямое и опосредованное действие ЛС. Прямые нейропротекторы подразделяют на первичные (действие направлено на прерывание ранних процессов ишемического каскада) и вторичные (прерывание отсроченных механизмов гибели нейронов).
К первичным прямым нейропротекторным ЛС относят препараты, блокирующие NMDA-рецепторы, ингибиторы синтеза пресинаптического высвобождения глутамата.
Глицин является первичным нейропротектором; это активатор тормозной нейротрансмиссии, тормозит передачу импульсов на NMDA-рецепторы в условиях их перевозбуждения при ишемии. Связываясь с глициновыми рецепторами, оказывает «тормозящее» воздействие на нейроны, уменьшает выделение из нейронов «возбуждающих» аминокислот, таких как глутаминовая кислота, и повышает выделение ГАМК. Помимо прочего, глицин обладает общеметаболическим, ноотропным и антистрессовым действием, что, при его минимальных побочных эффектах, позволяет рассматривать его как препарат выбора при лечении ГОН у собак.
Сегодня доказано, что прямым нейропротективным действием обладают блокаторы кальциевых каналов (БКК), к которым относят амлодипин, верапамил, нифедепин [23]. Так, данные ЛС блокируют кальциевые каналы пресинаптической мембраны, препятствуют избыточному входу ионов кальция внутрь терминали аксона и избыточному выбросу нейромедиатора глутамата в синаптическую щель, а также снижают сосудистое сопротивление в артериях сетчатки. Препараты группы БКК сегодня широко известны в ветеринарной кардиологической и неврологической практике. Отрицательная сторона лечения препаратами данной группы — наличие побочных эффектов, связанных со снижением артериального давления у животных.
ЛС, воздействие которых осуществляется на отсроченные механизмы гибели нейронов, называют вторичными нейропротекторами. К ним относят антиоксиданты, пептидные биорегуляторы. Преимущество данного направления нейропротекторной терапии — незначительные побочные эффекты и комплексное действие.
В нашей клинической практике широко применяется лекарственный препарат Мексидол-вет - сукцинат-2-этил-6-метил-3-оксипиридина, в форме таблеток или раствора для инъекций из расчета 20 мг на 1 кг веса 2–3 раза в день, первые 7 дней, затем 10 мг на 1 кг веса 2–3 раза в день – 21 день. Мексидол-вет обладает поликомпонентными фармакологическими свойствами антиоксиданта, реализуемыми, по крайней мере, на двух уровнях – нейрональном и сосудистом. Так, он обеспечивает угнетение процессов свободно-радикального окисления внутри клетки, ингибирование процессов перекисного окисления липидов, активное взаимодействие с первичными и гидроксильными радикалами, снижение повышенного уровня оксида азота, ингибирование кальций-независимой фосфодиэстеразы, вследствие чего повышается концентрация цАМФ в тканях, торможение гликолитического процесса. Важным моментом, по нашему мнению, является различные пути введения Мексидола-вет, разнообразие лекарственных форм, отсутствие значимых побочных эффектов при применении. Существуют также данные о положительном влиянии Мексидола-вет на сетчатку и ДЗН при парабульбарном введении 0,5 мл (0,25 мг) 5% раствора препарата 1 раз в день в течение 10–12 дней [33, 34, 35].
На сегодняшний день существуют данные о положительном нейропротекторном влиянии местных антиглаукомных гипотензивных препаратов на состояние сетчатки и ДЗН.
Так, бримонидин за счет ингибирования каскада апоптозных изменений и блокады поступления ионов кальция в нервные клетки повышает жизнеспособность в условиях ишемии. Также предполагается, что он снижает глутамат-индуцированную эксайтотоксичность или повышает экспрессию нейротрофина BDNF [21].
Нейропротективными свойствами обладает селективный β1-адреноблокатор бетаксолол, блокирующий поступление ионов кальция в ганглионарные клетки и улучшающий кровоснабжение в ДЗН [29].
Ингибиторы карбоангидразы (дорзоламид, бринзоламид) при местном применении оказывают вазодилатирующий эффект на сосуды сетчатки и улучшают глазничный кровоток [29]. Важным аспектом нейропротекции при глаукоме у собак является достижение стабильного толерантного ВГД, в противном случае эффективность терапии, направленная на защиту клеток сетчатки, значительно снижается.







Назад в раздел

















